Kimya, maddenin yapısını, özelliklerini, birleşimlerini, etkileşimlerini, tepkimelerini araştıran ve uygulayan bilim dalıdır. Kimya bilmi daha kapsamlı bir ifadeyle maddelerin özellikleriyle, sınıflandırılmasıyla, atomlarla, atom teorisiyle, kimyasal bileşiklerle, kimyasal tepkimelerle, maddenin hâlleriyle, moleküller arası ve moleküler kuvvetlerle, kimyasal bağlarla, tepkime kinetiğiyle, kimyasal dengenin prensipleriyle vb konularla ilgilenir. Kimyanın en önemli dalları arasında analitik kimya, anorganik kimya, organik kimya, fizikokimya ve biyokimya sayılır.

Mineral, doğal şekilde oluşan, homojen, belirli kimyasal bileşime sahip inorganik kristalleşmiş katı bir maddedir. Buna göre minerallerin özellikleri şöyledir; doğal olarak oluşur, herhangi bir parçası bütününün özelliklerini taşır, belirli bir kimyasal formülü vardır, katı hâlde olup nadiren sıvıdır ve inorganiktir.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.

Alkanlar, (diğer bir deyişle Parafinler) sadece karbon (C) ve hidrojen (H) elementlerinin bulunduğu ve bu elementlerin birbirleriyle tekli bağ yaptığı doymuş alifatik organik bileşiklerin genel ismidir. Alkanlar birbirlerini 1 karbon ve 2 hidrojen ile takip eden bir homolog seri oluştururlar. Örneğin tek karbonlu metan, CH4 formülüne sahipken, çift karbonlu etan C2H6 kapalı formülüne sahiptir. Alkanlarda tüm atomlar tekli bağlarla birbirlerine bağlandığı ve Karbon atomunu bağlayabileceği en fazla Hidrojen atomunu bağladığından dolayı doymuş bileşikler kategorisine girerler. Doymuş hidrokarbonlardan olan alkanlar, CnH2n+2 n=1,2,3,.... genel formülüne sahiptir. Burada n'in 3 veya 3'ten büyük olması hâlinde sikloalkan denilen halkalı yapılar oluşabilmektedirler.
Deoksiriboz veya bilinen adlarıyla D-Deoksiriboz ve 2-deoksiriboz, beş karbon atomu içeren ve aldehit grubu barındıran aldopentozların bir üyesidir. Deoksiriboz, penton riboz şekerinin 2 pozisyonundaki hidroksil grubunun hidrojen ile yer değiştirmesiyle oluşur, yani bu bir oksijen atomunun kaybı ile sonuçlanır. Hidroksil grubunun değişmesi aynı zamanda, halka yapısını C3'-endo pozisyonundan C2'-endo olacak şekilde değiştirir. Bu molekül, 1929 yılında Phoebus Levene tarafından keşfedilmiştir ve DNA nükleik asidinin önemli bir yapıtaşıdır.

Alkol, karbon atomuna doğrudan bir -OH (hidroksil) grubunun bağlı olduğu organik bileşiklere verilen genel ad. Genel formülü CnH2n+1OH olan mono alkoller, alkollerin önemli bir sınıfıdır. Bunlardan etanol (C2H5OH), alkollü içeceklerde bulunan türüdür. Genellikle alkol kelimesi ile etanol kastedilir ki yeni fermente olmuş birada etanol oranı %3-5 arasında iken şarapta %12-15 arasındadır.

Alkenler yapılarında en az bir tane karbon-karbon (C=C) çift bağı içeren organik bileşiklerdir. Alkenlerin yapısında karbon-karbon çift bağı bulunduğundan ve bu karbonların yapabileceği en fazla hidrojenle bağ yapmamış olduğundan alkenler doymamış bileşikler kategorisine girerler. Alkenlerin yapısında sadece bir karbon-karbon çift bağının bulunması durumunda homolog seriler oluşturur. Bu homolog serilerin genel formülü CnH2n şeklindedir. Burada n-in en az 2 olma şartı vardır. Aşağıda en basit alken olan eten, yaygın ismiyle etilenin, çeşitli modellemelerle çizilmiş şekillerinin yanı sıra alkenlerin çeşitli şekillerdeki yazılış şekilleri de bulunmaktadır.

Maltoz (malt şekeri veya di-glikoz olarak da bilinir), C12H22O11 moleküler formüllü bir disakkarittir. Sistematik ismi α-D-Glukopiranozil-(1→4)-α-D-Glukopiranoz'dur. Maltoz suda iyi çözülür ve tatlı bir tadı vardır. Eğer Maltozu Sakkarozla karşılaştıracak olursak %10 D-Maltozun tatlılık derecesi %41'lik Sakkarozunkine denk gelmektedir. Suda çözülmüş Maltozun kristalleştirilmesiyle monohidratlar oluşmaktadır. Aynı zamanda maltoz çimlenmiş arpada ve patatesin tohumlarında da görülmektedir.
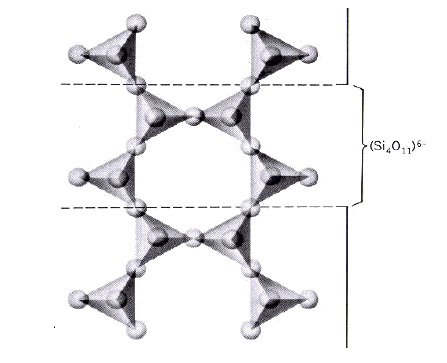
Mika bir düzleme göre çok iyi dilinimli bir takım mineralleri içeren bir mineraller grubudur. Dilinim (şistozite), yaprakcıkları elastik olarak bükülebilir. Dilinim yüzeyleri sedef parıltıdır. Mika grubu mineraller, yer kabuğunu oluşturan kayaçlar içerisinde ortalama % 3.8 oranında dağılım frekansına sahiptir.

Silikat, mineral grupları arasında en geniş gruptur.

Piroksen, mantonun önemli bileşenlerinden biri olduğu sanılan, magmatik ve metamorfik taşlarda sıkça rastlanan karmaşık bir inosilikat mineral grubudur.

Olivin, yüksek sıcaklık silikat minerali ailesidir. Rengi siyahtan zeytin yeşiline değişir. Olivin adını, tephroit (Mn2SiO4), monticellit (CaMgSiO4), larnit (Ca2SiO4) ve kirschsteinite (CaFeSiO4)içeren mineraller grubuyla ilgili bir yapıya denir. Ortorombik simetride kristalleşen olivin grubu minerallerden (Mg,Fe)-olivinlerde Mg2SiO4 ve Fe2SiO4 uç üyeleri arasında tam bir katı çözelti oluştururlar. Ayrıca Fe ve Mn olivinler arasında da sürekli bir seri bulunmaktadır.. Ultrabazik ve bazik kayaçlarda görülen önemli bir mafik mineraldir. Dünit adı verilen ultrabazik kayalar %90,100 olivinden oluşur. Dolomitik Kireç taşı bölgesel ve kontak metamorfizmaları sırasında yüksek dereceli metamorfizma koşullarında forsterit bakımından zengin olivinler oluşur. Olivinlerin kimyasal bileşimleri -plajioklaslarda An (anortit) cinsinden olduğu gibi- içerisinde barındırdığı forsterit (Fo) yüzdesi ile ifade edilir. Örneğin Fo47 şeklindeki bir ifade mineralin % 47 forsteritten, % 53 fayalitten oluştuğunu gösterir.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.

Magma, yeraltında bulunan, ergimiş haldeki kayaçlar. Kayaçların basınç düşmesi, sıcaklık yükselmesi, H2O ilavesi gibi etkenler altında erimesi sonucu oluşan silikat hamuru durumundaki eriyiklerdir. Yeryüzüne ulaşarak yanardağlardan püsküren magmaya lav denir. Magma, dünya yüzeyinin altında bulunur ve diğer karasal gezegenlerde ve bazı doğal uydularda da magmatizmanın kanıtı keşfedilmiştir. Erimiş kayanın yanı sıra, magma ayrıca kristaller ve volkanik gazlar içerebilir.
Oksit, içeriğinde en az bir adet oksijen atomu ve en az bir adet başka element içeren bileşiklere verilen genel isimdir. Soy gazlar oksitleri oluşturmazlar. OF2 ve KMnO4 oksit değildir.
Bilinen inorganik ve organometalik bileşiklerin elementlere göre sıralanmış listesidir. Sıralama elementlerin kısaltmalarının alfabetik sırasına göredir.

Ayrışma, çözünme veya günlenme, yerkabuğunu oluşturan kayaçların yüzey kısımlarında fiziksel ve kimyasal etkenlerle meydana gelen değişimlerdir. Bu etkenlerin yanında atmosferdeki gazlar, sıcaklık, su, organizmalar da ayrışmada etkilidir.
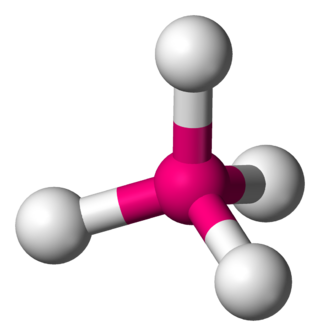
Dörtyüzlü veya tetrahedral molekül geometrisi, merkezi atomun, dört yüzlünün ortasında, dört köşede ise sübstitüentlerin yer aldığı molekül geometrisidir. Bağ açıları, dört sübstitüent aynı olduğunda (örn. metan CH4 ya da daha ağır analogları) cos−1 (-⅓) = 109,4712206 ...° ≈ 109.5° olur. Metan veya diğer simetrik yüzlü moleküller Td nokta grubuna aittir, ama dörtyüzlü moleküller genellikle düşük simetriye sahiptir. Tetrahedral moleküller kiral olabilir.

Amfibol, çift zincirli SiO'dan oluşan prizma veya iğne benzeri kristallerden oluşan önemli bir inosilikat mineral grubudur.

Kimyada, oktahedral moleküler geometri, bir oktahedronun köşelerini tanımlayan, merkezi bir atom etrafında simetrik olarak düzenlenmiş altı atomlu bileşiklerin veya atom gruplarının veya ligandların şeklini tanımlar. Oktahedronun sekiz yüzü vardır, dolayısıyla octa ön ekini alır. Oktahedron, Platonik katılardan biridir, ancak oktahedral moleküller tipik olarak merkezlerinde bir atom içerir ve ligand atomları arasında bağ yoktur. Mükemmel bir oktahedron Oh nokta grubuna aittir. Oktahedral bileşiklerin örnekleri arasında kükürt hekzaflorür SF6 ve molibden hekzakarbonil Mo (CO)6 gösterilebilir. "Oktahedral" terimi, kimyagerler tarafından, merkezi atoma olan bağların geometrisine odaklanarak ve ligandların kendi aralarındaki farklılıkları dikkate almadan biraz gevşek bir şekilde kullanılır. Örneğin, N-H bağlarının oryantasyonu nedeniyle matematiksel anlamda oktahedral olmayan [Co(NH3)6]3+, oktahedral olarak adlandırılır.