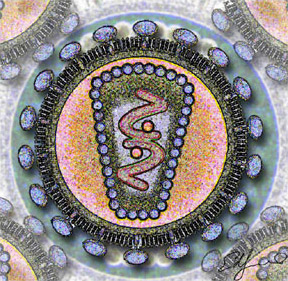
Viral protein

Viral protein, virüsün hem bir bileşeni hem de bir ürünüdür. Viral proteinler işlevlerine göre yapısal proteinler, yapısal olmayan proteinler, düzenleyici ve yardımcı proteinler olarak gruplandırılırlar.[1] Virüsler canlı değildir (Canlı olduklarını kabul eden araştırmacılar da vardır) ve kendi başlarına çoğalma araçlarına sahip değildirler. Çoğalmak için konakçı hücrelerinin enerji metabolizmalarına, enzimlerine ve yapı öncüllerine bağlıdırlar. Bu nedenle, virüsler kendi viral proteinlerinin birçoğunu kodlamazlar, aksine çoğaltma için ihtiyaç duydukları viral proteinleri üretmek için konakçı hücrenin organellerini ve döngülerini kullanırlar.[2]
Viral yapısal proteinler
Çoğu viral yapısal protein, virüsün kapsid ve zarf bileşenlerdir.
Kapsid
Bir virüsün genetik materyali, kapsid adı verilen viral bir protein yapısında depolanır. Kapsid, viral nükleik asitlerin, konakçı enzimleriyle, kimyasal maddelerle veya diğer zararlıların etkinliğiyle bozunmasını önleyen bir "kalkandır". Ayrıca virionun konakçıya tutunmasını ve konakçı hücre zarına nüfuz etmesini sağlar. Tek bir viral proteinin veya bir dizi farklı viral proteinin birçok kopyası kapsidi oluşturur ve bu viral proteinlerin her biri, viral genomdan bir gen tarafından kodlanır. Kapsidin yapısı, virüsün geniş bir kapside sahip olması için az sayıda viral gen kullanmasına izin verir.[3]
Birkaç öncül yapı (protomer), oligomerik (viral) protein alt birimleri, kapsomerleri oluşturmak üzere birleşir ve kapsomerler ise kapsidi oluşturmak için bir araya gelir.[1] Kapsomerler bir ikosahedral, sarmal veya karmaşık kapsid yapısına katılabilirler.[2] Üç asimetrik ve özdeş olmayan viral protein birimi, ikosahedral kapsiddeki yirmi özdeş üçgen yüzün her birini oluşturur.
Viral zarf
Bazı virüslerin kapsidi, viral zarf adı verilen bir zar içinde bulunur. Bir virüs konakçı hücresini tomurcuklanma adı verilen bir işlemle terk ettiğinde; viral zarf, konakçı hücrenin plazma zarından elde edilir.[4] Viral zarf, viral glikoproteinler de dahil olmak üzere viral proteinlerle gömülü bir çift katlı lipid katmanından oluşur.[1] Bu viral glikoproteinler, konakçı hücrelerin zarındaki spesifik reseptörlere ve koreseptörlere bağlanır ve virüslerin hedef konakçı hücrelerine tutunmasını sağlar. Bu glikoproteinlerden bazıları şunlardır:
- İnfluenza virüsünde hemagglutinin, nöraminidaz ve M2 proteini.
- İnsan immün yetmezlik virüsünde (HIV) gp120 ve gp41 alt birimlerinden oluşan gp160.[1]
Viral glikoproteinler virüs-hücre birleşiminde (füzyon) kritik bir rol oynar. Virüs-hücre birleşimi, viral glikoproteinler konak hücrenin reseptörlerine bağlandığında başlatılır.[5]
Viral zarf füzyon proteinleri
Viral zarın, konak hücresinin zarı ile kaynaşması için, yüksek enerji gereklidir. Viral zarf füzyon proteinleri, bu yüksek enerji bariyerini aşmak için katalizör görevi görür.[6] Hücresel reseptörlere viral glikoproteinlerin bağlanmasını takiben, viral membran füzyon proteinleri yapılarında bir değişikliğe uğrarlar. Bu yapısal değişiklik daha sonra viral zarf üzerindeki füzyon halkalarının (FH'ler) veya hidrofobik füzyon peptitlerinin (FP'ler) hücre zarıyla etkileşmesine izin vererek viral zarfın hücre zarıyla etkileşimini ve birleşimini (füzyonunu) kolaylaştırır. Çoğu viral membran füzyon proteini, füzyondan sonra saç tokası benzeri bir yapıya dönüşür.
Viral glikoproteinler ve bunların üç boyutlu yapıları, füzyondan önce ve sonra, çok çeşitli yapısal konformasyonların keşfedilmesine izin vermiştir.[6] Viral membran füzyon proteinleri dört farklı sınıfa ayrılmıştır ve her sınıf karakteristik yapılarıyla tanımlanır:
- Sınıf I: Füzyon sonrası konformasyon, α-sarmal saç tokalarının trimerlerinden oluşan ayrı bir merkezi sarmal bobin yapısına sahiptir. Sınıf I viral füzyon proteininin bir örneği HIV glikoproteinidir, gp41.[6]
- Sınıf II: Protein, merkezi sarmal bobin yapısından yoksundur. Bir saç tokası trimeri vermek için yeniden katlanan karakteristik bir uzun yapraklı dış bölge yapısı içerir. Sınıf II viral füzyon proteinlerinin örnekleri arasında dang virüsü E proteini ve batı Nil virüsü E proteini bulunur.[5]
- Sınıf III: Yapısal konformasyon, Sınıf I ve Sınıf II viral membran füzyon proteinlerinin özelliklerinin bir kombinasyonudur. Sınıf III viral füzyon proteininin bir örneği kuduz virüsü glikoproteinidir, G.
- Sınıf IV: Sınıf IV viral füzyon proteinleri, füzyonla ilişkili küçük transmembran (FAST) proteinlerdir. Saç tokası veya trimer yapılarından oluşmazlar ve bilinen en küçük viral füzyon proteinleridir. FAST proteinleri, zarfsız reovirüs ailesinin üyeleri tarafından kodlanır.
Viral yapısal olmayan proteinler
Viral yapısal olmayan proteinler, virüsün genomu tarafından kodlanan proteinlerdir ve enfekte olmuş hücrelerde eksprese edilir.[1] Bununla birlikte, bu proteinler virion içinde toplanmaz. Virüslerin replikasyonu sırasında, bazı viral yapısal olmayan proteinler replikasyon süreci etkileyen önemli işlevler yerine getirir. Benzer şekilde, virüslerin montajı (yapısal elemanlarının birleşimi) sırasında, bu proteinlerin bazıları ayrıca montaj işlemini etkileyen önemli işlevleri yerine getirir. Bu viral yapısal olmayan protein fonksiyonlarından bazıları, replikon oluşumu, immünomodülasyon ve viral yapısal proteini kodlayan genlerin transaktivasyonudur.
Replikon oluşumu
Viral yapısal olmayan proteinler, replikasyon kompleksi olarak da bilinen replikonu oluşturmak için konak hücre proteinleri ile etkileşir.[1] Hepatit C virüsünde, viral yapısal olmayan proteinler replikonu birleştirmek için hücresel vezikül membran nakil proteini hVAP-33 ile etkileşime girer. Viral yapısal olmayan 4b (NS4B) proteini, konakçı hücrenin zarını değiştirir ve replikasyon kompleksinin oluşum sürecini başlatır.[7] NS5A, NS5B ve NS3 gibi diğer viral yapısal olmayan proteinler de komplekse alınır ve NS4B onlarla etkileşerek viral RNA'ya bağlanır.
İmmünomodülasyon
Bir konağın enfekte olmuş bir hücreye bağışıklık yanıtı, viral yapısal olmayan proteinlerin immünomodülatör özellikleri yoluyla ayarlanabilir.[1] Birçok büyük DNA virüsü türü, konakçı bağışıklık tepkisini bozan ve virüsün çoğalmasına izin veren proteinleri kodlar.[8] Bu proteinlerin, insanlarda enflamatuar (yangısal) hastalıklar için yeni biyo-farmasötik tedaviler geliştirme potansiyeli vardır, çünkü proteinlerin enflamatuar bağışıklık aracılarını bozduğu kanıtlanmıştır.[9] Batı Nil virüsündeki viral yapısal olmayan protein NS1, bir kompleman kontrol proteinine, H faktörüne bağlanarak kompleman aktivasyonunu önler. Sonuç olarak, enfekte olmuş hücrelerin kompleman tarafından tanınması zorlaşır ve enfekte olmuş hücreler, konakçının bağışıklık sistemi tarafından zarar görmez.[10]
Viral düzenleyici ve yardımcı proteinler
Viral düzenleyici ve yardımcı proteinlerin birçok işlevi vardır. Bu viral proteinler, viral yapısal gen transkripsiyon oranları da dahil olmak üzere viral genomdaki viral gen ekspresyonlarını kontrol eder ve etkiler.[1] Viral düzenleyici ve yardımcı proteinler ayrıca konakçı hücrenin genlerin düzenlenmesi ve apoptoz gibi hücresel fonksiyonlarını etkiler ve ayarlar.
DNA virüsleri ve retrovirüslerde viral düzenleyici proteinler, viral gen transkripsiyonunu artırabilir, benzer şekilde, bu proteinler ayrıca konakçı hücresel gen transkripsiyonunu da artırabilir.[11]
Yardımcı proteinler olarak da bilinen viral aksesuar proteinler, retrovirüslerin genomu tarafından kodlanır.[12] Çoğu viral aksesuar protein, işlevlerini sadece belirli hücre tiplerinde yerine getirir. Ayrıca, virüsün replikasyonu üzerinde çok fazla etkisi yoktur. Bununla birlikte, bazı durumlarda virüslerin replikasyonunun sürdürülmesi, viral aksesuar proteinlerinin yardımını (ve fonksiyonunu) gerektirir.
Endojen retroviral proteinler
Syncytin, memeli genomunda bulunan ve plasental morfogenezde membran füzyonuna izin vermek için kullanılan bir proteindir. Aynı zamanda memeli genomundan elde edilenendojen bir retrovirüs proteinidir.[13]
Kaynakça
- ^ a b c d e f g h Vladimir Uversky; Sonia Longhi (20 Ekim 2011). Flexible Viruses (İngilizce). John Wiley & Sons. ISBN 9781118135549.
- ^ a b Slonczewski, Joan (2014). Microbiology : an evolving science. New York: W.W. Norton & Company. ISBN 978-0-393-12367-8. OCLC 881060733.
- ^ Lodish (1 Ocak 2000). "Viruses: Structure, Function, and Uses" (İngilizce). 9 Nisan 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Şubat 2020.
- ^ Pornillos (1 Aralık 2002). "Mechanisms of enveloped RNA virus budding". Trends in Cell Biology. 12 (12). ss. 569-579.
- ^ a b White (1 Ocak 2008). "Structures and Mechanisms of Viral Membrane Fusion Proteins". Critical Reviews in Biochemistry and Molecular Biology. 43 (3). ss. 189-219.
- ^ a b c Podbilewicz (2014). "Virus and Cell Fusion Mechanisms". Annual Review of Cell and Developmental Biology. 30 (1). ss. 111-139.
- ^ Gouttenoire (1 Mart 2010). "Hepatitis C virus nonstructural protein 4B: a journey into unexplored territory". Reviews in Medical Virology. 20 (2). ss. 117-129.
- ^ Engel (2012). "Viral immunomodulatory proteins: usurping host genes as a survival strategy". Advances in Experimental Medicine and Biology. Cilt 738. ss. 256-278.
- ^ Lucas (2004). "Secreted immunomodulatory viral proteins as novel biotherapeutics". J Immunol.
- ^ Chung (12 Aralık 2006). "West Nile virus nonstructural protein NS1 inhibits complement activation by binding the regulatory protein factor H". Proceedings of the National Academy of Sciences of the United States of America. 103 (50). ss. 19111-19116.
- ^ Flint (1997). "Viral Transactivating Proteins". Annual Review of Genetics. 31 (1). ss. 177-212.
- ^ Coffin (1 Ocak 1997). "Accessory Proteins and Assembly" (İngilizce). Cold Spring Harbor Laboratory Press. 3 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Şubat 2020.
- ^ Mi S, Lee X, Li X, Veldman GM, Finnerty H, Racie L, LaVallie E, Tang XY, Edouard P, Howes S, Keith JC Jr, McCoy JM (2000). "Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis". Nature. 403 (6771). ss. 785-9.
Dış bağlantılar
- UniProt'da bilinen tüm Viral Proteinlerin listesi 31 Mayıs 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- VirusMint