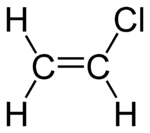
Vinil klorür
 | |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Sistematik IUPAC adı kloroeten | |||
Diğer adlar kloroetilen | |||
| Tanımlayıcılar | |||
CAS numarası | |||
| Kısaltmalar | VCM | ||
| 1731576 | |||
| ECHA InfoCard | 100.000.756 | ||
| EC Numarası |
| ||
| UN numarası | 1086 | ||
CompTox Bilgi Panosu (EPA) | |||
| Özellikler | |||
| Kimyasal formül | C2H3Cl | ||
| Molekül kütlesi | 62,50 g mol−1 | ||
| Görünüm | renksiz gaz | ||
| Yoğunluk | 0,911 g/cc | ||
| Erime noktası | −153.8 °C | ||
| Kaynama noktası | −13.4 °C | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | yanıcı gaz | ||
| NFPA 704 (yangın karosu) | |||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Vinil klorür, CH2=CHCl formülüyle ifade edilen organik bir bileşiktir. Madde, Alman kimyacı Justus von Liebig tarafından keşfedilmiştir. Vinil klorür, oda sıcaklığında gaz hâlindedir ve yoğunlaşabilir keskin kokusuyla fark edilebilmektedir. Kanserojendir.
Toprak organizmalarının klorlu solventleri parçalaması sonucu çevrede oluşabilir. Endüstriler tarafından salınan veya diğer klorlu kimyasalların parçalanmasıyla oluşan vinil klorür havaya ve içme suyu kaynaklarına karışabilir. Vinil klorür, atık depolama alanlarının yakınında bulunan yaygın bir kirletici maddedir.[1]
Nitrosomonas europaea bakteri türü, trikloroetilen ve vinil klorür dâhil olmak üzere çeşitli halojenli bileşikleri parçalayabilmektedir.[2]
Kullanımları
Vinil klorür monomeri (VCM) olarak da adlandırılan vinil klorür, yalnızca PVC'nin öncüsü olarak kullanılır. Toksik oluşu nedeniyle diğer ürünlerde vinil klorür bulunmaz. Poli(vinil klorür) (PVC) çok kararlıdır, depolanabilir ve toksik değildir.
1974 yılına kadar, vinil klorür aerosol sprey itici gazı olarak kullanılıyordu.[3] Vinil klorür, etil klorüre benzer şekilde inhalasyon anestezik olarak kısa bir süreliğine kullanıldı, ancak toksisitesi yüzünden bu uygulamanın bırakıldı.[4][5]
Elde edilişi
Vinil klorür ilk olarak 1835 yılında Justus von Liebig ve öğrencisi Henri Victor Regnault tarafından sentezlendi. 1,2-Dikloroetanı etanol içinde bir potasyum hidroksit çözeltisi ile işleyerek elde ettiler.[6]
1912'de Griesheim-Elektron için çalışan Alman kimyager Fritz Klatte, katalizör olarak cıva klorür kullanarak asetilen ve hidrojen klorürden vinil klorür üretmenin bir yolunun patentini aldı. Bu yöntem Batı'da 1930'lu ve 1940'lı yıllarda yaygın olarak kullanıldı. O zamandan beri Amerika Birleşik Devletleri ve Avrupa'da yerini etilene dayalı daha ekonomik süreçler aldı. Cıva bazlı teknoloji Çin'deki ana üretim yöntemidir.
Vinil klorür monomeri, dünya üretimindeki en büyük yirmi petrokimyasal (petrol türevi kimyasallar) arasında yer almaktadır. Vinil klorürün büyük çoğunluğu poli(vinil klorür), PVC yapmak için kullanılır. Bir ölçek vermek gerekirse, küresel olarak yılda yaklaşık 40 milyon ton PVC reçinesi üretiliyor.[7] Amerika Birleşik Devletleri, klor ve etilen hammaddelerindeki düşük üretim maliyeti konumu nedeniyle en büyük vinil klorür üretim bölgesi olmaya devam ediyor. Çin aynı zamanda büyük bir vinil klorür üreticisi ve en büyük tüketicilerinden biridir.[8]
Etan, özellikle ABD Körfez Kıyısında kolaylıkla bulunabilmektedir. Etilen, etanın parçalanmasıyla elde edilir ve daha sonra etilen, vinil klorür üretimi için kullanılır. Bu nedenle, etilen üretimi için işlem maliyetinden tasarruf etmek amacıyla, etanın doğrudan vinil klorüre dönüştürülmesi için çok sayıda girişimde bulunulmuştur. Etanın vinil klorür tesislerine doğrudan beslenmesi böylece hammadde maliyetlerini önemli ölçüde azaltabilir ve tesislerin kraker kapasitesine daha az bağımlı olmasını sağlayabilir.
Depolama ve taşıma
Vinil klorür sıvı olarak depolanır. Sağlık tehlikesi olarak kabul edilen üst güvenlik sınırı 500 ppm'dir. Çoğunlukla vinil klorür ürününün saklama kapları yüksek kapasiteli tüplerdir. Tüplerin bir iç tüpü bir de dış tüpü vardır. Birkaç inçlik boşluk, iç tüpü dış tüpten ayırır. Tüpler arasındaki boşluk Azot gibi inert bir gazla temizlenir. Azot gazı ara boşluktan çıkarken, iç tüpten herhangi bir vinil klorür sızıntısı olup olmadığını tespit eden bir analizörden geçer. Eğer vinil klorür iç tüpten sızmaya başlarsa veya tüpün dışında bir yangın tespit edilirse, tüpün içindekiler otomatik olarak acil durum yer altı depolama konteynerine boşaltılır. Vinil klorürün atmosferik sıcaklıkta taşınması için kullanılan kaplar her zaman basınç altındadır. Stabilize edilmiş vinil klorür, normal atmosferik koşullarda uygun basınçlı kaplarda saklanabilir. Stabilize edilmemiş vinil klorür, soğutma altında veya normal atmosferik sıcaklıkta, hava veya güneş ışığı olmadan, ancak yalnızca birkaç gün süreyle saklanabilir. Daha uzun süre saklanacaksa herhangi bir polimerizasyonun gerçekleşmediğini doğrulamak için düzenli kontroller yapılmalıdır.[9]
Vinil klorürün taşınması, toksisite riskine ek olarak propan, bütan veya doğal gaz gibi diğer yanıcı gazların taşınmasıyla aynı riskleri de taşır.[10] Bu tehlikenin gözlemlendiği olaylara örnek olarak, vinil klorür de dâhil olmak üzere 100.000 galon tehlikeli maddeyi boşaltan tankerlerin raydan çıktığı 2023 Ohio tren kazası dâhildir.
Sağlık üzerindeki etkileri
Çoğu ortam koşulunda bir gaz olduğu için, birincil maruz kalma, meslekî tehlikelerin en yüksek olduğu kontamine yiyecek veya su tüketiminin aksine, soluma yoluyladır. 1974'ten önce işçiler genellikle 1000 ppm vinil klorüre maruz kalıyordu ve bu da akroosteoliz ve Raynaud Fenomeni gibi "vinil klorür hastalığına" neden oluyordu. Vinil klorür maruziyetinin semptomları, ortam havasındaki ppm seviyelerine göre sınıflandırılır ve 4.000 ppm eşik etkiye sahiptir.[11] Semptomların yoğunluğu, baş dönmesi, mide bulantısı, görme bozuklukları, baş ağrısı ve ataksi dahil olmak üzere akut (1.000-8.000 ppm) ila narkotik etki, kardiyak aritmiler ve ölümcül solunum yetmezliği dahil olmak üzere kronik (12.000 ppm'in üzerinde) arasında değişir.[12]
Kanser
1972'de, Avrupa vinil klorür endüstrisini araştıran İtalyan Maltoni, işçilerde günde dört saat boyunca 250 ppm kadar düşük vinil klorür maruziyetinden kaynaklanan karaciğer tümörleri (anjiyosarkom dâhil) buldu.[13]
1997'de ABD Hastalık Kontrol ve Önleme Merkezleri (CDC), 1970'lerin sonlarında kapalı döngü polimerizasyon işleminin PVC endüstrisi tarafından geliştirilmesi ve kabul edilmesinin "işçilerin maruziyetini neredeyse tamamen ortadan kaldırdığı" ve "vinil klorür polimerizasyonunde çalışanlarda, yeni hepatik anjiyosarkom vakalarının neredeyse tamamen azaldığının" ortaya çıktığı sonucuna vardı."[14]
Houston Chronicle, 1998'de vinil endüstrisinin, işçilerin maruz kalmasından kaynaklanan sorumluluktan kaçınmak için vinil klorür çalışmalarını manipüle ettiğini ve yerel topluluklardaki kapsamlı ve şiddetli kimyasal sızıntıları gizlediğini iddia etti.[15]
Mekanizma
Vinil klorürün kanserojenliği iki metabolitin, kloroetilen oksit ve kloroasetaldehitin etkisine atfedilir. İlki sitokrom P-450'nin vinil klorür üzerindeki etkisiyle üretilir. Hem kloroetilen oksit hem de kloroasetaldehit alkilleyici maddelerdir.
Çevre kirliliği
ABD EPA'ya göre, "poli(vinil klorür) (PVC), etilen diklorür (EDC) ve vinil klorür monomer (VCM) tesislerinden kaynaklanan vinil klorür emisyonları, hava kirliliğinde artışla sonuçlanması makul olarak beklenebilecek hava kirliliğine ve ölümlerde veya ciddi hastalıklarda artışa neden olur veya katkıda bulunur. Vinil klorür, nadir görülen bir karaciğer kanserine neden olduğu bilinen bir insan kanserojenidir."[16]
Yangın ve patlama riskleri
ABD'de İş Güvenliği ve Sağlığı İdaresi (OSHA), vinil klorürü, Ulusal Yangından Korunma Birliği (NFPA) Yanıcılık Derecesi 4 olan Sınıf IA Yanıcı Sıvı olarak listelemektedir. Düşük kaynama noktasından dolayı sıvı vinil klorür, atmosferi basınca salındığında ani buharlaşmaya (yani otomatik soğutmaya) maruz kalacaktır. Buharlaşan kısım yoğun bir bulut oluşturacaktır (çevredeki havanın iki katından daha ağır). Daha sonra patlama veya yangın riski önemlidir. OSHA'ya göre vinil klorürün parlama noktası -78 °C'dir.[17]
Yanması, toksik hidrojen klorür (HCl) ve karbon monoksit (CO) ile eser miktarda fosgen açığa çıkarabilir.[18][19]
Vinil klorür, ısıtma nedeniyle ve havanın, ışığın etkisi altında ve bir katalizörle, güçlü oksitleyicilerle, bakır ve alüminyum gibi metallerle temas hâlinde, yangın veya patlama tehlikesiyle birlikte hızla polimerleşebilir. Vinil klorür havayla karışan bir gaz olduğundan yangın ve patlama tehlikesi oluşturur. Durduğunda vinil klorür, peroksitler oluşturabilir ve bu peroksitler daha sonra patlayabilir. Vinil klorür nem varlığında demir ve çelikle reaksiyona girer.[20]
Ayrıca bakınız
- Vinil grubu
- 2023 Ohio tren kazası; vinil klorür taşıyan trenin raydan çıkması sonucu Vinil klorür sızıntısı
Kaynakça
- ^ "Vinyl Chloride". Wisconsin Department of Health Services (İngilizce). 30 Ocak 2018. 7 Şubat 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Şubat 2023.
- ^ "Home – Nitrosomonas europaea". genome.jgi-psf.org. 3 Temmuz 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Nisan 2018.
- ^ Markowitz, Gerald; Rosner, David (2013). Deceit and Denial: The Deadly Politics of Industrial Pollution. Berkeley, California Press: University of California Press. s. 185.[]
- ^ Tamburro CH (1978). "Health effects of vinyl chloride". Texas Reports on Biology and Medicine. 37: 126-44, 146-51. PMID 572591.
- ^ Oster RH, Carr CJ (July 1947). "Anesthesia; narcosis with vinyl chloride". Anesthesiology. 8 (4): 359-61. doi:10.1097/00000542-194707000-00003. PMID 20255056. 15 Şubat 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Şubat 2023.
- ^ Regnault, H. V. (1835). "Sur la Composition de la Liqueur des Hollandais et sur une nouvelle Substance éthérée". Annales de Chimie et de Physique. Gay-Lussac & Arago. 5858: 301-320. 11 Temmuz 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2019.
- ^ "PVC applications". The European Council of Vinyl Manufacturers. 25 Şubat 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Şubat 2023.
- ^ "Vinyl Chloride Monomer (VCM) – Chemical Economics Handbook". S&P Global. 18 Ağustos 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Nisan 2018.
- ^ "aseh.net" (PDF). 20 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 6 Ekim 2013.
- ^ "Vinyl Chloride Monomer (VCM) Production". The European Council of Vinyl Manufacturers. 7 Ocak 2019 tarihinde kaynağından arşivlendi.
- ^ Harrison, Henrietta (2008). Vinyl chloride Toxicological overview 15 Mart 2023 tarihinde Wayback Machine sitesinde arşivlendi., Health Protecction Agency, UK
- ^ International Programme on Chemical Safety (IPCS) (1999). Vinyl chloride. Environmental Health Criteria 215. WHO. Geneva.
- ^ Maltoni, C. "Cancer Detection and Prevention" (1972) Presented at the Second International Symposium on Cancer Detection and Prevention. Bologna, April 9–12, 1973.
- ^ Epidemiologic Notes and Reports Angiosarcoma of the Liver Among Polyvinyl Chloride Workers – Kentucky 16 Eylül 2010 tarihinde Wayback Machine sitesinde arşivlendi.. Centers for Disease Control and Prevention. 1997.
- ^ Jim Morris, "In Strictest Confidence. The chemical industry's secrets," Houston Chronicle. Part One: "Toxic Secrecy," June 28, 1998, pp. 1A, 24A–27A; Part Two: "High-Level Crime," June 29, 1998, pp. 1A, 8A, 9A; and Part Three: "Bane on the Bayou," July 26, 1998, pgs. 1A, 16A.
- ^ National Emission Standards for Hazardous Air Pollutants (NESHAP) for Vinyl Chloride Subpart F, OMB Control Number 2060-0071, EPA ICR Number 0186.09 (Federal Register: September 25, 2001 (Volume 66, Number 186) 22 Mart 2003 tarihinde Wayback Machine sitesinde arşivlendi.)
- ^ "Aseh.net" (PDF). 20 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 6 Ekim 2013.
- ^ "Occupational Safety and Health Guideline for Vinyl Chloride"1988."
- ^ O'Mara, M. M.; Grider, L. B.; Daniel, R. L. (March 1971). "Combustion Products from Vinyl Chloride Monomer". American Industrial Hygiene Association Journal. 32 (3): 153-156. doi:10.1080/0002889718506429. PMID 5551110.
- ^ "Vinyl chloride: health effects, incident management and toxicology". www.gov.uk. 10 Şubat 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Nisan 2018.