Vaccinia
| Vaccinia | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Vaccinia virüsü virionlarının TEM mikrografı | |||||||||||||||||
| Virüs sınıflandırması | |||||||||||||||||
| |||||||||||||||||
| Üye virüsler [1] | |||||||||||||||||
| |||||||||||||||||
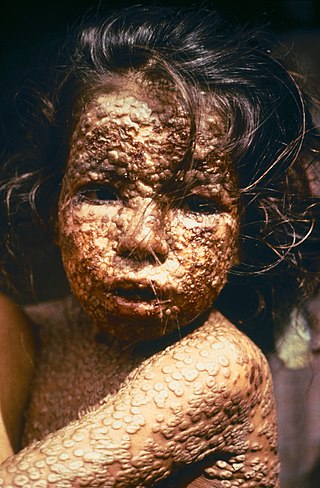
Vaccinia virüsü (VACV veya VV), poxvirüs ailesine ait büyük, kompleks, zarflı bir virüstür.[2] Yaklaşık 250 geni kodlayan, yaklaşık 190 kbp uzunluğunda doğrusal, çift sarmallı bir DNA genomuna sahiptir. Virionun boyutları kabaca 360 × 270 × 250 nm'dir ve kütlesi yaklaşık 5-10 fg'dir.[3] Vaccinia virüsü, Dünya Sağlık Örgütünün (WHO) 1958-1977 yılları arasında küresel bir aşılama kampanyasında çiçek hastalığını ortadan kaldırmak için kullandığı modern çiçek aşısının kaynağıdır. Çiçek hastalığı artık vahşi doğada bulunmamasına rağmen, vaccinia virüsü gen terapisi ve genetik mühendisliği için bir araç olarak bilim insanları tarafından hala geniş çapta incelenmektedir.
Çiçek hastalığı %30 ölüm oranına sahip endemik bir insan hastalığıydı. 1796'da İngiliz doktor Edward Jenner, nispeten hafif olan inek çiçeği virüsünün bulaşmasının ölümcül çiçek hastalığına karşı da bağışıklık kazandıracağını kanıtladı. Jenner çiçek hastalığından variolae vaccinae (inek çiçek hastalığı) olarak bahsetmiştir. Ancak çiçek aşısının kökenleri, özellikle Louis Pasteur'ün 19. yüzyılda aşı oluşturmak için laboratuvar teknikleri geliştirmesinden sonra, zaman içinde bulanıklaştı.[4] Allan Watt Downie 1939'da modern çiçek aşısının serolojik olarak inek çiçeğinden farklı olduğunu göstermiş[5] ve daha sonra vaccinia ayrı bir viral tür olarak kabul edilmiştir. Tüm genom dizilimi, vaccinia'nın en çok at çiçeği ile yakından ilişkili olduğunu ve Büyük Britanya'da bulunan inek çiçeği suşlarının vaccinia ile en az yakından ilişkili olduğunu ortaya koymuştur.[6]
Vaccinia enfeksiyonlarının sınıflandırılması
Komplike olmayan primer aşılamanın morbiditesine, enfeksiyonun kaşıma yoluyla diğer bölgelere taşınmasına ve aşılama sonrası ensefalite ek olarak, aşı enfeksiyonlarının diğer komplikasyonları aşağıdaki tiplere ayrılabilir.[7]:391
- Yaygın vaccinia
- Egzema vaccinatum
- İlerleyici vaccinia (vaccinia gangrenosum, vaccinia necrosum)
- Roseola vaccinia
Köken
Vaccinia virüsü, sığır çiçeğine neden olan virüsle yakından ilişkilidir; tarihsel olarak bu ikisinin genellikle bir ve aynı olduğu düşünülmüştür.[8] Aşı virüsünün kesin kökeni, kayıt tutma eksikliğinden dolayı bilinmemektedir, çünkü virüs onlarca yıl boyunca araştırma laboratuvarlarında tekrar tekrar yetiştirilmiş ve pasajlanmıştır.[9] En yaygın görüş, vaccinia virüsü, inek çiçeği virüsü ve variola virüsünün (çiçek hastalığının etkeni) ortak bir atasal virüsten türediği yönündedir. Ayrıca vaccinia virüsünün ilk olarak atlardan izole edildiği[8] ve erken dönem (1902) çiçek aşısı örneğinden elde edilen DNA'nın analizinin at çiçeği virüsüne %99,7 oranında benzediğini gösterdiği yönünde spekülasyonlar da vardır.[10]
Viroloji
Poxvirüsler DNA virüsleri arasında benzersizdir çünkü sadece konak hücrenin sitoplazmasında, çekirdeğin dışında replike olurlar.[11] Bu nedenle, viral DNA replikasyonu ve gen transkripsiyonunda yer alan çeşitli enzim ve proteinlerin kodlanması için büyük genom gereklidir. VV replikasyon döngüsü sırasında, dış membranları bakımından farklılık gösteren dört enfeksiyöz form üretir: hücre içi olgun virion (IMV), hücre içi zarflı virion (IEV), hücre ile ilişkili zarflı virion (CEV) ve hücre dışı zarflı virion (EEV).[12] Konu tartışmalı olmaya devam etse de hakim görüş IMV'nin tek bir lipoprotein zardan oluştuğu, CEV ve EEV'nin her ikisinin de iki zar tabakası ile çevrili olduğu ve IEV'nin üç zarfa sahip olduğu yönündedir. IMV en bol bulunan enfeksiyöz formdur ve konaklar arasında yayılmadan sorumlu olduğu düşünülmektedir. Öte yandan, CEV'in hücreden hücreye yayılmada rol oynadığı ve EEV'nin konak organizma içinde uzun menzilli yayılma için önemli olduğu düşünülmektedir.[]
Çoklu reaktivasyon
Vaccinia virüsü çoklu reaktivasyon (MR) geçirebilmektedir.[13] MR, aksi takdirde ölümcül hasar içeren iki veya daha fazla virüs genomunun enfekte bir hücre içinde etkileşime girerek canlı bir virüs genomu oluşturması sürecidir. Abel,[13] tek virüs partikülleri konak civciv embriyo hücrelerini enfekte ettiğinde döl oluşumunu önlemek için yeterli UV ışığı dozlarına maruz kalan vaccinia virüslerinin, konak hücreler bu inaktive virüslerden iki veya daha fazlası tarafından enfekte edildiğinde yine de canlı döl virüsleri üretebildiğini, yani MR'nin meydana gelebildiğini bulmuştur. Kim ve Sharp, UV ışığı,[14] nitrojen hardalı[15] ve X-ışınları veya gama ışınları[16] ile muameleden sonra vaccinia virüsünün MR'ını göstermiştir. Michod ve arkadaşları[17] farklı virüslerde çok sayıda MR örneğini gözden geçirmiş ve MR'nin virüslerde genom hasarlarının rekombinasyonel onarımı avantajını sağlayan yaygın bir cinsel etkileşim biçimi olduğunu öne sürmüştür.[]
Konak direnci
Vaccinia, genomunda virüse interferonlara karşı direnç kazandıran çeşitli proteinlerin genlerini içerir:
- K3L (P18378), ökaryotik başlatma faktörü 2 (eIF-2alpha) proteinine homolojisi olan bir proteindir. K3L proteini, bir interferon aktivatörü olan PKR'nin etkisini engeller.[18]
- E3L (P21605) Vaccinia tarafından kodlanan başka bir proteindir. E3L de PKR aktivasyonunu inhibe eder; ve ayrıca çift sarmallı RNA'ya bağlanabilir.[18]
- B18R, Moderna'nın teknolojilerinden birinde interferon inhibitörü olarak görev yapan bir proteindir.[19]
Aşı olarak kullanım

Vaccinia virüs enfeksiyonu tipik olarak çok hafiftir ve genellikle sağlıklı bireylerde belirtilere neden olmaz, ancak kızarıklık ve ateşe neden olabilir. Aşı virüsü enfeksiyonu sonucu oluşan bağışıklık tepkileri kişiyi ölümcül çiçek hastalığı enfeksiyonuna karşı korur. Bu nedenle, vaccinia virüsü çiçek hastalığına karşı canlı virüs aşısı olarak kullanılmıştır ve halen de kullanılmaktadır. Aşılanan virüsün zayıflatılmış formlarını kullanan aşıların aksine, vaccinia virüs aşısı çiçek virüsü içermediği için çiçek enfeksiyonuna neden olamaz. Ancak zaman zaman bazı komplikasyonlar ve/veya aşı yan etkileri ortaya çıkabilir. Bağışıklık sistemi baskılanmış kişilerde bu olasılık önemli ölçüde artmaktadır. Aşılanan her 1 milyon kişiden yaklaşık 1 ila 2'si aşıya karşı yaşamı tehdit eden reaksiyonlar sonucu ölebilir.[20] ACAM2000 ile miyoperikardit oranı primer aşılananların 1.000'inde 5,7'dir.[21]
1 Eylül 2007 tarihinde ABD Gıda ve İlaç Dairesi (FDA) çiçek hastalığına karşı ihtiyaç halinde hızla üretilebilen yeni bir aşı olan ACAM2000'e ruhsat vermiştir. Sanofi Pasteur tarafından üretilen yeni aşıdan ABD Hastalık Kontrol ve Korunma Merkezleri 192.5 milyon doz stoklamıştır (aşağıdaki yaygın suşların listesine bakınız).[22]
Modifiye edilmiş vaccinia Ankara suşuna dayanan Imvanex adlı çiçek aşısı 2013 yılında Avrupa İlaç Ajansı (EMA) tarafından onaylanmıştır.[23] Bu suş, 2022 maymun çiçeği salgını sırasında aşılarda kullanılmıştır.[]
Vaccinia ayrıca rekombinant aşılarda, bir bağışıklık yanıtı oluşturmak için bir konak içinde yabancı genlerin ekspresyonu için bir vektör olarak kullanılır. Diğer poxvirüsler de canlı rekombinant aşı olarak kullanılmaktadır.[24]
Tarihçe
Çiçek hastalığı için orijinal aşı ve aşılama fikrinin kökeni, 1798 yılında Edward Jenner tarafından tanımlanan inek çiçeğidir. İnek çiçeği için kullanılan Latince terim Variolae vaccinae idi ve Jenner'ın kendi çevirisiyle "inek çiçek hastalığı" anlamına geliyordu. Bu terim tüm aşılama fikrine adını vermiştir.[25] Çiçek aşısında kullanılan virüsün inek çiçeği virüsüyle aynı olmadığı ya da artık aynı olmadığı fark edildiğinde, çiçek aşısındaki virüs için 'vaccinia' adı kullanıldı. (Bkz. OED.) Soğutmalı taşıma yöntemlerinin icadından önce aşının etki gücü ve etkinliği güvenilmezdi. Aşı, ısı ve güneş ışığıyla etkisiz hale gelirdi ve örnekleri tüy kalemler üzerinde kurutma ve ihtiyacı olan ülkelere gönderme yöntemi genellikle inaktif bir aşıyla sonuçlanırdı. Kullanılan bir diğer yöntem de "koldan kola" yöntemiydi. Bu, bir bireyin aşılanmasını ve ardından bulaşıcı püstül oluşur oluşmaz bir başkasına, sonra bir başkasına vb. aktarılmasını içeriyordu. Bu yöntem aşının canlı olarak taşınması için kullanılıyordu ve genellikle yetimler taşıyıcı olarak kullanılıyordu. Ancak bu yöntem, 1861 yılında 41 İtalyan çocuğun "koldan kola" yöntemiyle aşılandıktan sonra frengiye yakalanması örneğinde olduğu gibi, hepatit ve frengi gibi diğer kan hastalıklarının yayılma olasılığı nedeniyle sorunluydu.[26] Henry Austin Martin buzağılardan aşı üretimi için bir yöntem geliştirmiştir.[27]
1913'te E. Steinhardt, C. Israeli ve R. A. Lambert domuz kornea doku kültürü parçalarında vaccinia virüsü üretmiştir.[28]

Willian Bulloch'un öğrencisi olan Fredrick W. Twort tarafından 1915 yılında yayınlanan bir makale, modern faj araştırmalarının başlangıcı olarak kabul edilir. Twort, canlı hücrelerin yokluğunda agar besiyerinde vaccinia virüsünü büyütmeye çalışırken, birçok kontamine mikrokok kolonisinin büyüdüğünü ve mukoid, sulu veya camsı göründüğünü ve bu dönüşümün, taze koloninin sulu koloniden alınan materyalle aşılanması yoluyla diğer kolonilerde indüklenebileceğini fark etti. Mikroskop kullanarak, bakterilerin Giemsa boyası ile kırmızıya boyanan küçük granüllere dönüştüğünü gözlemlemiştir. "...bu [dönüşüm ajanı] neredeyse mikrokokların akut bulaşıcı bir hastalığı olarak düşünülebilir" sonucuna varmıştır.[30]
1939 yılında Allan Watt Downie, 20. yüzyılda kullanılan çiçek aşıları ile inek çiçeği virüsünün aynı olmadığını, ancak immünolojik olarak ilişkili olduğunu göstermiştir.[5][31]
2000-günümüz
Mart 2007'de Indiana'da yaşayan 2 yaşındaki bir çocuk ve annesi, çocuğun babasından hayatı tehdit eden bir vaccinia enfeksiyonu kapmıştır.[32] Çocuk, Birleşik Devletler Ordusu tarafından denizaşırı bir göreve gönderilmeden önce çiçek aşısı olan babasıyla yakın temasa girdikten sonra vücudunun yüzde 80'inde belirgin döküntüler geliştirmiştir. Birleşik Devletler ordusu çiçek aşılarına 2002 yılında yeniden başlamıştır. Çocuk, aşı enfeksiyonu için bilinen bir risk faktörü olan egzama nedeniyle enfeksiyonu kapmıştır. Çocuk intravenöz immünoglobulin, cidofovir ve SIGA Technologies tarafından geliştirilen (o zamanlar) deneysel bir ilaç olan Tecovirimat (ST-246) ile tedavi edilmiştir.[33] 19 Nisan 2007'de, ciltte olası yara izi dışında herhangi bir yan etki görülmeden eve gönderilmiştir.[32]
2010 yılında Hastalık Kontrol ve Korunma Merkezleri (CDC) Washington'da bir kadının, yakın zamanda çiçek aşısı olmuş bir ordu mensubu olan erkek arkadaşıyla dijital vajinal temas sonrasında vaccinia virüs enfeksiyonuna yakalandığını bildirmiştir. Kadının çocukluğunda egzama öyküsü vardı ancak yetişkinliğinde semptomatik olmamıştı. CDC, önceki 12 ay içinde yakın zamanda askeri aşı olmuş bir kişiyle cinsel temas sonrası aşı enfeksiyonu görülen dört benzer vakadan haberdar olduğunu belirtmiştir.[34] Yine egzama öyküsü olan hastalarda 2012 yılında başka vakalar da ortaya çıkmıştır.[35]
Yaygın suşlar
Bu, araştırma ve aşılama için kullanılan iyi karakterize edilmiş bazı vaccinia suşlarının bir listesidir.[]
- Lister (Elstree olarak da bilinir): Leslie Collier tarafından toz halinde ısıya dayanıklı aşı geliştirmek için kullanılan İngiliz aşı suşu. Dünya Sağlık Örgütü Çiçek Eradikasyon Kampanyası (SEC) sırasında aşı üretimi için temel olarak kullanılmıştır
- Dryvax ("Wyeth" olarak da bilinir): Wyeth tarafından üretilen ve daha önce Amerika Birleşik Devletleri'nde kullanılan aşı türü. SEC'de kullanılan bu aşı 2008 yılında Acambis tarafından üretilen ACAM2000 (aşağıya bakınız) ile değiştirilmiştir.[36] Dondurularak kurutulmuş ve antibiyotiklerle muamele edilmiş buzağı lenf preparatları olarak üretilmiştir.
- EM63; SEC'de kullanılan Rus suşu
- ACAM2000: Acambis tarafından üretilen ve ABD'de kullanılmakta olan mevcut suş. ACAM2000, plak saflaştırma yoluyla Dryvax virüsünün bir klonundan türetilmiştir. Vero hücrelerinin kültürlerinde üretilir.
- Modifiye vaccinia Ankara (MVA olarak da bilinir): vaccinia virüsünün tavuk embriyo fibroblastlarında birkaç yüz kez pasajlanmasıyla oluşturulan oldukça zayıflatılmış (virülan olmayan) bir türdür. Diğer bazı vaccinia suşlarının aksine bağışıklık sistemi yetersiz fareleri hasta etmez ve bu nedenle çok genç, çok yaşlı, HIV/AIDS'li vb. olması nedeniyle bağışıklık sistemi zayıf olan insanlarda kullanılması daha güvenli olabilir.
- LC16m8: Japonya'da geliştirilen ve şu anda kullanılan zayıflatılmış bir suş
- CV-1: Amerika Birleşik Devletleri'nde geliştirilen ve 1960'ların sonu ile 1970'lerde kullanılan zayıflatılmış bir tür
- Batı Rezervi
- Kopenhag
- Connaught Laboratories (Kanada)
Kaynakça
- ^ "ICTV 9th Report (2011) Poxviridae". International Committee on Taxonomy of Viruses (ICTV) (İngilizce). 8 Ağustos 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Aralık 2018.
- ^ Ryan KJ, Ray CG, (Ed.) (2004). Sherris Medical Microbiology. 4th. McGraw Hill. ISBN 978-0-8385-8529-0.
- ^ Johnson, L.; Gupta, A. K.; Ghafoor, A.; Akin, D.; Bashir, R. (2006). "Characterization of vaccinia virus particles using microscale silicon cantilever resonators and atomic force microscopy". Sensors and Actuators B Chemical. 115 (1). ss. 189-197. doi:10.1016/j.snb.2005.08.047.
- ^ Baxby, Derrick (1981). Jenner's Smallpox Vaccine: The Riddle of Vaccinia Virus and Its Origin (İngilizce). Heinemann Educational Books. ISBN 978-0-435-54057-9.
- ^ a b Downie, AW (1939). "The Immunological Relationship of the Virus of Spontaneous Cowpox to Vaccinia Virus". British Journal of Experimental Pathology. 20 (2). ss. 158-176. PMC 2065307 $2.
- ^ Carroll, Darin S.; Emerson, Ginny L.; Li, Yu; Sammons, Scott; Olson, Victoria; Frace, Michael; Nakazawa, Yoshinori; Czerny, Claus Peter; Tryland, Morten; Kolodziejek, Jolanta; Nowotny, Norbert; Olsen-Rasmussen, Melissa; Khristova, Marina; Govil, Dhwani; Karem, Kevin; Damon, Inger K.; Meyer, Hermann (8 Ağustos 2011). "Chasing Jenner's Vaccine: Revisiting Cowpox Virus Classification". PLOS ONE (İngilizce). 6 (8). ss. e23086. Bibcode:2011PLoSO...623086C. doi:10.1371/journal.pone.0023086. ISSN 1932-6203. PMC 3152555 $2. PMID 21858000.
- ^ James, William D.; Berger, Timothy G.; ve diğerleri. (2006). Andrews' Diseases of the Skin: clinical Dermatology. Saunders Elsevier. ISBN 978-0-7216-2921-6.
- ^ a b Huygelen C (1996). "Jenner's cowpox vaccine in light of current vaccinology". Verh. K. Acad. Geneeskd. Belg. (Felemenkçe). 58 (5). ss. 479-536; discussion 537-538. PMID 9027132.
- ^ Henderson DA, Moss B (1999) [1988]. "Smallpox and Vaccinia". Plotkin SA, Orenstein WA (Ed.). Vaccines. 3rd. Philadelphia, Pennsylvania: WB Saunders. ISBN 978-0-7216-7443-8. 1 Haziran 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
- ^ Schrick, Livia; Tausch, Simon H; Dabrowski, P. Wojciech; Damaso, Clarissa R; Esparza, José; Nitsche, Andreas (2017). "An Early American Smallpox Vaccine Based on Horsepox". New England Journal of Medicine. 377 (15). ss. 1491-1492. doi:10.1056/NEJMc1707600. PMID 29020595.
- ^ Tolonen N, Doglio L, Schleich S, Krijnse Locker J (1 Temmuz 2001). "Vaccinia Virus DNA Replication Occurs in Endoplasmic Reticulum-enclosed Cytoplasmic Mini-Nuclei". Mol. Biol. Cell. 12 (7). ss. 2031-46. doi:10.1091/mbc.12.7.2031. PMC 55651 $2. PMID 11452001.
- ^ Smith GL, Vanderplasschen A, Law M (1 Aralık 2002). "The formation and function of extracellular enveloped Vaccinia virus". J. Gen. Virol. 83 (Pt 12). ss. 2915-31. doi:10.1099/0022-1317-83-12-2915. PMID 12466468.
- ^ a b ABEL P (August 1962). "Multiplicity reactivation and marker rescue with vaccinia virus". Virology. 17 (4). ss. 511-9. doi:10.1016/0042-6822(62)90150-2. PMID 13858909.
- ^ Sharp DG, Kim KS (July 1966). "Multiplicity reactivation and radiation survival of aggregated vaccinia virus. Calculation of plaque titer based on MR and particle aggregation seen in the electron microscope". Virology. 29 (3). ss. 359-66. doi:10.1016/0042-6822(66)90211-X. PMID 5922451.
- ^ Kim KS, Sharp DG (February 1967). "Multiplicity reactivation of vaccinia virus particles treated with nitrogen mustard". J. Virol. 1 (1). ss. 45-9. doi:10.1128/JVI.1.1.45-49.1967. PMC 375503 $2. PMID 5623957.
- ^ Kim KS, Sharp DG (January 1968). "Multiplicity reactivation of gamma- and x-irradiated Vaccinia virus in L cells". Radiat. Res. 33 (1). ss. 30-6. Bibcode:1968RadR...33...30K. doi:10.2307/3572239. JSTOR 3572239. PMID 5634978.
- ^ Michod RE, Bernstein H, Nedelcu AM (2008). "Adaptive value of sex in microbial pathogens". Infect Genet Evol. 8 (3). ss. 267-285. doi:10.1016/j.meegid.2008.01.002. PMID 18295550.
- ^ a b Davies MV, Chang HW, Jacobs BL, Kaufman RJ (1 Mart 1993). "The E3L and K3L vaccinia virus gene products stimulate translation through inhibition of the double-stranded RNA-dependent protein kinase by different mechanisms". J. Virol. 67 (3). ss. 1688-1692. doi:10.1128/JVI.67.3.1688-1692.1993. PMC 237544 $2. PMID 8094759.
- ^ Warren, Luigi; Manos, Philip D.; Ahfeldt, Tim; Loh, Yuin-Han; Li, Hu; Lau, Frank; Ebina, Wataru; Mandal, Pankaj K.; Smith, Zachary D.; Meissner, Alexander; Daley, George Q.; Brack, Andrew S.; Collins, James J.; Cowan, Chad; Schlaeger, Thorsten M.; Rossi, Derrick J. (2010). "Highly Efficient Reprogramming to Pluripotency and Directed Differentiation of Human Cells with Synthetic Modified mRNA". Cell Stem Cell. 7 (5). ss. 618-630. doi:10.1016/j.stem.2010.08.012. PMC 3656821 $2. PMID 20888316.
- ^ "Side Effects of Smallpox Vaccination | Smallpox | CDC". 12 Temmuz 2017. 26 Mayıs 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Mayıs 2022.
- ^ Rao, Agam K.; Petersen, B. W.; Whitehill, F.; Razeq, J. H.; Isaacs, S. N.; Merchlinsky, M. J.; Campos-Outcalt, D.; Morgan, R. L.; Damon, I.; Sánchez, P. J.; Bell, B. P. (3 Haziran 2022). "Use of JYNNEOS (Smallpox and Monkeypox Vaccine, Live, Nonreplicating) for Preexposure Vaccination | Smallpox | CDC". MMWR. Morbidity and Mortality Weekly Report. 71 (22). ss. 734-742. doi:10.15585/mmwr.mm7122e1. PMC 9169520 $2. PMID 35653347. 8 Ağustos 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Ağustos 2022.
- ^ Heilprin, John (1 Eylül 2007). "FDA approves new smallpox vaccine". Houston Chronicle. AP. 26 Mayıs 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Mayıs 2018.
- ^ "European public assessment report summary: Imvanex". 17 Eylül 2018. 20 Haziran 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 Mayıs 2014.
- ^ Vanderplasschen, A.; Pastoret, P.-P. (December 2003). "The Uses of Poxviruses as Vectors". Current Gene Therapy. 3 (6). ss. 583-595. doi:10.2174/1566523034578168. PMID 14683453.
- ^ Baxby, D (1999). "Edward Jenner's Inquiry; a bicentenary analysis". Vaccine. 17 (4). ss. 301-307. doi:10.1016/S0264-410X(98)00207-2. PMID 9987167.
- ^ Tucker, Jonathan B. (2001). Scourge: The Once and Future Threat of Smallpox. New York: Grove/Atlantic Inc.
- ^ Esparza, José; Lederman, Seth; Nitsche, Andreas; Damaso, Clarissa R. (19 Haziran 2020). "Early smallpox vaccine manufacturing in the United States: Introduction of the "animal vaccine" in 1870, establishment of "vaccine farms", and the beginnings of the vaccine industry". Vaccine. 38 (30). ss. 4773-4779. doi:10.1016/j.vaccine.2020.05.037. ISSN 0264-410X. PMC 7294234 $2. PMID 32473878.
- ^ Steinhardt E, Israeli C, Lambert RA (September 1913). "Studies on the cultivation of the virus of vaccinia". J Inf Dis. 13 (2). ss. 294-300. doi:10.1093/infdis/13.2.294. JSTOR 30073371. 31 Mart 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Eylül 2019.
- ^ "Tube for smallpox vaccine with two sealed needles". Thackray Museum of Medicine Collections Online. 474.058. 29 Mayıs 2024 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Mayıs 2024.
- ^ Waldor, Matthew K.; Friedman, David I.; Adhya, Sankar Lal, (Ed.) (2005). Phages : their role in bacterial pathogenesis and biotechnology. Washington, D.C.: ASM Press. ISBN 1-55581-307-0. OCLC 57557385.
- ^ Tyrrell, D. A. J.; McCarthy, K. (1990). "Allan Watt Downie. September 1901 – 26 January 1988". Biographical Memoirs of Fellows of the Royal Society. Cilt 35. ss. 98-112. doi:10.1098/rsbm.1990.0004. PMID 11622284.
- ^ a b Centers for Disease Control and Prevention (CDC) (2007). "Household transmission of vaccinia virus from contact with a military smallpox vaccinee—Illinois and Indiana, 2007". Morbidity and Mortality Weekly Report. 56 (19). ss. 478-81. PMID 17510612. 10 Mart 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
- ^ "SIGA's Smallpox Drug Candidate Administered to Critically Ill Human Patient" (Basın açıklaması). SIGA Technologies. 17 Mart 2007. 20 Temmuz 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Temmuz 2018.
- ^ Centers for Disease Control and Prevention (CDC) (2010). "Vaccinia Virus Infection After Sexual Contact with a Military Smallpox Vaccinee—Washington, 2010". Morbidity and Mortality Weekly Report. 59 (25). ss. 773-75. PMID 20592687. 23 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
- ^ Centers for Disease Control and Prevention (CDC) (March 2013). "Secondary and tertiary transmission of vaccinia virus after sexual contact with a smallpox vaccinee—San Diego, California, 2012". Morbidity and Mortality Weekly Report. 62 (8). ss. 145-7. PMC 4604863 $2. PMID 23446513. 9 Mart 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
- ^ "Notice to Readers: Newly Licensed Smallpox Vaccine to Replace Old Smallpox Vaccine". MMWR Morb. Mortal. Wkly. Rep. 57 (8). 29 Şubat 2008. ss. 207-8. 20 Mayıs 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
Konuyla ilgili yayınlar
- Gubser C, Hué S, Kellam P, Smith GL (January 2004). "Poxvirus genomes: a phylogenetic analysis". J Gen Virol. 85 (1). ss. 105-17. doi:10.1099/vir.0.19565-0. PMID 14718625.
- Centers for Disease Control and Prevention (CDC) (2007). "Vulvar vaccinia infection after sexual contact with a military smallpox vaccinee—Alaska, 2006". MMWR Morb. Mortal. Wkly. Rep. 56 (17). ss. 417-9. PMID 17476203. 28 Haziran 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Eylül 2017.
- Al Ali, S; Baldanta, S; Fernández-Escobar, M; Guerra, S (2016). "Use of Reporter Genes in the Generation of Vaccinia Virus-Derived Vectors". Viruses. 8 (5). s. 134. doi:10.3390/v8050134. PMC 4885089 $2. PMID 27213433.
- Rubins, K. H.; Hensley, L. E.; Bell, G. W.; Wang, C; Lefkowitz, E. J.; Brown, P. O.; Relman, D. A. (2008). "Comparative analysis of viral gene expression programs during poxvirus infection: A transcriptional map of the vaccinia and monkeypox genomes". PLOS ONE. 3 (7). ss. e2628. Bibcode:2008PLoSO...3.2628R. doi:10.1371/journal.pone.0002628. PMC 2440811 $2. PMID 18612436.
- "Vaccinia virus, complete genome". National Center for Biotechnology Information. Erişim tarihi: 25 Temmuz 2007.
- Condit RC, Moussatche N, Traktman P. "The Vaccinia Virion: 3D Tour". Erişim tarihi: 26 Temmuz 2007.
- "Smallpox". Emergency Preparedness & Response. Centers for Disease Control and Prevention. 13 Ağustos 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Temmuz 2007.
- Gorvett, Zaria. "The mystery virus that protects against monkeypox". Erişim tarihi: 26 Temmuz 2022.
Dış bağlantılar
| Sınıflandırma | |
|---|---|
| Dış kaynaklar |