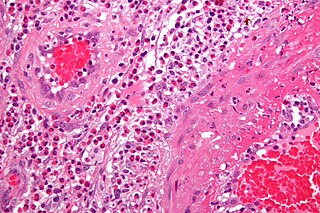
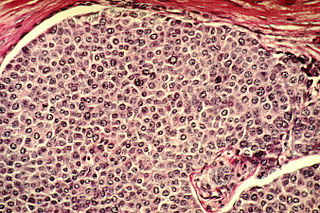
Tümör mikro çevresi

Tümör mikro çevresi (TME), tümörün etkileşim içerisinde olduğu hücresel ortamdır.[1] Bu hücresel ortam; kanser hücrelerini, stromal dokuyu (bağışıklık hücreleri, fibroblastlar, miyofibroblastlar, sitokinler ve vasküler doku) ve hücre dışı matriksi ("extracellular matrix", ECM) içeren dinamik bir ağı oluşturmaktadır.[2] TME, tümördeki kanserli olmayan hücreleri ve bu hücreler tarafından ifade edilen, tümör büyümesine katkıda bulunan proteinleri içermektedir. Yapılan çalışmalar, tümör mikro çevresinin kanser tedavilerine direnci artıran kritik bir faktör olduğunu göstermektedir.[3]
Tümör gelişimi, nüksü ve metastazları sadece kanser hücreleri tarafından belirlenmemektedir. Aynı zamanda TME'nin tümöral olmayan hücreleriyle de ilişkilidir. Makrofajlar, dendritik hücreler, T hücreleri, endotelyal hücreler ve fibroblastlar gibi hücrelerin yanı sıra ECM bileşenleri, proteazlar ve sitokinlerin de tümör gelişiminde rol oynadığı kabul edilmektedir.[1][4][5]
Hücre Dışı Matriks ("Extracellular Matrix", ECM)

ECM; kolajen, elastin, hyaluronan, proteoglikan, polisakkaritler, ilgili enzimler ve büyüme faktörlerini içeren bileşenlerinin etkileriyle hücre çoğalmasını düzenler. Bu bileşenler bir araya gelmesi, hücre davranışlarının düzenlenmesinde kritik role sahiptir.[6]
TME'de ECM'nin biyomekanik ve fiziksel özellikleri, karsinojenez ve metastazı kolaylaştıracak şekilde değişime uğrar. ECM yapısı, protein makromoleküllerini hidrolize edebilen MMP-matriks metaloproteinazlar olarak adlandırılan enzimler tarafından yeniden modellenebilmektedir.[7] Çalışmalarda, MMP'lerin insan kanserlerinde ifadesinin fazla olduğu gösterilmiştir.[8] Kanserle ilişkili fibroblastlar (CAF'ler) ve bağışıklık hücreleri, ECM'nin parçalanmasından sorumlu olan proteaz ailesinin (ürokinaz, katepsinler ve matriks metaloproteinazlar) enzimlerini salgılamaktadır. Bu süreç invazyon, anjiyogenez ve hücre göçüne neden olur. Lisil oksidaz tarafından başlatılan kolajen ve bileşenlerin çapraz bağlanması, artmış stromal sertlik ve yoğunluktan sorumludur. Kolajen çapraz bağlanma durumunun artışı, kemoterapötik ajanların girişini engeller. Bu süreç ilaç direncine yol açmaktadır.[9][10]
Kanser İlişkil Fibroblastlar ("Cancer Associated Fibroblasts", CAF)
CAF, kanser hücrelerinin büyümesini ve invazyonunu destekleyen TME'nin bileşenlerinden biridir. Diğer yandan CAF'lerin vasküler endotelyal büyüme faktörü (VEGF) ve fibroblast büyüme faktörü (FGF) gibi anjiyogenez sürecine dahil olan çeşitli büyüme faktörlerini salgılayarak damarlanmada da rol almaktadır.[11] ECM sertliğinin (ECM-stiffnes), hücresel davranışların yönlendirilmesi üzerinde kritik bir etkisi vardır.[12] Çoğunlukla mekanotransdüksiyon yoluyla artan sertlik, farklı hücre türlerinde biyolojik yanıtları modüle edebilir. ECM sertliği, stromal fibroblastların CAF'a farklılaşmasında önemli bir rol oynar.[13]
CAF'lar, iğ şekline sahip olmaları açısından morfolojik olarak miyofibroblastlara benzer. CAF'lar, herhangi bir doku zedelenmesi sonrasında yara iyileşmesi sürecinde aktive olmaktadır. Yara iyileşmesi süreci tamamlandıktan sonra, normal fibroblastlara geri dönmekte veya apoptoz sürecine girmektedir.[9] Ancak TME'de CAF'ler fibroblastlara geri dönmemekte ve apoptoz sürecine girmemektedir.[14] Bu süreç tümör mikro çevresinin oluşması ve kanser hücrelerinin proliferasyonu için uygun bir ortamı oluşturmaktadır.
Tablo 1. Tümör Mikro çevresinde Bulunan Hücreler ve Rolleri
| HÜCRE TİPLERİ | TÜMÖR DOKUSUNDAKİ ROLÜ |
| Tümör-ilişkili makrofaj (TAM) | · İmmünosupresyon; sitokinler ve büyüme faktörleri üretir. · Tümörün yeniden şekillenmesi; matris metaloproteinazlar (MMP'ler) ve ürokinaz tipi plazminojen aktivatörü (uPA) salgılar. |
| Nötrofil | · Sitokinler ve reaktif oksijen türleri üretir. |
| Treg hücresi | · İmmünosupresyon; sitotoksik T hücrelerin ve doğal öldürücü hücrelerin anti-tümör aktivitesini inhibe eden dönüştürücü büyüme faktörü (TGF)-β ve interlökin (IL)-10 salgılar. |
| Th hücresi | · Bağışıklık sistemini baskılayan sitokinlerin üretimi |
| B hücresi | · Sitokin üretimi ve mast hücrelerinin aktivasyonu |
| Mezenkimal kök hücre | · Tümör yayılımını ve metastazı teşvik eden sitokinler üretir; · Kanser hücrelerini yeniler. |
| Kanser-ilişkili fibroblast (CAF) | · Tümörün yeniden şekillenmesinde rol oynayan MMP'leri salgılar; · Anjiyogenezi indükleyen vasküler endotelyal büyüme faktörü (VEGF) üretir. |
| Vasküler endotel hücresi | · Tümör büyümesini ve metastazı destekleyen kan damarları oluşturur. |
Bağışıklık Hücreleri - T ve B Lenfositler
T lenfositleri, adaptif anti-tümör immün tepkisinin en güçlü aracılarıdır. CD4 + T yardımcı (Th1) hücreler tarafından desteklenen sitotoksik CD8 + T hücre popülasyonu, tümör eliminasyonu bağlamında ana mekanizmayı oluştururmaktadır.[15][16] Çeşitli interlökinler üreten CD4 + T hücresi alt kümeleri Th2 ve Th17, genellikle doku inflamasyonu ve pro-tümörijenik etki ile ilişkilidir. CD8 aracılı bağışıklık yanıtı, CD4 + T hücreleri sınıfı tarafından modüle edilir. Bu yanıt, bağışıklık toleransını yöneten CD25 ve FOXP3 molekülleri üzerinden olur. T düzenleyici (Treg) olarak bilinen bağışıklık bastırıcı CD4 + T hücreleri bu süreçte görev almaktadır.[17]
TME'de, yüksek miktarda Treg hücreleri bulunur. Bu hücrelerin ana rolü, anti-tümör cevabı baskılamaktır.[18] Tümör parankiminde inhibe edici hücreler (makrofajlar, fibroblastlar, Treg, baskılayıcı miyeloid hücreler ve B hücreleri) ile hem CD8 + hem de CD4 + T hücreler aynı anda bulunabilmektedir. Bu hücreler, inhibitör reseptörlerin ifadesini artırıp T hücresi işlev bozukluğuna-tükenmesine yol açarak T lenfosit işlevselliğini etkilemektedir.[19]
B hücreler, tümör bağışıklığında hem olumlu hem de olumsuz etkilerle ilişkilendirilebilmektedir. B hücrelerinin anti-tümör rolü, fare modellerinde bildirilmiştir. Bu durum B hücrelerinin T hücresi işlevselliğini artırdığını göstermektedir.[20][21] Diğer yandan koruyucu role rağmen, fare skuamöz karsinojenez modelinde yapılan çalışmalar B hücrelerin anti-tümör bağışıklığını bozacak şekilde etki gösterebildiğini belirtilmektedir.[22] Tüm bu veriler T ve B lenfositlerin tümör dokusuna karşı cevaplarının değişken olabileceğini raporlamaktadır. Bu değişkenliğin modüle edilebilmesi ile yeni tedavi yaklaşımları oluşturulabilir.
Tümör İlişkili Makrofajlar ("Tumor-Associated Macrophages", TAM)
Tümör stromasında bulunan bağışıklık hücresi popülasyonları, kansere bağlı inflamasyonun düzenlenmesinde önde gelen "tümör ilişkili makrofajlardan" (TAM'ler) oluşur. Klinik öncesi ve klinik veriler, TME'de yüksek miktarda TAM bulunmasının kanserin kötü ilerleyişi ile ilişkili olduğunu göstermiştir.[23] TAM, antitümör bağışıklığını baskılayabilen ve tümör ilerlemesini destekleyebilen sitokinleri ve kemokinleri ifade etmektedir.[24] Patojenlere karşı önemli bir rol oynayan proinflamatuar makrofajlar, IFNy, TNFa ve mikrobiyal ürünler gibi sitokinler tarafından yönlendirilir. Bu makrofaj grubu M1 alt tipi olarak adlandırılır. Diğer yandan IL-4 veya IL-13, makrofaj farklılaşmasında tümör destekleyici M2 alt tipi polarizasyonunu oluşturur. Bu süreç M2 makrofajların meydana gelmesi ile T hücresi işlevselliğini engelleyen bir immün baskılayıcı TME oluşumuna katkıda bulunur.[25] Tümör dokusunda makrofajları hedefleyen birkaç farmakolojik ajan denemesi, deneysel ortamda anlamlı sonuçlar göstermiştir. Bu veriler TAM'ı tümör tedavi yaklaşımlarında kritik bir hedef haline getirmektedir.[24] Gelecekte planlanan klinik araştırmalarda yeni terapötik denemeler bağlamında umut vermektedir.
Kaynakça
- ^ a b "Tumor microenvironment: Sanctuary of the devil".
- ^ "The tumor microenvironment in the post-PAGET era".
- ^ "The tumor microenvironment is a dominant force in multidrug resistance".
- ^ "microRNA-mediated regulation of the tumor microenvironment".
- ^ "Tumor-Derived Exosomes and Their Role in Cancer Progression".
- ^ "The extracellular matrix: A dynamic niche in cancer progression".
- ^ "The tumor microenvironment".
- ^ "The possible role of matrix metalloproteinase (MMP)-2 and MMP-9 in cancer, e.g. acute leukemia."
- ^ a b "Tumor microenvironment targeted nanotherapeutics for cancer therapy and diagnosis: A review".
- ^ "Nanomedicine targeting the tumor microenvironment: Therapeutic strategies to inhibit angiogenesis, remodel matrix, and modulate immune responses".
- ^ "Cancer-associated fibroblasts affect breast cancer cell gene expression, invasion and angiogenesis".
- ^ "Cancer associated fibroblasts (CAFs) in tumor microenvironment".
- ^ "Biophysics of Tumor Microenvironment and Cancer Metastasis - A Mini Review".
- ^ "The role of multipotent cancer associated fibroblasts in hepatocarcinogenesis".
- ^ "The immune contexture in cancer prognosis and treatment".
- ^ "The immune contexture in human tumours: impact on clinical outcome".
- ^ "Regulatory T cells: mechanisms of differentiation and function".
- ^ "Immunometabolic Checkpoints of Treg Dynamics: Adaptation to Microenvironmental Opportunities and Challenges".
- ^ "Signatures of T cell dysfunction and exclusion predict cancer immunotherapy response".
- ^ "B cells are required for optimal CD4+ and CD8+ T cell tumor immunity: therapeutic B cell depletion enhances B16 melanoma growth in mice".
- ^ "B cells are associated with survival and immunotherapy response in sarcoma".
- ^ "De novo carcinogenesis promoted by chronic inflammation is B lymphocyte dependent".
- ^ "Tumour-associated macrophages as treatment targets in oncology".
- ^ a b "Targeting Tumor-Associated Macrophages in Cancer".
- ^ "Macrophage activation and polarization: nomenclature and experimental guidelines".