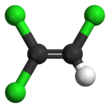
Trikloroetilen
 | |||
| |||
 | |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Trikloroeten | |||
Diğer adlar 1-kloro-2,2-dikloroetilen 1,1-dikloro-2-kloroetilen Asetilen Triklorür Anamenth HCC-1120 TCE Trethylene Triclene Tri Trico Trilene Trimar Chloréthérise (Laurent, 1835) | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| Kısaltmalar | TCE | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.001.062 | ||
| EC Numarası |
| ||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | C2HCl3 | ||
| Molekül kütlesi | 131,39 g mol−1 | ||
| Görünüm | renksiz sıvı | ||
| Koku | Kloroform benzeri[1] | ||
| Yoğunluk | 1,46 g/cm3 (20 °C'de) | ||
| Erime noktası | -84,8 °C (-120,6 °F; 188,3 K)[4] | ||
| Kaynama noktası | 87,2 °C (189,0 °F; 360,3 K)[5] | ||
| Çözünürlük (su içinde) | 1,280 g/L[2] | ||
| Çözünürlük | Eter, etanol, kloroform | ||
| log P | 2,26[3] | ||
| Buhar basıncı | 58 mmHg (0,076 atm) 20 °C'de[1] | ||
| -65,8·10−6 cm3/mol | |||
| Kırınım dizimi (nD) | 1,4777 (19,8 °C'de) | ||
| Akmazlık | 0,532 mPa·s[6] | ||
| Farmakoloji | |||
| N01AB05 (DSÖ) | |||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | kanserojen | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  | ||
| NFPA 704 (yangın karosu) | |||
Kendiliğinden tutuşma sıcaklığı | 420 °C (788 °F; 693 K) | ||
| Patlama sınırları | %8-10,5[1] | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LC50 (medyan konsantrasyon) | 8450 ppm (fare, 4 sa) 26300 (sıçan, 1 sa)[7] | ||
LCLo (yayınlanan en düşük) | 2900 ppm (insan) 37200 ppm (hint domuzu, 40 d) 5952 ppm (kedi, 2 sa) 8000 ppm (sıçan, 4 sa) 11000 (tavşan)[7] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 100 ppm C 200 ppm 300 ppm (Herhangi bir 2 saatte 5 dakikalık maksimum zirve)[1] | ||
| REL (tavsiye edilen) | Ca[1] | ||
| IDLH (anında tehlike) | Ca [1000 ppm][1] | ||
| Güvenlik bilgi formu (SDS) | Mallinckrodt Baker | ||
| Hukuki durum |
| ||
| Benzeyen bileşikler | |||
Benzeyen vinil halojenürler | Vinil klorür | ||
Benzeyen bileşikler | Kloroform 1,1,1-Trikloroetan 1,1,2-Trikloroetan Tetrakloroetilen | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Trikloroetilen (TCE), C2HCl3 formülüne sahip bir organoklorür. Renksiz bir sıvıdır ve Kloroform benzeri bir kokuya sahiptir. Düşük sıcaklıklarda yanıcı değildir. Sanayide özellikle metaller için yağ çözücü olarak kullanılır. Geçmişte Trilene adı altında inhalasyon anesteziği ve obstetrik analjezik olarak kullanıldı. Metal temizliği gibi benzer alanlarda kullanılan trikloroetan ile karıştırılmamalıdır.
Tarihçe
Trikloroetilen sentezinin en eski kaydı 1836'ya kadar uzanır. Auguste Laurent tarafından, potasyum hidroksitin 1,1,2,2-tetrakloroetan ve 1,1,1,2-tetrakloroetan üzerindeki etkisinden elde edildi ve formülü C
4HCl
3 olarak not edildi (o dönemlerde karbonun atom ağırlığının, gerçekte olanın yarısı kadar olduğu düşünülüyordu). Laurent, bileşiği elinde yeterli miktarda bulunmadığı için daha fazla araştıramadı.[9][10]
Trikloroetilen, 1864 yılında Alman doktor E. Fischer tarafından hekzakloroetanın hidrojen ile indirgenmesiyle elde edildi ve araştırıldı. Fischer, kimyasalın kaynama noktasının 87 ile 90 santigrat derece arasında olduğunu kaydetti.[11][12]
Ticari üretimi 1920'de Almanya'da ve 1925'te ABD'de başladı.[13]
Gıda ve ilaç endüstrilerinde trikloroetilenin kullanımı, toksisitesi ile ilgili endişeler nedeniyle 1970'lerden beri dünyanın birçok yerinde yasaklanmıştır. Mevzuat, kimyasal R45: Kansere neden olabilir risk ibaresi taşıyan kanserojen olarak sınıflandırıldığından, Avrupa'daki birçok işlemde trikloroetilenin yerinin değiştirilmesini zorunlu kılmıştır.
1995 yılında Jonathan Harr tarafından yazılan A Civil Action kitabı, 1970'lerde şebeke suyundaki trikloroetilen kirlenmesi sonrası çocuklarda artan lösemi vakaları nedeniyle iki şirkete karşı açılan bir davayı (Anderson v. Cryovac) konu edinmiş ve 1998 yılında sinemaya uyarlanmıştır.
Üretimi
1970'lerin başından önce, çoğu trikloroetilen asetilenden iki aşamalı bir işlemle üretildi. İlk olarak asetilen, kimyasal denkleme göre 1,1,2,2-tetrakloroetan üretmek için 90 °C'de bir ferrik klorür katalizörü kullanılarak klor ile işlenir:
- HC≡CH + 2 Cl2 → Cl2CHCHCl2
1,1,2,2-Tetrakloroetan daha sonra trikloroetilen verecek şekilde dehidroklorine edilir. Bu, sulu bir kalsiyum hidroksit çözeltisi ile gerçekleştirilebilir:
Ancak günümüzde çoğu trikloroetilen etilenden üretilmektedir. İlk olarak etilen, 1,2-dikloroetan üretmek için bir ferrik klorür katalizörü üzerinde klorlanır:
- CH2=CH2 + Cl2 → ClCH2CH2Cl
Fazladan klor ile yaklaşık 400 °C'ye ısıtıldığında 1,2-dikloroetan, trikloroetilene dönüştürülür:
- ClCH2CH2Cl + 2 Cl2 → ClCH=CCl2 + 3 HCl
Bu reaksiyon, çeşitli maddeler tarafından katalize edilebilir. En yaygın olarak kullanılan katalizör, potasyum klorür ve alüminyum klorürün bir karışımıdır. Bununla birlikte, gözenekli karbonun çeşitli formları da kullanılabilir. Bu reaksiyon, bir yan ürün olarak tetrakloroetilen üretir ve reaksiyona beslenen klor miktarına bağlı olarak, tetrakloroetilen ana ürün bile olabilir. Tipik olarak trikloroetilen ve tetrakloroetilen birlikte toplanır ve daha sonra damıtma yoluyla ayrılır.
Reaktan ve teknik TCE'deki yaygın safsızlıklar; metil kloroform, karbon tetraklorür, etilen diklorür, tetrakloroetanlar, benzen ve fenoldür. Ancak bu bileşikler çok küçük miktarlarda bulunur ve herhangi bir risk taşımazlar.[14]
Kullanımları
Metallerin yağlarının temizlenmesinde, ekstraksiyon çözücüsü olarak yağ ve wax'larda, boyalarda çözücü olarak, kuru temizlemede leke çıkarıcı, soğutucu ve ısı transferi sıvısı olarak, elektronik parçaların temizlenmesinde, boya ve tutkallarda seyreltici, tekstil sanayiinde kimyasal ara madde, havacılık endüstrisinde ise sıvı oksijen püskürtülmesinde kullanılır.
Temizlik
Trikloroetilen geçmişte yaygın olarak kuru temizleme çözücüsü olarak da kullanılmıştır, ancak leke temizleme dışında çoğunlukla tetrakloroetilen (perkloroetilen olarak da bilinir) ile değiştirilmiştir.
Büyük ihtimalle TCE'nin en yaygın kullanımı metal parçalar için yağ çözücü olarak kullanılmasıdır. Düşük maliyeti, düşük yanıcılığı, düşük toksisitesi ve yüksek etkinliği nedeniyle 1920'li yıllardan beri yağ giderme ve temizlemede yaygın olarak kullanılmaktadır. Yağ giderici olarak TCE'ye olan talep, 1950'lerde daha az toksik olan 1,1,1-trikloroetan lehine azalmaya başladı. Bununla birlikte, 1,1,1-trikloroetan üretimi dünyanın birçok yerinde Montreal Protokolü uyarınca aşamalı olarak kaldırılmıştır ve bunun sonucunda trikloroetilenin yağ giderici olarak kullanımı yeniden yaygınlaşmıştır.[14]
Trikloroetilen, dokumadan önce yündeki yağı ve lanolini uzaklaştırmak için kullanılır.[14]
TCE, Amerika Birleşik Devletleri'nde kerosen yakıtlı roket motorlarını temizlemek için de kullanılmıştır (TCE, hidrojen yakıtlı motorları temizlemek için kullanılmamıştır). Statik ateşleme sırasında, RP-1 yakıtı motorda hidrokarbon birikintileri ve buharlar bırakacaktır. Motor kullanımı ve gelecekteki ateşleme sırasında patlama olasılığını önlemek için bu birikintilerin motordan yıkanması gerekiyordu. TCE, her test ateşlemesinden hemen önce ve sonra motorun yakıt sistemini yıkamak için kullanıldı. Yıkama prosedürü, TCE'nin motorun yakıt sisteminden pompalanmasını ve motora bağlı olarak solventin birkaç saniye ile 30-35 dakika arasında değişen bir süre boyunca taşmasına izin verilmesini içeriyordu.[15][16]
Anestezi


Britanya'daki Imperial Chemical Industries'in "Trilene" ticari adı altında öncülük ettiği bu gelişme, anestezide bir devrim olarak görüldü. Amerika Birleşik Devletleri'nde çoğunlukla "Trimar" olarak biliniyordu, –mar son eki, Maryland Üniversitesi'ndeki çalışma ve geliştirmeyi belirtir; örneğin, fluroksen için "Fluoromar" ve etil vinil eter için "Vinamar" isimleri verildi.[17] Başlangıçta kloroformdan daha az hepatotoksisiteye sahip olduğu ve eterin "hoş olmayan keskinliği" ve yanıcılığı olmadığı düşünüldüğünde, yine de daha sonraları TCE'nin sanıldığı kadar masum olmadığı kısa süre sonra ortaya çıktı. Yan etkileri arasında kardiyak aritmiler, hızlı anestezi indüksiyonunu önleyen düşük uçuculuk ve kanda yüksek çözünürlük, karbon dioksit absorbe eden sistemlerde kullanılan soda kireç ile reaksiyonlar, soda kireç ile kullanıldığında uzun süreli nörolojik işlev bozukluğu ve kloroformunkine yakın hepatotoksisite yer alır.
Avrupa ve Kuzey Amerika'da 1930'lar ila 1970'ler arasında Trimar ve Trilene isimleri altında uçucu anestetik olarak kullanılmıştır. Birleşik Krallık'ta "Trilene" ismi altında, benzer kokulu kloroform ile karıştırılmaması için maviye boyanarak satılmıştır. TCE, 1940'larda kloroform ve dietil eter gibi ilk dönem anesteziklerinin yerini almıştır, kendisinin yeri 1960'larda halotan tarafından alınmıştır.
Trikloroetilen anestezisi, Türkiye'ye ilk olarak 1947'de getirilmiş ve 1950'de kullanılmaya başlanmıştır.[18] Trikloroetilenin anestezik olarak kullanımı, 1984 öncesinde Sağlık Bakanlığı tarafından yasaklanmıştır.[19]
1956'da halotanın piyasaya sürülmesi, TCE'nin genel anestezik olarak kullanımını büyük ölçüde azalttı. TCE'nin fetal toksisitesi ve kanserojenik potansiyeline ilişkin endişeler, 1980'lerde gelişmiş ülkelerde anestezide kullanımının terk edilmesine yol açtı. 2000 yılındaki verilere göre hâlâ Afrika'da TCE anestezik olarak kullanılmaktaydı.[20]
Uyuşturucu niyetine kullanımı
TCE, keyif verici madde olarak kullanılmıştır.[21] Trikloroetileni eğlence amaçlı almanın yaygın yöntemleri arasında bir bezden soluma (inhalasyon anesteziği alımına benzer şekilde) ve içme yer alır.[22] TCE'yi bu niyetle kullananların çoğu, gençler ve kimyasalı işyerlerinde kullanan işçilerdi. Kötüye kullanımın ana nedeni, TCE'nin coşku verici ve hafif halüsinojenik etkisidir.[22] Bazı işçilerin TCE'ye bağımlı olduğu gözlemlenmiştir.[23]
Güvenlik
Amerika Birleşik Devletleri'nde, Trikloroetilen içeren endüstriyel atıklardan kaynaklanan yeraltı suyu ve içme suyu kirliliği, insan sağlığı için büyük bir endişe kaynağıdır ve çok sayıda davaya yol açmıştır.
Kimyasal kararsızlık
Metallerin yağlardan arındırılmasında geniş bir kullanım alanına sahip olmasına rağmen trikloroetilen zaman içinde metallere maruz kaldığında stabilitesini yitirir ve bozunmaya başlar. Bu fenomen 1961 gibi erken yıllarda fark edildiğinde ticarî trikloroetilene stabilizatörler katılmaya başlandı. Genellikle stabile edilmesi için etil metil keton kullanılır. TCE için stabilizatör olarak 1,4-dioksanın kullanımına dair bilgi, TCE formülasyonlarını açıklayan eski patent literatüründeki eksiklik nedeniyle yetersizdir.[24][25]
Fizyolojik etkileri
Trikloroetilenin solunması, merkezî sinir sistemine anestezik etki eder. GABA reseptörlerini inhibe eder. Düşük konsantrasyonlarısolunum yollarını tahriş etmez.
1940'larda, TCE'nin karbon dioksit absorbe sistemlerinde (sodyum hidroksit ve kalsiyum oksit) tepkimeye girip aşırı zehirli fosgen ve nörotoksik dikloroasetilen bileşiklerini oluşturduğu anlaşılmıştır.[26] Ameliyat için yeterli olan TCE anestezisinde kas gevşemesi yetersizdi. Hepatotoksisite ile ilgili sorunların yanı sıra bu nedenlerden dolayı, TCE 1960'larda Kuzey Amerika ve Avrupa'da halotan gibi daha güçlü anesteziklere popülaritesini kaybetti.[27]
Tıbbî olmayan akut maruziyetin semptomları, baş dönmesi ve kafa karışıklığı ile başlar, artan maruziyetle bilinç kaybına kadar gider, sarhoşluk semptomlarına benzer.[28]
Trikloroetilenin insan sağlığına etkileri hakkında bilinenlerin çoğu meslekî maruziyetlere dayanmaktadır. Merkezî sinir sistemi üzerindeki etkilerin ötesinde, işyerinde trikloroetilene maruz kalma, karaciğer ve böbreklerde olumsuz etkilerle ilişkilendirilmiştir.[28]
Amerikan eyalet ve federal sağlık kuruluşları ve uluslararası kuruluşlar, trikloroetileni bilinen veya olası kanserojen olarak sınıflandırıyor. 2014 yılında, Uluslararası Kanser Araştırma Ajansı, trikloroetilenin sınıflandırmasını Grup 1 olarak güncelledi; bu, insanlarda böbrek kanserine neden olduğuna ve ayrıca karaciğer kanseri ve lenfoma ile ilgili bazı kanıtlara neden olduğuna dair yeterli kanıtın mevcut olduğunu belirtti.[29]
Maruziyet ve düzenlemeler
Genel olarak, atmosferik TCE seviyeleri sanayinin ve nüfusun yoğunlaştığı bölgelerde en yüksektir. Kırsal ve uzak bölgelerde atmosferik seviyeler en düşük olma eğilimindedir.
Özgül ağırlığı 1'den büyük (sudan daha yoğun) olan trikloroetilen, eğer çevreye yeterli miktarda dökülürse yoğun susuz faz sıvısı (DNAPL) olarak bulunur.
Yeraltı suyunda TCE'nin bilinen ilk raporu, 1949'da, TCE'nin endüstriyel salınımlarından kaynaklanan iki ayrı kuyuda kirlenme örneğini tanımlayan iki İngiliz kimyager tarafından verildi.[30] Mevcut federal ve eyalet araştırmalarına göre, ABD'de test edilen içme suyu tedarik kaynaklarının %9 ila %34'ü bir miktar TCE kirliliğine sahip olabilir. EPA, çoğu su kaynağının 5 ppb'lik maksimum kirletici madde düzeyine (MCL) uygun olduğunu bildirmiştir.[31] EPA'ya göre, trikloroetilen hem solunum hem de deri yoluyla maruz kalma nedeniyle tehlikelidir ve en güçlü şekilde, akut maruz kalma durumunda bağışıklık sistemini baskılayıcı etkilerle, ayrıca kronik maruz kalmalarda otoimmün etkilerle ilişkilidir.[32]
2023 yılında iki ABD eyaleti, Minnesota ve New York, trikloroetileni yasaklamıştır.[33][34]

İşçileri sağlıklarına yönelik risklere karşı korumayı amaçlayan mevcut AB mevzuatı (Kimyasal Maddeler Direktifi 98/24/EC ve Kanserojen Direktifi 2004/37/EC dâhil) şu anda Trikloroetilenin kullanımda işçilere yönelik risklerin kontrol altına alınmasına yönelik bağlayıcı, asgari gereklilikler getirmemektedir.
Remediasyon
Son araştırmalar, trikloroetilenin toprak ve yeraltı suyunda, saha dışında yok edilmek üzere uzaklaştırılması yerine, yerinde yok edilmesine odaklanmıştır. Doğal olarak oluşan Dehalococcoides türü bakterilerin TCE'yi parçalama yeteneğine sahip olduğu tespit edilmiştir. Anaerobik koşullar altında indirgeyici klorsuzlaştırma yoluyla trikloroetileni yok eder. Aerobik koşullar altında Pseudomonas fluorescent, TCE'yi metabolize edebilir.
TCE'nin neden olduğu toprak ve yeraltı suyu kirliliği de kimyasal arıtma ve ekstraksiyon yoluyla başarılı bir şekilde giderilmiştir. Nitrosomonas europaea bakterisi, trikloroetilen de dâhil olmak üzere çeşitli halojenli bileşikleri parçalayabilmektedir.[35] Toluen dioksijenazın, Pseudomonas putida tarafından TCE'nin bozulmasında rol oynadığı rapor edilmiştir. Bazı durumlarda Xanthobacter autotrophicus, TCE'nin %51'e kadarını CO ve CO
2'ye dönüştürebilir.[36]
Kaynakça
- ^ a b c d e f NIOSH Pocket Guide to Chemical Hazards. "#0629". National Institute for Occupational Safety and Health (NIOSH).
- ^ "Trichloroethylene". Sigmaaldrich.com. 26 Aralık 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Ekim 2014.
- ^ "Trichloroethylene". www.chemsrc.com. 11 Temmuz 2017 tarihinde kaynağından arşivlendi.
- ^ "Safety Data Sheet". 29 Aralık 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Şubat 2022.
- ^ ChemIDplus veritabanından Trikloroetilen
- ^ Venkatesulu, D.; Venkatesu, P.; Rao, M. V. Prabhakara (1997). "Viscosities and Densities of Trichloroethylene or Tetrachloroethylene with 2-Alkoxyethanols at 303.15 K and 313.15 K". Journal of Chemical & Engineering Data. 42 (2): 365-367. doi:10.1021/je960316f. ISSN 0021-9568.
- ^ a b "Trichloroethylene". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ Anvisa (31 Mart 2023). "RDC Nº 784 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial" [Collegiate Board Resolution No. 784 - Lists of Narcotic, Psychotropic, Precursor, and Other Substances under Special Control] (Portekizce). Diário Oficial da União (4 Nisan 2023 tarihinde yayınlandı). 3 Ağustos 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Ağustos 2023.
- ^ Essai sur l'Action du Chlore sur la Liqueur des Hollandais et sur quelques Ethers in Annal. de Chimie, LXIII. (1836) page 379 29 Ekim 2023 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ The so-called Perchloride of Formyl, Gmelin, L. (İngilizce çevirisi 1855 basımı). Hand-book of Chemistry: Organic chemistry. UK: Cavendish Society. pages 200–201 29 Ekim 2023 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Waters EM, Gerstner HB, Huff JE. Trichloroethylene. I. An overview. J Toxicol Environ Health. 1977 Jan;2(3):671-707. doi: 10.1080/15287397709529469. PMID 403297.
- ^ Hardie DWF (1964). Chlorocarbons and chlorohydrocarbons. 1,1,2,2-Tetrachloroethane. In: Encyclopedia of Chemical Technology. Kirk RE, Othmer DF, editors. New York: John Wiley & Sons, s. 159–164
- ^ Mertens JA (1993). Chlorocarbons and chlorohydrocarbons. In: Kirk-Othmer Encyclopedia of Chemical Technology, 4th Ed. Kroschwitz JI, Howe-Grant M, editors. New York: John Wiley & Sons, s. 40–50.
- ^ a b c Bölüm 4: Trichloroethylene, Morrison, R. D., Murphy, B. L. (2015). Chlorinated Solvents: A Forensic Evaluation: Royal Society of Chemistry. Kaynak hatası: Geçersiz
<ref>etiketi: "forensic" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ "Santa Susana Field Laboratory : The Use of Trichloroethylene at NASA's SSFL Sites" (PDF). Ssfl.msfc.nasa.gov. 14 Kasım 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 22 Şubat 2015.
- ^ "F-1 Rocket Engine Operating Instructions". Ntrs.nasa.gov. 15 Mart 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Ekim 2014.
- ^ A Portrait of Medical History and Current Medical Problem (1962), p. 130
- ^ Türkiye'de Anesteziyoloji ve Reanimasyon Biliminin Tarihsel Gelişimi
- ^ Anesteziyoloji (1984)
- ^ P. Fenton (2000). "Volatile Anaesthetic Agents". 7 Ocak 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Şubat 2012.
- ^ Trichloroethylene 5 Aralık 2023 tarihinde Wayback Machine sitesinde arşivlendi. in Neurology in Clinical Practice, Daroff, R. B., Fenichel, G. M., Jankovic, J., Mazziotta, J. C. (2012).
- ^ a b Chapter 50: Trichloroethylene 5 Aralık 2023 tarihinde Wayback Machine sitesinde arşivlendi. Medical Toxicology of Drug Abuse: Synthesized Chemicals and Psychoactive Plants.Barceloux, D. G. (2012).
- ^ Trichlorethylene Addiction and its Effects (1972) Boleslaw Alapin M.D., M.R.C. Psych. British Journal of Addiction to Alcohol & Other Drugs, Volume 68, Issue 4 p. 331-335 DOI
- ^ Murphy, Brian L; Morrison, Robert D. (2015). "9. Source Identification and Age Dating of Chlorinated Solvents". Introduction to environmental forensics (3. bas.). sec. 9.2.2.1 1,4-Dioxane: Academic Press. ISBN 978-0124047075.
- ^ Mohr, Thomas K. G. (2010). "Historical Use of Chlorinated Solvents and Their Stabilizing Compounds". Environmental investigation and remediation: 1,4-dioxane and other solvent stabilizers. p. 53 "Was 1,4-Dioxane a Stabilizer for Trichloroethylene?": CRC Press. ISBN 978-1566706629.
- ^ Orkin, F. K. (1986) Anesthesia Systems (Chapter 5). In R. D. Miller (Ed.), Anesthesia. New York, NY: Churchill Livingstone.
- ^ Stevens, W.C. and Kingston H. G. G. (1989) Inhalation Anesthesia (Chapter 11). In P. G. Barash et al. (Eds.) Clinical Anesthesia. Philadelphia, PA: Lippincott
- ^ a b "Trichloroethylene | Technology Transfer Network Air Toxics Web site | US EPA". Epa.gov. 11 Haziran 2002 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ekim 2013.
- ^ Trichloroethylene (IARC Summary & Evaluation, Volume 106, 2014) (PDF). iarc.fr. 11 Mart 2016 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 8 Mart 2016.
- ^ Lyne FA, McLachlan T (1949). "Contamination of water by trichloroethylene" s. 513, Lilliman, B.; Houlihan, J. E.; Lyne, F. A.; McLachlan, T. (1949). "Notes". The Analyst. 74 (882): 510-513. Bibcode:1949Ana....74..510L. doi:10.1039/AN9497400510.
- ^ "Consumer Factsheet on: Trichloroethylene" (PDF). Epa.gov. 24 Eylül 2015 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 22 Şubat 2015.
- ^ US EPA, OCSPP (12 Şubat 2020). "Final Risk Evaluation for Trichloroethylene" (PDF). www.epa.gov (İngilizce). 3 Haziran 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Haziran 2023.
- ^ "How Minnesota passed the country's first ban on trichloroethylene". www.pca.state.mn.us/news-and-stories (İngilizce). Minnesota Pollution Control Agency. 28 Ağustos 2023. 6 Eylül 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Eylül 2023.
- ^ "Chapter 116, Section 116.385". Minnesota Statutes (act) (İngilizce). 2022. 6 Eylül 2023 tarihinde kaynağından arşivlendi. Bilinmeyen parametre
|index=görmezden gelindi (yardım); Bilinmeyen parametre|article-type=görmezden gelindi (yardım); Bilinmeyen parametre|legislature=görmezden gelindi (yardım) - ^ "Nitrosomonas europaea". Genome.jgi-psf.org. 5 Şubat 2015. 3 Temmuz 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Şubat 2015.
- ^ Robert L. Irvine; Subhas K. Sikdar (1998). Bioremediation Technologies: Principles and Practice. CRC Press. ss. 142, 144. ISBN 978-1566765619. 15 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Şubat 2015.