
Asit, pH derecesi 7'den düşük olup, değişen oranlarda yakıcı ve/veya aşındırıcı özelliğe sahip olan ve oldukça geniş kullanım alanına sahip kimyasal maddelere verilen isimdir. Suda çözündüklerinde hidrojen iyonu derişimini artırarak çözeltiyi asidik yapar. Mavi turnusol kâğıdının rengini kırmızıya çeviren asitlere eski Türkçede hamız veya ekşit denir.
pH belirteçleri (İndikatörler), çözeltinin pH'sine bağlı olarak renk değiştiren, karmaşık yapıdaki organik bileşiklerdir. Bu tür bileşikler, asit ya da baz titrasyonunun bitiş noktasını saptamak amacıyla kullanılır. pH belirteçlerini asit, baz, redoks ve çöktürme belirteçleri olarak sınıflamak mümkündür.

Tuz, kimyada, bir asitle bir bazın tepkimeye girmesi neticesinde meydana gelen maddedir. Tuz, asitteki eksi yüklü iyonla (anyon) bazdaki artı yüklü iyondan (katyon) meydana gelir. Asitle baz arasındaki nötralleşme tepkimesi esnasında tuz ve su açığa çıkar. Erimiş tuz veya çözelti halindeki tuzların çoğu eksi ile artı yüklü iyonlarına ayrışır ve elektriği iletir. Tuz adı ayrıca sofra tuzu veya sodyum klorür (NaCl) için de kullanılır.
Hidroliz işlemi suyu oluşturan hidrojen ve oksijen elementlerinin birbirinden ayrılması ile sonuçlanan bir işlemdir. Bazı kaynaklarda hidroliz, moleküllerin su ilavesiyle daha fazla sayıda parçacık oluşturması olarak da geçer. Hidroliz, su ile bir kimyasal bağın parçalanmasıdır yani bir kimyasal reaksiyondur. Hidroliz genel olarak suyun nükleofil olduğu ikame(yer değiştirme reaksiyonu), eliminasyon(organik reaksiyon türü) ve solvasyon (çözme) reaksiyonları için kullanılır.
Tampon, şu anlamlara gelebilir:
- Tampon bellek, bilgisayar dünyasında "bilgilerin topluca yazılması için arada biriktirildikleri yer".
- Araba tamponu, bir aracın arka ve önünde bulunan şok emici katman.
- Tampon, esas olarak kadınsı hijyen ürünü olarak kullanılan emici bir malzeme.
- Tampon bölge, düşman birlikleri, grupları ya da milletleri birbirinden ayırmak için oluşturulmuş ara bölge.
- Tampon devlet, iki güçlü ve birbirine husumet besleyen devletin arasında kurulan göreli olarak daha küçük ve güçsüz devlet.
- Tampon çözelti, zayıf asit ve konjuge bazın veya zayıf baz ve konjuge asitin karşımından oluşan sulu çözelti
- Tampon mekanizma, sosyoloji kavramı.
- Tampon, Türk punk rock grubu
- Tampon (jinekoloji), hijyen ürünü olarak kullanılan emici bir malzeme
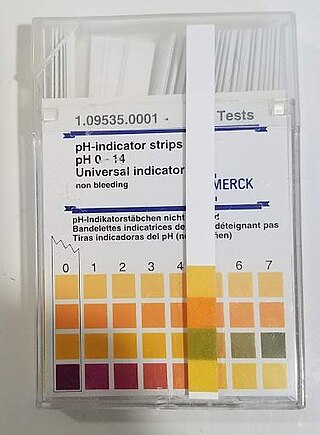
pH, bir çözeltinin asitlik veya bazlık derecesini tarif eden ölçü birimidir. pH'in açılımının ne olduğu kesin olarak bilinmese de genellikle "potential of hydrogen" veya "power of hydrogen" olduğu varsayılır.
Baz, suda iyonlaştıklarında ortama OH− (hidroksit) iyonu ve elektron çifti verebilen maddelerdir. Bazlar da, asitler gibi tehlikeli maddelerdir. Suda iyonlaştıklarında hidroksit (OH−) iyonu derişimini arttıran maddelere baz denir. Bilinen en güçlü baz Sezyum hidroksittir (CsOH).
Turnusol kâğıdı, kimyada kullanılan ayıraçlardan bir tanesidir. Çözeltilerdeki asit ve bazları ayırt etmekte kullanılır. Turnusol, asitle temas ettiğinde kırmızı, bazla temas ettiğinde mavi renk verir. Turnusol belirli likenlerden (kuzukulağı) elde edilen, içeriğinde orsein bulunan ve suda çözünen bir boyadır. Çözelti olarak veya bir filtre kâğıdına emdirilerek kullanılır. Bu kâğıda pH belirteci denir ve maddelerin asitliğini ölçmek için kullanılır. Mavi turnusol kâğıdı asidik ortamlarda kırmızıya ve kırmızı turnusol kâğıdı bazik ortamlarda maviye döner. Renk değişimi 4,5-8,3 pH aralığında menekşe tonlarında olur (25 °C'de). Turnusolün aktif maddesi eritrolitmindir. Düşük pH değerli maddeler asit olarak ve yüksek değerliler alkali olarak adlandırılır. Sadece asit ve bazlar değil, bazı çözünen tuzlar da turnusol kâğıdını mavi veya kırmızıya dönüştürür. Kuvvetli asit ve zayıf bazdan oluşan tuzlar asidik, zayıf asit ve kuvvetli bazdan oluşan tuzlar bazik özellik gösterdiğinden turnusolü boyarlar (hidroliz).

Kimyada amid sözcüğü iki anlama sahiptir: - Birinci anlamıyla amid, bir azot atomuna (N) bağlı bir karbonil grubu bulunduran bir organik fonksiyonel grup veya bu gruba sahip bir bileşiktir. - İkinci anlamıyla amid, bir azot anyonudur.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.
Hidronyum (H3O) ;IUPAC'te adlandırılması oksonyum şeklindedir. Bir molekülünde 3 hidrojen ve 1 oksijen atomu bulunur. Hidronyum iyonu, (H3O) asitler suda çözündüklerinde açığa çıkan katyondur. Aynı zamanda asitleri bazlardan ayırmada kullanılır. (Brønsted-Lowry asit-baz teorisi)Bir asit suda çözündüğü zaman hidronyum katyonu ortaya çıkar. Bazı asit çözünme tepkimelerinde kolaylık olması amacıyla (H+) iyonu şeklinde de gösterilse de doğru kullanımı (H3O) şeklindedir. pH'ın belirlemesinde kullanılır. Eğer çözünen maddenin [H+] konsantrasyonu ile [OH-] eşitse o madde nötrdür.
Kronik rumen asidozu, Acidosis ingesta ruminis chronica, Latent laktik asidoz veya Subakut laktik asidoz (S.A.R.A). Latent asidotik stres (yüklenme) uçucu yağ asitlerinin, bilhassa propiyonik asit sentezi ve rezorpsiyonunun artması, aynı zamanda salya sekresyonunun azalması olayıdır. Rumen pH’sı belirgin şekilde normalden sapmalar göstermediğinden kronik rumen asidozisi ifadesi tam doğru değildir.
Kimyasal reaktiflik, bir reaksiyonun meydana gelme eğilimiyle ilişkilidir. Kimyasal tepkimelerin gerçekleşmesini belirleyen faktörler termodinamik düzeyinde incelenir. Termodinamik olarak bir reaksiyon eğer tepkimenin ürünleri reaktanlara kıyasla daha düşük serbest enerji düzeyinde ise gerçekleşir. Diğer taraftan Reaktiflik ise genel olarak bir maddenin kimyasal değişikliklere ya da kimyasal tepkimelere girme eğilimine denir. Elementlerin atomik yapısı ve elektronlarının dizilişi elementlerin ve oluşturdukları moleküllerin reaktifliğinde önemli rol oynar. Soygazların örneğin kimyasal olarak çok az reaktiflik gösterdiği belirtilir. Dolayısıyla kimyasal bileşik oluşturmaları zordur. Bu durum soygazların tam dolu olan en dış elektron kabuğundan dolayıdır.
Kimyasal denge, asit ve baz kimyası, elektron aktarımı tepkimesi ve entropi gibi konular kimyasal reaktifliğin temel kavramlarıdır.
Brønsted–Lowry asit–baz teorisi, Johannes Nicolaus Brønsted ve Thomas Martin Lowry'nin birbirlerinden bağımsız oluşturdukları bir asit-baz tepkime kuramıdır. Kuramın temel kavramı asitlerin proton (H+ iyonu) veren maddeler, bazların ise proton alan maddeler olarak tanımlanmasıdır.
Asit-baz homeostazı insan homeostazının asitler ve bazlar arasındaki denge (pH) ile ilgilenen dalıdır. İnsan dokuları küçük pH değişikliklerine oldukça hassastır; bu nedenle pH'ı düzenleyen güçlü mekanizmalar vardır. Uygun pH aralığının dışındaki pH değerlerinde proteinler denatüre olur, enzimlerin çalışması durur ve kişi hayatını kaybedebilir.

Bikarbonat tampon sistemi kandaki, onikiparmak bağırsaktaki ve diğer dokulardaki uygun metabolik işlevleri desteklemek amacıyla pH'ı koruyan, karbonik asit, bikarbonat iyonu ve karbondioksitin dengesini içeren bir asit-baz homeostaz mekanizması. Karbondioksit, hızlıca ve sırasıya bikarbonat ve hidrojen iyonlarına ayrışacak olan karbonik asiti oluşturmak için, suyla tepkime verir.Bu tepkime karbonik anhidraz ile katalize edilir.Tepkime aşağıda gösterilmiştir:
Tampon çözelti zayıf asit ve konjuge bazın veya zayıf baz ve konjuge asitin karşımından oluşan sulu çözelti. Tampon çözeltiye küçük veya orta miktarda güçlü asit veya baz eklendiğinde pH değişimi çok az olur ve bu nedenle çözeltilerde pH değişimini engellemek için kullanılır. Çoğu canlı formu sadece küçük bir pH aralığında gelişir, bundan dolayı sabit pH'ı sürdürmek için tampon çözeltiyi kullanırlar. Doğada, bikarbonat tampon sistemi kandaki pH'ı düzenlemek için kullanılır.
Konjuge asit, Brønsted–Lowry asit–baz kuramında, bir bazın proton alışı (H+) ile oluşan tür.Konjuge baz ise asit proton verdikten sonra oluşan türdür.

İyodik asit, HIO3, beyaz veya kirli beyaz bir katı madde olarak elde edilebilir. Suda çok iyi çözünür, ancak klorik asit veya bromik asidin aksine saf halde bulunur. İyodik asit +5 oksidasyon durumunda iyot içerir ve halojenlerin saf halde en stabil okso-asitlerinden biridir. İyot asidi dikkatle ısıtıldığında pentoksit iyice dehidre olur. Daha sonraki ısıtmada, iyot pentoksit ayrıca iyot, oksijen ve düşük iyot oksitleri karışımı vererek ayrışır.
Kimya ve biyokimyada ayrışma, moleküllerin (veya tuzlar veya bileşikler gibi iyonik bileşiklerin) atomlar, iyonlar veya radikaller gibi daha küçük parçacıklara ayrıldığı genel bir süreçtir. Örneğin, bir asit suda çözündüğünde, bir elektronegatif atom ile bir hidrojen atomu arasındaki kovalent bir bağ, bir proton (H+) ve bir negatif iyon veren heterolitik fisyon tarafından kırılır. Ayrışma, birleşme veya rekombinasyonun tersidir.






