Sayı, sayma, ölçme ve etiketleme için kullanılan bir matematiksel nesnedir. En temel örnek, doğal sayılardır. Sayılar, sayı adı (numeral) ile dilde temsil edilebilir. Daha evrensel olarak, tekil sayılar rakam adı verilen sembollerle temsil edilebilir; örneğin, "5" beş sayısını temsil eden bir rakamdır. Yalnızca nispeten az sayıda sembolün ezberlenebilmesi nedeniyle, temel rakamlar genellikle bir rakam sisteminde organize edilir, bu da herhangi bir sayıyı temsil etmenin organize bir yoludur. En yaygın rakam sistemi Hint-Arap rakam sistemidir, bu sistem on temel sayısal sembol, yani rakam kullanılarak herhangi bir negatif olmayan tam sayının temsil edilmesine olanak tanır. Sayılar sayma ve ölçme dışında, etiketlerde, sıralamada ve kodlarda kullanılmak için de sıklıkla kullanılır. Yaygın kullanımda, bir rakam ile temsil ettiği sayı net bir şekilde ayrılmaz.

Doğal sayılar,  şeklinde sıralanan tam sayılardır ve kimi tanımlamalara göre 0 sayısı da bu kümeye dâhil edilebilir. Aralarında standart ISO 80000-2'nin de bulunduğu bazı tanımlar doğal sayıları 0 ile başlatır ve bu durum negatif olmayan tam sayılar için 0, 1, 2, 3, ... şeklinde bir karşılık bulurken, bazı tanımlamalar 1 ile başlamakta ve bu da pozitif tam sayılar için 1, 2, 3, ... şeklinde bir eşlenik oluşturur. Doğal sayıları sıfır olmadan ele alan metinlerde, sıfırın da dahil edildiği doğal sayılar bazen tam sayılar olarak adlandırılırken diğer bazı metinlerde bu terim, negatif tam sayılar da dahil olmak üzere tam sayılar için kullanılmaktadır. Özellikle ilkokul seviyesindeki eğitimde, doğal sayılar, negatif tam sayıları ve sıfırı dışlamak ve saymanın ayrık yapısını, gerçek sayıların bir karakteristiği olan ölçümün sürekliliğiyle karşıtlık oluşturmak amacıyla sayma sayıları olarak adlandırılabilir.
şeklinde sıralanan tam sayılardır ve kimi tanımlamalara göre 0 sayısı da bu kümeye dâhil edilebilir. Aralarında standart ISO 80000-2'nin de bulunduğu bazı tanımlar doğal sayıları 0 ile başlatır ve bu durum negatif olmayan tam sayılar için 0, 1, 2, 3, ... şeklinde bir karşılık bulurken, bazı tanımlamalar 1 ile başlamakta ve bu da pozitif tam sayılar için 1, 2, 3, ... şeklinde bir eşlenik oluşturur. Doğal sayıları sıfır olmadan ele alan metinlerde, sıfırın da dahil edildiği doğal sayılar bazen tam sayılar olarak adlandırılırken diğer bazı metinlerde bu terim, negatif tam sayılar da dahil olmak üzere tam sayılar için kullanılmaktadır. Özellikle ilkokul seviyesindeki eğitimde, doğal sayılar, negatif tam sayıları ve sıfırı dışlamak ve saymanın ayrık yapısını, gerçek sayıların bir karakteristiği olan ölçümün sürekliliğiyle karşıtlık oluşturmak amacıyla sayma sayıları olarak adlandırılabilir.

Element, aynı cins atomlardan oluşan ve kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere verilen isimdir.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.
Deoksiriboz veya bilinen adlarıyla D-Deoksiriboz ve 2-deoksiriboz, beş karbon atomu içeren ve aldehit grubu barındıran aldopentozların bir üyesidir. Deoksiriboz, penton riboz şekerinin 2 pozisyonundaki hidroksil grubunun hidrojen ile yer değiştirmesiyle oluşur, yani bu bir oksijen atomunun kaybı ile sonuçlanır. Hidroksil grubunun değişmesi aynı zamanda, halka yapısını C3'-endo pozisyonundan C2'-endo olacak şekilde değiştirir. Bu molekül, 1929 yılında Phoebus Levene tarafından keşfedilmiştir ve DNA nükleik asidinin önemli bir yapıtaşıdır.

Alkol, karbon atomuna doğrudan bir -OH (hidroksil) grubunun bağlı olduğu organik bileşiklere verilen genel ad. Genel formülü CnH2n+1OH olan mono alkoller, alkollerin önemli bir sınıfıdır. Bunlardan etanol (C2H5OH), alkollü içeceklerde bulunan türüdür. Genellikle alkol kelimesi ile etanol kastedilir ki yeni fermente olmuş birada etanol oranı %3-5 arasında iken şarapta %12-15 arasındadır.

Alkenler yapılarında en az bir tane karbon-karbon (C=C) çift bağı içeren organik bileşiklerdir. Alkenlerin yapısında karbon-karbon çift bağı bulunduğundan ve bu karbonların yapabileceği en fazla hidrojenle bağ yapmamış olduğundan alkenler doymamış bileşikler kategorisine girerler. Alkenlerin yapısında sadece bir karbon-karbon çift bağının bulunması durumunda homolog seriler oluşturur. Bu homolog serilerin genel formülü CnH2n şeklindedir. Burada n-in en az 2 olma şartı vardır. Aşağıda en basit alken olan eten, yaygın ismiyle etilenin, çeşitli modellemelerle çizilmiş şekillerinin yanı sıra alkenlerin çeşitli şekillerdeki yazılış şekilleri de bulunmaktadır.

Halka, matematikte cebirin temel yapılarından biridir ve soyut cebirde tam sayıların soyutlamasıdır. Bu yapıyı işleyen dala halka kuramı denir. Halkalar diğer bir temel yapı olan grupların üzerine inşa edilir. Her halka, aynı zamanda değişmeli bir gruptur, ama bir halkadan daha fazla özelliği sağlaması istenir. Örneğin halkada grup işlemine ek olarak ikinci bir işlem daha vardır. Halkalara örnek olarak tam sayılar, modülo n sayılar, polinomlar ya da karmaşık sayılar verilebilir.
Karbonil grubu karbon atomu ile oksijen atomunun çiftli bağ yapması ile oluşan fonksiyonel grup. sp2 hibritleşmesi yapmış ve oksijenle çift bağ oluşturmuş bir karbon atomu taşır. bu grubun geometrisini sp2 melezleşmesi yapmış olan karbon atomu belirler. Karbonil grubu sp2 karbonu dolayında düzlemseldir. Karbonla oksijen arasında bir sigma bağı, bir pi bağı vardır. Ayrıca oksijende iki ortaklanmamış elektron çifti bulunur.

Enerji seviyesi, atom çekirdeğinin etrafında katman katman biçiminde bulunan kısımların her biridir. Bu yörüngelerde elektronlar bulunur. Yörüngenin numarası; 1, 2, 3, 4, ... gibi sayı değerlerini alabilir. Yörünge numarasına baş kuantum sayısı da denir ve "n" ile gösterilir. Yörünge numarası ile yörüngenin çekirdeğe uzaklığı doğru orantılıdır.

Atom yarıçapı, küre şeklinde olduğu düşünülen atomların büyüklüklerini ölçmekte kullanılan bir niceliktir. Bu nicelik bir atomun çekirdeği ile elektron bulutu arasındaki uzaklığı ifade eder.

Dizi, bir sıralı listedir. Bir küme gibi, ögelerden oluşur. Sıralı ögelerin sayısına dizinin uzunluğu denir. Kümenin aksine sıralı ve aynı ögeler dizide farklı konumlarda birkaç kez bulunabilir. Tam olarak bir dizi, tanım kümesi sayılabilen toplam sıralı kümelerden oluşan bir fonksiyon olarak tanımlanabilir. Örneğin doğal sayılar gibi. Diziler bu örnekte olduğu gibi sonlu olabilir. Ya da tüm çift pozitif tam sayılar gibi sonsuz olabilir.

Dietil eter, (IUPAC adı etoksietan) kısaca eter olarak da bilinen (C2H5)2O formülüne sahip berrak, renksiz, uçucu, kolay yanan ve parlayabilen, oda sıcaklığında sıvı hâlde bir bileşiktir. Kaynama noktası düşük olup hoş, karakteristik bir kokusu vardır. Toksisitesi çok düşüktür. Eterler olarak bilinen kimyasal bileşik sınıfının en çok tanınan üyesidir. Bütanolün izomeridir. Yapısı bir oksijene iki etil grubunun bağlanması ile oluşur ve CH3-CH2-O-CH2-CH3 şeklindedir. Çözücü olarak çokça kullanılır.

Kısaca vinil eter olarak bilinen divinil eter, (CH=CH
2)
2O formülüne sahip doymamış, simetrik bir eterdir. Kaynama noktası düşük, yüksek uçuculuğa sahip ve aşırı yanıcı bu sıvı geçmişte narkoz araştırmalarının odağı olmuştur. Anestezik özellikleri diğer bir simetrik eter olan dietil etere benzer. Özellikle kısa süreli ameliyatlarda ve diş cerrahisinde kullanıldı.

Eterler, iki organik kısmın bir oksijen atomu üzerinden birbirine bağ yapmış organik moleküllerdir. Eterlerin genel formülü R-O-R' şeklindedir. Buradaki R ve R' aynı olabileceği gibi farklı organik kısımlar da olabilirler.

Vinil, (IUPAC ismi: Etenil) "CH2=CH-R" formülüne sahip bir tür fonksiyonel gruptur. Etilenin (CH2=CH2) bir Hidrojen (H) eksik hâli olarak tanımlanmaktadır. Bir vinil molekülü, bir hidrojen atomunun, başka bir organik moleküle bağlanmasıyla elde edilir. Aynı zamanda bu grup ile oluşmuş organik bileşiklerin adlandırılmasında "Vinil ..." şeklinde de kullanılabilir. Örneğin bir etilen molekülüne bağlı bir hidrojen atomu ayrılır, yerine Cl atomu bileşiğe dâhil olursa bu madde vinil klorür olarak adlandırılır.
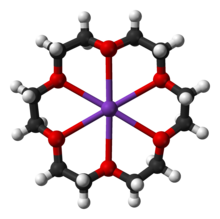
Ligand ya da ligant, merkezî bir metale bağlanan bir atom, iyon veya moleküldür. Bu bağ genelde bir veya birkaç elektron verilmesiyle oluşur, kovalent de olabilir iyonik de. Ayrıca, metal-ligand bağ değeri birden üçe kadar uzanabilir. Ligandlar genelde Lewis bazı(en) olarak sayılırlar ama ender olarak Lewis asidi ligandlar da olabilir.

Katı hal fiziğinde, bir katının elektron kuşak yapısı ; katıdaki bir elektronun sahip olabileceği enerji aralıkları ya da sahip olamayacağı enerji aralıkları olarak tanımlanır. Enerji bant teorisi bu bant ve bant boşluklarını atom veya moleküllerin büyük periyodik kafeslerindeki bir elektron için, izinli kuantum mekaniksel dalga fonksiyonlarını inceleyerek çıkarır. Bant teorisi katıların birçok fiziksel özelliklerini; örneğin elektriksel direnç ve optik soğurum gibi, açıklamak için başarılı bir biçimde kullanılmaktadır ve katı hal cihazları anlamanın temelini oluşturmaktadır.
Etilen oksit veya oksiran (C2H4O), hafifçe tatlı kokusu olan renksiz, zehirli ve yanıcı bir gazdır. Halkalı bir eter ve en basit epoksittir: bir oksijen atomu ve iki karbon atomundan oluşan üç üyeli bir halkadır. Gerilmiş bir halka olduğu için etilen oksit, halka açılmasıyla sonuçlanan bir dizi katılma reaksiyonlarına kolayca katılır.
Polieterler genellikle ana zincirlerinde eter bağları içeren polimerlerdir.