Kimyada, sülfür terimi -2 yükseltgenme seviyesinde kükürt içeren kimyasal bileşiklerin birkaç tipi için kullanılır.

Kükürt, simgesi S, atom numarası 16 olan, limon sarısında ametal, yalın katı bir elementtir.

Fotosentez, bitkiler ve diğer canlılar tarafından, ışık enerjisini organizmaların yaşamsal eylemlerine enerji sağlamak için daha sonra serbest bırakılabilecek kimyasal enerjiye dönüştürmek için kullanılan bir işlemdir. Bu kimyasal enerji, karbondioksit ve sudan sentezlenen şekerler gibi karbonhidrat moleküllerinde depolanır.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Bir ototrof, karbondioksit gibi basit maddelerden karbon kullanarak, genellikle ışıktan (fotosentez) veya inorganik kimyasal reaksiyonlardan (kemosentez) gelen enerjiyi kullanarak karmaşık organik bileşikler üreten bir organizmadır. Abiyotik bir enerji kaynağını organik bileşiklerde depolanan ve diğer organizmalar tarafından kullanılabilen enerjiye dönüştürürler. Ototroflar canlı bir karbon veya enerji kaynağına ihtiyaç duymazlar ve karadaki bitkiler veya sudaki algler gibi bir besin zincirindeki üreticilerdir. Ototroflar karbondioksiti indirgeyerek biyosentez için organik bileşikler ve depolanmış kimyasal yakıt yapabilirler. Çoğu ototrof indirgeyici madde olarak su kullanır, ancak bazıları hidrojen sülfür gibi diğer hidrojen bileşiklerini de kullanabilir.

Molibden, periyodik cetvelde atom numarası 42 ve simgesi Mo olan elementtir..

Kobalt kimyasal bir element'tir. Sembol'ü Co ve atom numarası 27'dir. Nikel gibi kobalt da, doğal meteorik demir alaşımlarında bulunan küçük birikintiler dışında, yer kabuğunda yalnızca kimyasal olarak birleşik formda bulunur. İndirgeyici eritme yoluyla üretilen serbest element sert, parlak, gümüş rengi bir metal'dir.

Proteobakteriler (Proteobacteria), bakteriler üstaleminin ana gruplarından birisini meydana getiren ve önemli cins ve türleri içeren şubesidir. Çeşitli hastalık etmenleri ve başka çok bilinen cinsler bu gruba dahildir. Ayrıca doğada serbest yaşayan türleri ve azot fiksasyonundan sorumlu pek çok bakteri türünü de içerir. Bu grup ribozomal RNA (rRNA) dizinlerine göre tanımlanmıştır. Bakteri biçimlerinin çeşitliliğinden dolayı grup, ismini Yunan mitolojisinde yer alan, her şekle girebilen tanrı Proteus'tan almıştır.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.

Sülfat iyonu, inorganik kimyada bir sülfür atomu ile bunu tetrahedral yapıda çevreleyen dört eş oksijen atomundan oluşan, negatif yüklü bir anyondur. Ampirik formülü SO42- ve moleküler ağırlığı 96,06 daltondur. Hidrojenle birleştiğinde sülfürik asit oluşturur. Ayrıca,Dimetil sülfat gibi organik sülfatlar, kovalent bileşiklerdir ve sülfürik asidin esterleridir.
- Sülfürik asitte metalin eritilmesi
- Sülfürik asidin bir metal hidroksit veya oksit ile reaksiyonu
- Metal sülfür veya sülfitlerin oksidasyonu

Kükürtlü asit, sülfüröz asit ya da sülfürik(IV) asit formüllü H2SO3 olan bir kimyasal bileşiktir.
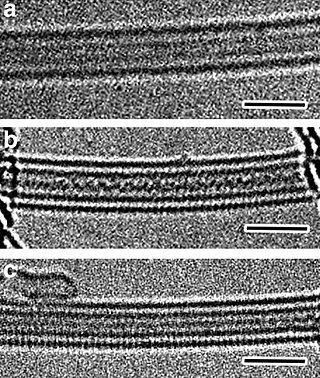
Polisülfürler kükürt atom zincirleri içeren bir sınıf kimyasal bileşiklerdir. Polisülfürler iki ana sınıfa ayrılır: anyonlar ve organik polisülfürler. Anyonlar S2−ngenel formülüne sahiptir. Bu anyonlar hidrojen polisülfürlerin H2Sn konjüge bazlarıdır. Organik polisülfürler genellikle RSnR formülüne sahiptir, burada R = alkil veya arildir.

Hidrojen iyodür (HI) iki atomlu bir molekül ve hidrojen halojenürdür. Sulu çözeltisi, güçlü bir asit olan hidroiyodik asit veya hidriyodik asit olarak bilinir. Bununla birlikte, hidrojen iyodür ve hidroiodik asit, birincisinin standart koşullar altında bir gaz olması, diğerinin ise söz konusu gazın sulu bir çözeltisi olması bakımından farklıdır. Birbirine dönüştürülebilir. HI, organik ve inorganik sentezlerde birincil iyot kaynaklarından biri ve bir indirgeyici madde olarak kullanılır.
Disülfür diklorür S
2Cl
2 formüllü kükürt ve Klor bileşiğidir.

Trioksidan, hidrojen trioksit veya dihidrojen trioksit olarak da adlandırılan, H[O]3H (H2O3 olarak da yazılır) kimyasal formülüne sahip bir inorganik bileşiktir. Kararsız hidrojen polioksitlerdendir. Sulu çözeltilerde, trioksidan su ve tekli oksijen oluşturmak için ayrışır:

Fototroflar (Yunanca: φῶς, φωτός = ışık, τροϕή = beslenme) karmaşık organik bileşikler (karbonhidratlar gibi) üretmek ve bundan enerji elde etmek için foton yakalayan organizmalardır. Hücresel çeşitli metabolik süreçleri gerçekleştirmek için ışıktan gelen enerjiyi kullanırlar. Fototrofların zorunlu olarak fotosentetik olduğu yaygın bir yanılgıdır. Hepsi olmasa da birçok fototrof sıklıkla fotosentez yapar: karbon dioksiti yapısal olarak, fonksiyonel olarak veya daha sonraki katabolik süreçler için bir kaynak olarak (örneğin nişasta, şeker ve yağ şeklinde) kullanılmak üzere anabolik olarak organik maddeye dönüştürürler. Tüm fototroflar, hücrenin moleküler enerji birimini(ATP) oluşturmak adına ATP sentaz tarafından kullanılan elektrokimyasal bir devinim oluşturmak için elektron taşıma sistemini veya doğrudan proton pompalamayı kullanır. Fototroflar, ototrof ya da heterotrof olabilir. Elektron ve hidrojenin kaynağı inorganik bileşikler ise (örn. Na2S2O3, bazı mor kükürt bakterilerinde olduğu gibi veya H2S, bazı yeşil kükürt bakterilerinde olduğu gibi) bunlara litotroflar da denebilir ve bu nedenle bazı fotoototroflara fotoliotoototroflar da denir. Fototrof organizmalarına örnekler: Rhodobacter capsulatus, Chromatium, Chlorobium vb.

Ultramarine, başlangıçta lapis lazuli 'nin bir toz halinde öğütülmesiyle elde edilen derin bir mavi renk pigment'idir. Adı Latin "ultramarinus" dan gelir, kelimenin tam anlamı "denizin ötesinde" demektir çünkü pigment Avrupa 'ya Afganistan'daki madenlerden İtalyan tüccarlar tarafından 14. ve 15. yüzyıllar'da ithal edilirdi.
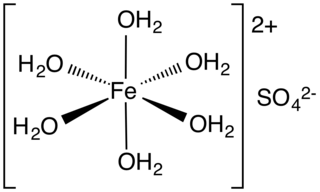
Demir (II) sülfat veya demir sülfat FeSO4•xH2O formülüne sahip bir dizi tuz anlamına gelir. Bu bileşikler en yaygın olarak heptahidrat (x = 7) olarak bulunursa da x için birkaç değer bilinmektedir. Hidratlı form tıp alanında demir eksikliğini tedavi etmek ve ayrıca endüstriyel uygulamalar için kullanılır. Antik çağlardan beri, Zaç-ı Kıbrıs ve yeşil vitriyol (vitriyol, sülfat için eski bir isimdir) olarak bilinen, mavi-yeşil heptahidrat (7 molekül su içeren hidrat) bu maddenin en yaygın şeklidir. Tüm demir (II) sülfatlar suda çözünerek oktahedral moleküler geometriye sahip ve paramanyetik olan aynı akua kompleksi [Fe(H2O)6]2+ verir.

VMS cevher yatakları olarak da bilinen volkanojenik masif sülfid cevher yatakları, denizaltı ortamlarında volkanik ilişkili hidrotermal olaylarla ilişkili ve bu olaylar tarafından oluşturulan, başta bakır - çinko olmak üzere bir tür metal sülfit cevher yatağıdır.




















