
Uranyum, radyoaktif bir kimyasal elementtir. Simgesi "U"dur. 1789 yılında Martin Heinrich Klaaproth tarafından keşfedilmiş ve 1841 yılında Eugene-Melchior Peligot tarafından izole edilmiştir. Uranyum ilk zamanda radyoaktivite ile ilgili fazla bilgi sahibi olunmadığından diğer elementler gibi zannedilse de, 1896 yılında bilim tarihinin önemli isimlerinden olan Dimitri Mendeleyev’in çalışmalarıyla radyoaktif bir element olduğu ispatlanmıştır.
Ametal, metal özelliği göstermeyen elementlerdir. Isıyı ve elektrik akımını iletmek gibi metallere özgü özellikleri göstermezler. Ayrıca kendi aralarındaki ortak özellikleri yok denecek kadar azdır. Genellikle karbon, azot, fosfor, oksijen, kükürt, selenyum, flor, klor, brom, iyot ve soy gaz elementlerine ametal denir.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.
CAS kayıt numaraları kimyasal bileşikler, polimerler, biyolojik dizinler, karışımlar ve alaşımlar için kullanılan tek tanımlayıcı (unique) sayılardır. CAS numarası olarak da bilinirler.
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.

Molekül, birbirine bağlı gruplar halindeki atomların oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır. Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farklı sayılarda farklı atomların bağlanması sonucunda oluşabilirler. Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve 2 oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 1996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen. Molekülleri oluşturan kimyasal bağlara Moleküler bağlar denir. Bunlar kovalent, iyonik ve metalik bağlardır.

Çamaşır suyu, genellikle etken madde olarak sodyum hipoklorit (NaClO) içeren ağartma, temizlik ve hijyen amacıyla kullanılan kimyasal maddedir.

İyonik bağ, zıt yüklü iyonlar arasındaki elektrostatik kuvvetlere dayanan bir kimyasal bağ türüdür.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.
Kimyasal formül, bir kimyasal birleşiği oluşturan atomlar hakkında detaylı ve açık bilgi veren bir yöntemdir. Moleküler bileşikler için, içindeki elementleri kimyasal sembolleriyle, o elementlerin sayısını da o atomun yanındaki sayılarla belirtirler. Eğer bir molekül, birden çok atom içeriyorsa, bu atomların nicelikleri, yanlarında altyazı olarak belirtilir. İyonik bileşikler ve moleküler olmayan maddeler içinse, atomların girdiği oranlar, bu altyazılarla belirtilir.
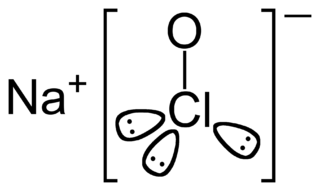
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.

Potasyum klorür kimyasal bir bileşiktir. KCl formülü ile gösterilir. Potasyum ve klor elementlerinin birleşmesi ile oluşur. Saf hali, kokusuzdur. Beyaz kristallerden oluşur. Bu kristallerde yüzey merkezli küp şeklinde istiflenerek dizilirler.

Klorat, ClO3− formülüyle gösterilen bir kimyasal kök. Bileşiklerinde daima bir adet elektron alır. Kloratlar, genel olarak klorik asitin tuzu olarak bilinirler. Klorat molekülleri organik bileşikleri kolayca oksitleyeceğinden dolayı kimyasal olarak zararlı bir maddedir. Geçmişte birçok patlayıcı ve havai fişekte kullanılan klorat, günümüzde yerini perklorata bırakmıştır.

Fritz Haber Alman kimyager. 1918 yılında Nobel Kimya Ödülü'nü kazanmıştır. I. Dünya Savaşı süresince klor ve diğer zehirli gazları geliştirme ve dağıtımı konusundaki çalışmaları nedeniyle "kimyasal savaşın babası" olarak da tanımlanır.

Sodyum klorit (NaClO2) kâğıt üretiminde ve dezenfektan olarak kullanılan kimyasal bir bileşiktir.

Azot triklorür, trikloramin olarak da bilinen formülü NCl3 olan kimyasal bileşik. Sarı, yağımsı, keskin kokulu bir sıvıdır. En sık amonyak türevleri ve klor arasındaki kimyasal reaksiyon sonrası oluşmaktadır, yüzme havuzlarındaki oluşumu buna bir örnektir.

2017 İdlib kimyasal saldırısı veya Han Şeyhun kimyasal saldırısı, 4 Nisan 2017 tarihinde Suriye İç Savaşı sırasında İdlib'in Han Şeyhun beldesinde düzenlen kimyasal saldırı. İdlib Sağlık Otoritesi, sarin veya benzeri bir maddeyi içeren zehirli gazın salınımı sonucu en az 74 kişinin öldüğünü ve 557'den fazla kişinin yaralandığını açıkladı.

İyot monoklorür ICl formülü ile gösterilen bir interhalojen bileşiktir. Oda sıcaklığına yakın eriyen kırmızı-kahverengi renge sahip bir kimyasal bileşiktir. İyot ve klorun elektronegatifliği arasındaki fark nedeniyle, ICl oldukça kutupsaldır ve I+ kaynağı olarak davranır.

Organoklorürler, klorlu hidrokarbonlar ya da klorokarbonlar, en az bir adet kovalent bağlanmış klor atomuna sahip organik bileşiklerdir. En basit örnekleri kloroalkanlardır. Organoklorürlerin geniş bir yapısal çeşitliliğe sahip olması onların farklı kimyasal özelliklere, isimlere ve kullanım alanlarına sahip olmasına sebep olmuştur. Bazı organoklorürlerin yararlı olmasına karşın bazıları zehirli ve çevreye zararlıdır.
2007'de Irak'ta temiz içme suyu eksikliği kolera salgınına yol açtı. Toplamda yaklaşık 7.000 kişi enfekte oldu ve 10 ölüm bildirildi.















