Somatik hipermutasyon
Somatik hipermutasyon veya SHM, edinilmiş bağışıklık sisteminin bir parçası olarak, sistemin yabancı cisimlere (örn. mikroplara) karşı durmasında görev alan hücre içi bir mekanizmadır. İlginlik olgunlaşmasının ana bileşenlerinden biridir.
SHM, bağışıklık sisteminin, yabancı yapıları (antijenleri) tanımakta kullandığı almaç gruplarını çeşitlendirir ve bağışıklık sisteminin canlının yaşamı süresince karşılaştığı yeni tehditlere karşı uyum sağlamasını sağlar[1]
Somatik hipermutasyon immunoglobulin genlerinin çeşitli bölgelerini etkileyen programlanmış bir mutasyon sürecini kapsamaktadır. Mutasyonların diğer çeşitlerinden farklı olarak, SHM sadece yaşayan bağışıklık hücrelerini etkiler ve bu mutasyonlar yavrulara aktarılmaz[2] Yanlış hedeflenmiş somatik hipermutasyon B-hücreleri, lenfomalarının gelişiminden sorumlu mekanizma olabileceği nedeniyle günümüzde araştırılmaktadır.[3]
Hedeflenme
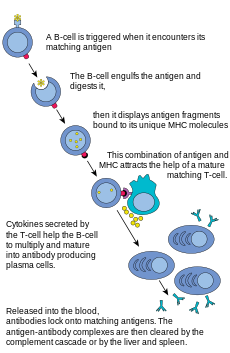
Bir B hücresi bir antijeni tanıdığında, bölünmek ya da çoğalmak için uyarılmış olur. Çoğalma sırasında, B hücresi reseptörü lokusu son derece yüksek somatik mutasyon oranı gösterir ki; bu genom çapındaki mutasyonların normal oranından en az 105-106 kat daha büyüktür.[2] Meydana gelen mutasyonlar, baçlıca tek baz yerine geçmeler (subsitüsyonlar) şeklindedir, eklemeler (insersiyonlar) ve kayıplar (delesyonlar) daha ender olur. Bu mutasyonlar en çok, çok-değişebilen (hypervariable) bölgeler olarak da bilinen, DNA'nın "sıcak-noktalar"ında meydana gelirler. Yönlendirilen bu hipermutasyon, özgül bir yabancı antijeni tanıyabilme ve ona bağlanabilme yeteneğine sahip olan immünoglobülin reseptörlerini ifade eden B hücrelerinin seçilimi için olanak sağlar. Bu bölgeler, "tamamlayıcı karar-bölgeleri"ne benzerler, immünoglobulindeki antijen tanıma bölgeleriyle ilişkilidirler.[4]
Bu hedeflenmenin kesin doğasının ne yazık ki çok az anlaşılmış olmasına rağmen, bunun, hata-eğilimli ve yüksek-doğruluklu onarımların dengesi ile kontrol edildiği düşünülmektedir.[5] Bu yönlendirilmiş hipermutasyon, özgül bir yabancı antijeni arttırılmış şekilde tanıma ve bağlama yetisine sahip olan immunoglobulin reseptörlerini ifade eden B hücrelerinin seçilimini olanak sağlar.[1]
İşleyiş


Deneysel bulgular, SHM mekanizmasının, DNA'daki sitozinin urasile deaminasyonunu sağlayan aktivasyonu-teşvikleyen (sitidin) deaminaz (İngilizce Activation-Induced (Cytidine) Deaminase veya AID) olarak adlandırılan bir enzim tarafından yapıldığı görüşünü desteklemektedir.[6][7] Bir sitozin-guanin çifti bu yüzden, doğrudan bir urasil-guanin yanlış eşleşmesine değiştirilmiş olur. Urasil kalıntıları normalde DNA'da bulunmaz, bu nedenle genom bütünlüğünü sağlamak için, bu mutasyonların birçoğu yüksek-doğruluklu DNA yanlış-eşleşim-onarım enzimleriyle düzeltilmelidir. Urasil bazları, onarım enzimi urasil-DNA glikolilaz tarafından çıkarılır.[7] Hata-eğilimli DNA polimerazlar bundan sonra, boşluğu doldurmak ve mutasyonlar yaratmak için seferber edilebilir.[6][8]
Bu yeni DNA sentezi, ya deaminlenmiş sitozininin kendinde ya da bitişiğindeki baz çiftlerinde sıklıkla oluşan mutasyonları ortaya çıkaran, hata eğilimli DNA polimerazları içerir. B hücresi bölünmesi sırasında, DNA'nın immünoglobulin değişebilir bölgesi, okunur ve çevirilir. B hücrelerinin hızla çoğalan popülasyonlarındaki mutasyonların ortaya çıkması, nihai olarak, hafifçe farklılık gösteren reseptörler ve antijen için çeşitlenmiş özgüllüğe sahip olan binlerce B hücresinin üretimine yol açar, bunların arasından antijen için en büyük yatkınlığı gösteren B hücresinden seçilir. En yüksek afiniteyi gösteren B hücreleri, bundan sonra, tekrar bir enfeksiyon durumunda arttırılmış bağışıklık yanıtının verilmesine katkıda bulunan uzun-yaşamlı hafıza B hücrelerine ve antikor üreten plazma hücrelerine farklılaşmak üzere seçilirler.[2]
Hipermutasyon süreci ayrıca, bir canlının kendi hücrelerinin imzası karşısında "kendini-seçen" hücrelerden yararlanır. Bu oto-seçim sürecindeki hatalarının, bir öz-bağışıklık yanıtının gelişmesine neden olduğu da hipotez olarak ileri sürülmüştür.
Ayrıca bakınız
- İlginlik olgunlaşması
- Anerji
- Bağışıklık sistemi
- V(D)J rekombinasyonu
Kaynakça
- ^ a b Janeway, C.A., Travers, P., Walport, M., Shlomchik, M.J. (2005). Immunobiology (6.6yayıncı=Garland Science bas.). ISBN 0815341016.
- ^ a b c Oprea, M. (1999) Antibody Repertoires and Pathogen Recognition: 6 Eylül 2008 tarihinde Wayback Machine sitesinde arşivlendi. The Role of Germline Diversity and Somatic Hypermutation (Thesis) University of Leeds.
- ^ Odegard V.H., Schatz D.G. (2006). "Targeting of somatic hypermutation". Nat. Rev. Immunol. 6 (8). ss. 573-583. doi:10.1038/nri1896. PMID 16868548.
|başlık=dış bağlantı (yardım) - ^ Li, Z., Wool, C.J., Iglesias-Ussel, M.D., Ronai, D., and Scharff, M.D. (2004). "The generation of antibody diversity through somatic hypermutation and class switch recombination". Genes & Development. 18 (1). ss. 1-11. doi:10.1101/gad.1161904. PMID 14724175.
|başlık=dış bağlantı (yardım) - ^ Liu, M., Schatz, D.G. (2009). "Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology". Cilt 30. ss. 173-181.
|başlık=dış bağlantı (yardım) - ^ a b Teng, G. and Papavasiliou, F.N. (2007). "Immunoglobulin Somatic Hypermutation". Annu. Rev. Genet. Cilt 41. ss. 107-120. doi:10.1146/annurev.genet.41.110306.130340. PMID 17576170.
|başlık=dış bağlantı (yardım) - ^ a b Larson, E.D. and Maizels, N. (2004). "Transcription-coupled mutagenesis by the DNA deaminase AID". Genome Biology. 5 (3). s. 211. doi:10.1186/gb-2004-5-3-211. PMC 395756 $2. PMID 15003109.
|başlık=dış bağlantı (yardım) - ^ Bachl, J., Ertongur, I., Jungnickel, B. (2006). "Involvement of Rad18 in somatic hypermutation". Proc. Natl. Acad. Sci. USA. Cilt 103. ss. 12081-86.
|başlık=dış bağlantı (yardım)
Dış bağlantılar
- http://www.nlm.nih.gov/cgi/mesh/2011/MB_cgi?mode=&term=Immunoglobulin+somatic+hypermutation11 Mart 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- İmmünogenetik ders sunumu-Dr.C.Dundar