Alkali metaller periyodik tablonun birinci grubunda yer alan metallerdir. Fransiyum dışında hepsi, yumuşak yapıda ve parlak görünümdedir.

Su, Dünya üzerinde bol miktarda bulunan ve tüm canlıların yaşaması için vazgeçilmez olan, kokusuz ve tatsız bir kimyasal bileşiktir. Sıklıkla renksiz olarak tanımlanmasına rağmen kızıl dalga boylarında ışığı hafifçe emmesi nedeniyle mavi bir renge sahiptir.

Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Brom (Br), Antoine Balard tarafından 1826 yılında keşfedilen halojen ametal. Yunanca dışkı gibi koku anlamındaki bromosdan gelmiştir.

Erime noktası, kristal ve saf olan bir maddenin katı halden sıvı hale geçtiği belirli bir sıcaklıktır. Bu sıcaklığa o maddenin erime noktası denir. Bütün kristal yapıya sahip saf maddelerin erime noktasında, yani katı halden sıvı hale geçene kadar, sıcaklığı sabit kalır. Ancak tamamen sıvı hale geçtikten sonra sıcaklığı yükselir. Saf kristal cisimlerin erime noktası ile donma noktası arasında sıcaklık farkı yoktur. Mesela saf su, 0 °C de donar. Fakat saf olmayan maddelerin, yani karışımların donma ve erime noktaları farklıdır.

Güney Okyanusu ya da Antarktika Okyanusu, bazı coğrafya ve çoğu hidrografi kaynaklarına göre Antarktika kıtasını çevreleyen su kütlesidir. Bu okyanus, dünyanın dördüncü büyük ve en son tanımlanmış okyanusudur.

Sıvı, maddenin ana hâllerinden biridir. Sıvılar, belli bir şekli olmayan maddelerdir; içine konuldukları kabın şeklini alır, akışkandırlar. Sıvı molekülleri, sıvı hacmi içinde serbest hareket ederler, fakat partiküllerin ortak çekim kabiliyeti, hacmin izin verdiği ölçüdedir. Sıvılar sıkıştırılamaz.

Stearik asit, CH3(CH2)16COOH formülüyle gösterilen doymuş bir yağ asididir. Çoğu hayvan ve bitkiden elde edilen katı-sıvı yağlarda, ekseriya gliserid stearin şeklinde bulunur.

Çözelti ya da solüsyon, iki ya da daha fazla maddenin herhangi bir oranda bir araya gelerek oluşturdukları homojen karışımdır.

Atlas Okyanusu veya Atlantik Okyanusu, 106.460.000 km2 yüzölçümü ile Dünya'nın en büyük ikinci okyanusudur. Dünya yüzeyinin yaklaşık %20'sini ve Dünya'nın su yüzeyinin yaklaşık %29'unu kaplar. Bir zamanlar tek parça olan ana kıtanın bölünmesiyle oluşmuştur. Avrupa ve Afrika'yı Amerika kıtalarını ayırır. Avrupalı bakış açısıyla "Eski Dünya"yı "Yeni Dünya"dan ayırdığı kabul edilir.
Klorür, nötr hâldeki klor atomunun, bir elektron alarak iyon (anyon) hâline geçtiğinde aldığı isim. Cl− olarak gösterilir. Klorür iyonu içeren maddelere de verilen bir isimdir. Bir iyon olduğundan dolayı, kendi başına doğada yer almaz; ancak bir çözeltide karşı iyonu ile yer alabilir.
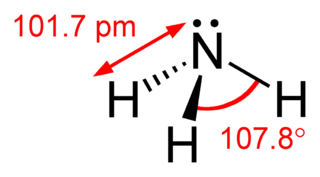
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir. OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.

Atomik kütle birimi (sembolü akb) veya dalton (sembolü Da), çok ufak kütleli maddelerin, özellikle atom ve moleküllerin kütlelerini hesaplamak için kullanılan ölçü birimidir. Bir karbon12 (C12) atomunun kütlesinin tam olarak 1/12'sine eşittir. Bunun sebebi, karbonun en kararlı ve en kolay bulunabilen elementlerden biri olmasıdır.

Deniz suyu, denizlerde ve okyanuslarda bulunan su. Dünyadaki bütün okyanuslardaki ortalama tuzluluk yaklaşık %3.5'tur. Bu oran, her bir kilogram (ya da litre) deniz suyuda yaklaşık 35 gram çözünmüş tuz (çoğunluğu sodyum klorür iyonları olan Na+ ve Cl-) içeriğini belirtir. Deniz suyunun ortalama yoğunluğu su yüzeyinde 1.025 g/ml (1025 kg/m³)'dir. İçeriğindeki tuz taneciklerinin kütlesinden dolayı deniz suyunun yoğunluğu tatlı/saf suyun yoğunluğundan fazladır; (4oC sıcaklıkta 1.000 g/ml). Deniz suyunun donma noktası tuzluluktaki artışla orantılı düşer; %3.5 tuzluluk derecesinde yaklaşık -2oC'dir.
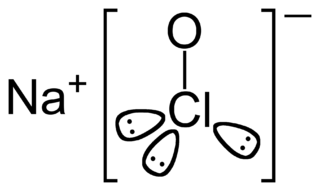
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.
Kaynama, sıvının buhar basıncının dış basınca eşit olduğunda, sıvının her yerinden gaz kabarcıklarının çıkması. Saf maddelerin sabit atmosfer basıncı altında kaynama noktası sabittir. Kaynama süresi boyunca maddenin sıcaklığı değişmez. Sıvı bir maddenin içine uçucu olmayan bir çözünen eklenirse çözeltinin kaynama noktası yükselir. Çözünen madde miktarı arttıkça kaynama noktası yükselecektir. Aynı ortamdaki bütün sıvıların kaynama anındaki buhar basınçları eşittir, ancak maddelerin kaynama sıcaklığı maddenin cinsine, saflığına ve ortamın dış basıncına bağlıdır. Kaynama sıcaklığı maddeler için ayırt edici bir özelliktir.

Sodyum bikarbonat ya da soda kimyasal formülü NaHCO3 olan bir kimyasal bileşiktir. Kabartma tozu olarak da bilinir. Sodyum tuzlarından birisidir. Antiasit özelliği vardır. Kabartma tozu olarak da kullanılır. Suda çözünür. Beyaz katı kristal tozdur. Sodyum karbonat'ı andıran hafif alkali tadı vardır. Salin solüsyonu bileşiminde de kullanılır.

Potasyum perklorat formülü KClO4 olan bir kimyasal bileşiktir. Diğer perkloratlar gibi, bu tuz da güçlü bir oksitleyici olup potansiyel olarak birçok organik maddeyle reaksiyona girer. Havai fişek, mühimmat kapsülleri ve primer patlayıcılarda yaygın bir oksitleyici olarak kullanılan katı ve renksiz kristallerden oluşan bu madde çeşitli şekilde itici yakıtlar, flaş bileşimleri, yıldızlar ve maytaplarda da kullanılmaktadır. Daha yüksek performanslı amonyum perklorat yerine çoğu kez ikame edilerek katı yakıtlı roket itici yakıtı olarak da kullanılmıştır. KClO4 alkali metal perkloratlar içerisinde en düşük çözünürlüğe sahiptir (25 °C'deki 100 ml. suda 1.5 gr.).

Sodyum klorür, yaygın olarak 'tuz' ismiyle bilinen kimyasal formülü NaCl; 1/1 oranında sodyum ve klorür iyonları olan iyonik bileşik. Molar kütleleri sırasıyla 22.99 ve 35.45 g/moldur. 100 g NaCl, 39.34 g Na ve 60.66 g Cl içerir. Sodyum klorür, deniz suyunun tuzluluğundan ve birçok çok hücreli organizmanın hücre dışı sıvısından en çok sorumlu olan tuzdur. Yenilebilir sofra tuzu biçiminde yaygın olarak bir çeşni ve gıda koruyucusu olarak kullanılır. Birçok endüstriyel proseste büyük miktarlarda sodyum klorür kullanılır ve daha ileri kimyasal sentezler için hammadde olarak kullanılan sodyum ve klor bileşiklerinin ana kaynağıdır. Sodyum klorürün ikinci bir ana uygulaması donma sıcaklığı altındaki havalarda yolların buzunun çözülmesidir.

















