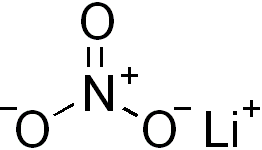
Sodyum nitrat
 | |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Sodyum nitrat | |||
Diğer adlar Şili güherçilesi Nitratin Peru güherçilesi | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.686 | ||
| EC Numarası |
| ||
| E numaraları | E251 (koruyucular) | ||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
| UN numarası | 1498 | ||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Molekül formülü | NaNO3 | ||
| Molekül kütlesi | 84,9947 gr/mol | ||
| Görünüm | Beyaz toz ya da renksiz kristaller | ||
| Koku | tatlı | ||
| Yoğunluk | 2,257 gr/cm3, katı | ||
| Erime noktası | 308 °C (586 °F; 581 K) | ||
| Kaynama noktası | 380 °C (716 °F; 653 K) bozunur | ||
| Çözünürlük (su içinde) | 73 gr/100 mL su (0 °C) 91,2 gr/100 mL su (25 °C)[1][2] 180 gr/100 mL su (100 °C) | ||
| Çözünürlük | amonyak, hidrazinde çok çözünür alkolde çözünür piridinde çok az çözünür asetonda çözünmez | ||
| −25,6·10−6 cm3/mol | |||
| Kırınım dizimi (nD) | 1,587 (trigonal) 1,336 (rombohedral) | ||
| Akmazlık | 2,85 cP (317 °C) | ||
| Yapı | |||
| trigonal ve rombohedral | |||
| Termokimya | |||
Isı sığası (C) | 93,05 J/mol K | ||
Standart molar entropi (S⦵298) | 116 J•mol−1•K−1[3] | ||
Standart formasyon entalpisi (ΔfH⦵298) | −467 kJ•mol−1[3] | ||
Gibbs serbest enerjisi (ΔfG⦵) | -365,9 kJ/mol | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Zararlı (Xn) Oksitleyici (O) | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |   | ||
| Tehlike ifadeleri | H272, H319 | ||
| Önlem ifadeleri | P220, P305+P351+P338 | ||
| NFPA 704 (yangın karosu) | |||
| Parlama noktası | Yanıcı değildir | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 3236 mg/kg | ||
| AB sınıflandırması | Hazchem O | ||
| Güvenlik bilgi formu (SDS) | ICSC 0185 | ||
| Benzeyen bileşikler | |||
Diğer anyonlar | Sodyum nitrit | ||
Diğer katyonlar | Lityum nitrat Potasyum nitrat Rubidyum nitrat Sezyum nitrat | ||
Benzeyen bileşikler | Sodyum sülfat Sodyum klorür | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||

Sodyum nitrat formülü NaNO3 olan kimyasal bileşiktir. Güherçile'den ayırmak için Şili güherçilesi (bu ülkede büyük miktarda yığınlar halinde bulunması nedeniyle bu ad verilmiştir) adı da verilen bu beyaz renkli kristal tuz, potasyum nitrata oranla suda çok fazla çözünmektedir. Havadan nem çeker.
Sodyum nitrat gıda katkısı ve gübrelerde, piroteknik malzeme olarak, sis bombasının içeriğinde, katı roket itici yakıtı olarak kullanıldığı gibi, cam ve seramik sektöründe de kullanılır. Bileşik bu amaçlar için kullanılmak için Şili’de bulunan geniş güherçile yataklarından çok miktarda çıkarılmaktadır.
Tarihçe
Şili güherçilesinin Avrupa’ya ilk sevkiyatı 1820 ya da 1825 yılında İngiltere’ye gerçekleşse de herhangi bir alıcı bulunamadığından dolayı gümrük ücretini ödememek için denize döküldü.[4][5] Ancak zamanla, Güney Amerika güherçile madenciliği karlı bir iş haline geldi (1859 yılında, sadece İngiltere 47,000 metrik ton tüketti[5]). Şili, Pasifik Savaşında Peru ve Bolivya müttefik kuvvetlerine karşı savaştı ve bütün zengin maden yataklarını aldı. 1919 yılında, Ralph Walter Graystone Wyckoff X ışını kristalografisini kullanarak sodyum nitratın kristal yapısını belirledi.
Oluşumu
Doğal olarak oluşan sodyum nitratın en büyük birikimleri, nitrat tuzlarının kaliş cevheri adı verilen tuz yataklarına bağlandığı Şili ve Peru'da bulunur.[6] Nitratlar, denizden gelen sis yağışı ve deniz serpintisinin yükseltgenip kurumasıyla ve ardından havada taşınan NaNO3, KNO3, NaCl, Na2SO4 ve I’un yerçekimine uyarak kuru çöl atmosferinde karada çökmesi sonucu birikirler.[7] El Niño/La Niña aşırı kuraklık / şiddetli yağmur döngüleri, hem kuraklık hem de su çözeltisi / yeniden taşınma / yamaçlara ve havzalara taşınması yoluyla nitrat birikimini destekler; kılcal çözelti hareketi nitrat katmanları oluşturur; saf nitrat nadir damarlar oluşturur. 20. yüzyılın dönümünde, Alman kimyagerler Fritz Haber ve Carl Bosch, endüstriyel ölçekte atmosferden amonyak üretmek için bir süreç (bkz. Haber işlemi) geliştirene kadar, bileşiğin dünya arzı yüzyılı aşkın bir süre boyunca neredeyse tamamen Kuzey Şili‘deki Atacama Çölünden karşılandı. I. Dünya Savaşı'nın başlamasıyla Almanya, Amonyak'ı bu süreç yardımıyla barut ve diğer mühimmat üretiminde doğal bileşik kadar pratik olan, sentetik Şili güherçilesine dönüştürmeye başladı. 1940'lara gelindiğinde, bu dönüşüm süreci doğal kaynaklardan tedarik edilen sodyum nitrat talebinde çarpıcı bir düşüşe neden oldu.
Şili, Pedro de Valdivia, María Elena ve Pampa Blanca gibi yerlerdeki aktif maden ocaklarıyla hâlâ en büyük kaliş rezervine sahiptir. Oralarda eskiden kaliş madenine beyaz altın adı veriliyordu.[8][9] Sodyum nitrat, potasyum nitrat, sodyum sülfat ve iyot kalişin işlenmesi ile elde edilir. Humberstone ve Santa Laura’nın eski Şili güherçilesi madenleri halkının yaşadığı yerler 2005 yılında Unesco Dünya Mirası alanları olarak ilan edildi.
Sentezi
Sodyum nitrat, ayrıca nitrik asitin sodyum karbonat veya sodyum bikarbonat ile nötürleştirilmesiyle:
- 2 HNO3 + Na2CO3 → 2 NaNO3 + H2O + CO2
- HNO3 + NaHCO3 → NaNO3 + H2O + CO2
veya, ayrıca sodyum hidroksit ile nötralize ederek (ancak bu reaksiyon çok ekzotermiktir):
- HNO3 + NaOH → NaNO3 + H2O
veyahut stokiyometrik miktarlarda amonyum nitrat ve sodyum hidroksit, sodyum bikarbonat ya da sodyum karbonat karıştırılarak endüstiyel olarak sentezlenir:
- NH4NO3 + NaOH → NaNO3 + NH4OH
- NH4NO3 + NaHCO3 → NaNO3 + NH4HCO3
- 2NH4NO3 + Na2CO3 → 2NaNO3 + (NH4)2CO3
Kullanımı
Sodyum nitrat, damıtma yoluyla, nitrik asit üretmek için sülfürik asit ile birleştirilebilir. Daha az ayrışma için ihtiyaç duyulan düşük sıcaklık, damıtmada daha düşük basınç uygulanarak sağlanır. 1 mol sülfürik asit başına teorik olarak 2 mol nitrik asit verimi, çok yüksek bir reaksiyon bitiş sıcaklığı, fazla bozunma ve uzaklaştırılması zor bir katı nötr sülfat eldesi ile sonuçlanır. Bu reaksiyon endüstriyel olarak önemli olduğundan, imbikten erimiş halde dökülen çoğunlukla bisülfat ürünü üzerinde aşırı sülfürik asit ile çalışmak yaygın bir uygulamadır.
Amatör altın arıtıcıları, altın ve diğer metalleri çözen hibrit bir kral suyu yapmak için sodyum nitrat kullanır.
Daha az yaygın olan uygulamalar arasında havai fişeklerde oksitleyici, karabarutta yaygın olarak kullanılan potasyum nitratın yerine ve ani soğuk paketlerde bileşen olarak bulunur.[10]
Sodyum nitrat, ısı depolama ve daha yakın zamanda güneş enerjisi santrallerinde ısı aktarımı için potasyum nitrat ve kalsiyum nitrat ile birlikte kullanılır. Andasol Güneş Enerjili Elektrik Santrali ve Arşimet projesi gibi prototip tesislerde enerji depolama malzemesi olarak sodyum nitrat, kalsiyum nitrat ve potasyum nitrat karışımı kullanılır.
Atık su endüstrisinde fakültatif mikroorganizma solunumu için de kullanılır. Bir mikroorganizma cinsi olan Nitrosomonas, oksijen yerine nitrat tüketerek arıtılacak atık suda daha hızlı büyümesini sağlar.
Sodyum nitrat bazen karbon dozajlama tekniklerini kullanan deniz akvaryumcuları tarafından da kullanılır. Sudaki nitrat seviyelerini artırmak ve bakteri üremesini teşvik etmek için kullanılır.
Gıda
Sodyum nitrat ayrıca tütsülenmiş et ve kümes hayvanlarında koruyucu ve renk sabitleyici olarak kullanılan bir gıda katkısıdır; INS numarası 251 veya E numarası E251 olarak listelenmiştir. Kullanımı için AB,[11] ABD[12] ile Avustralya ve Yeni Zelanda’da[13] onay almıştır. Sodyum nitrat, örneğin salam gibi yemeye hazır şarküteri etlerinde kullanılan yaygın bir gıda katkı maddesi ve koruyucu olan sodyum nitrit ile karıştırılmamalıdır.
Sağlık sorunları
Çalışmalar, nitrat seviyelerinin artması ve Alzheimer hastalığı, şeker hastalığı, mide kanseri ve Parkinson hastalığı da dahil olmak üzere belirli hastalıklardan kaynaklanan ölümlerin artması arasında bir bağlantı olduğunu göstermiştir: ancak nitrozaminlerin DNA üzerindeki olası zararlı etkisi sayesinde, epidemiyolojik sonuçlardaki diğer olası nedenleri kontrol etmek için çok az şey yapılır.[14] Sodyum nitrat ve nitrit içeren tütsülenmiş etlerde oluşan nitrozaminler, mide kanseri ve yemek borusu kanserine bağlanmıştır.[15] Sodyum nitrat ve nitrit daha yüksek olarak kalın bağırsak kanseri riski ile ilişkilidir.[16]
İşlenmiş etin kolon kanseri riskini artırmasının nedenlerinden biri, nitrat içeriğidir. Koruyucu olarak ete ilave edilen az miktarda nitrat, ilave edilebilecek herhangi bir nitrite ek olarak nitrite dönüşür. Nitrit daha sonra kanserojen NOCs (nitrozo bileşikleri) üretmek için protein açısından zengin gıdalarla (et gibi) reaksiyona girer. Nitrozo bileşikleri, et tütsülendirildiğinde veya et sindirildikçe vücutta oluşturulabilir.[17]
Ancak bazı şeyler, "gıdadaki nitratların kanser riskinizi artırdığı" önermesini bozar. İşlenmiş etlerde lif, vitamin veya fitokimyasal antioksidanlar bulunmaz, sodyum oranı yüksektir, yüksek yağ içerebilir ve genellikle proteini nitrozaminlere indirgemeye yetecek bir sıcaklıkta kızartılır veya pişirilir. Nitratlar, tüm memelilerin hayatta kalması için gerekli olan birincil damar sistemi sinyallemesinde anahtar ara maddeler ve efektörlerdir.[18]
Ayrıca bakınız
- Pasifik Savaşı (1879-1884), "Güherçile Savaşı" olarak da bilinir.
Kaynakça
- ^ Haynes, William M. (22 Haziran 2016). CRC Handbook of Chemistry and Physics. CRC Press. ISBN 978-1-4987-5429-3.
- ^ "Sodium nitrate". PubChem. 21 Mayıs 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Haziran 2021.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. s. A23. ISBN 0-618-94690-X.
- ^ S. H. Baekeland "Några sidor af den kemiska industrien" (1914) Svensk Kemisk Tidskrift, p. 140 3 Mart 2016 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ a b Friedrich Georg Wieck, Uppfinningarnas bok (1873, Swedish translation of Buch der Erfindungen), vol. 4, p. 473 11 Ekim 2016 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ Stephen R. Bown, A Most Damnable Invention: Dynamite, Nitrates, and the Making of the Modern World, Macmillan, 2005, 0-312-32913-X, p. 157.
- ^ Arias, Jaime (24 Temmuz 2003). On the Origin of Saltpeter, Northern Chile Coast. International Union for Quaternary Research. 4 Mart 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 Ağustos 2018.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;nitrate_townsisimli refler için metin sağlanmadı (Bkz: ) - ^ Kaynak hatası: Geçersiz
<ref>etiketi;ghost_townsisimli refler için metin sağlanmadı (Bkz: ) - ^ Albert A. Robbins "Chemical freezing package" ABD patent 2.898.744, Issue date: August 1959.
- ^ UK Food Standards Agency: "Current EU approved additives and their E Numbers". 2 Mayıs 2006 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Ekim 2011.
- ^ US Food and Drug Administration: "Listing of Food Additives Status Part II". 8 Ocak 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Ekim 2011.
- ^ Australia New Zealand Food Standards Code"Standard 1.2.4 - Labelling of ingredients". 19 Ocak 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Ekim 2011.
- ^ De La Monte, SM; Neusner, A; Chu, J; Lawton, M (2009). "Epidemilogical trends strongly suggest exposures as etiologic agents in the pathogenesis of sporadic Alzheimer's disease, diabetes mellitus, and non-alcoholic steatohepatitis". Journal of Alzheimer's Disease. 17 (3): 519-29. doi:10.3233/JAD-2009-1070. PMC 4551511 $2. PMID 19363256.
- ^ Jakszyn, Paula; Gonzalez, Carlos-Alberto (21 Temmuz 2006). "Nitrosamine and related food intake and gastric and oesophageal cancer risk: a systematic review of the epidemiological evidence". World Journal of Gastroenterology. 12 (27): 4296-4303. doi:10.3748/wjg.v12.i27.4296. PMC 4087738 $2. PMID 16865769. 14 Ekim 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Temmuz 2020.
- ^ Cross, AJ; Ferrucci, LM; Risch, A; Graubard, BI; Ward, MH; Park, Y; Hollenbeck, AR; Schatzkin, A; Sinha, R (2010). "A large prospective study of meat consumption and colorectal cancer risk: An investigation of potential mechanisms underlying this association". Cancer Research. 70 (6): 2406-14. doi:10.1158/0008-5472.CAN-09-3929. PMC 2840051 $2. PMID 20215514.
- ^ "The Associations between Food, Nutrition and Physical Activity and the Risk of Colorectal Cancer" 26 Temmuz 2019 tarihinde Wayback Machine sitesinde arşivlendi., World Cancer Research Fund (2010)
- ^ Machha, Ajay; Schechter, Alan N. (August 2011). "Dietary nitrite and nitrate: a review of potential mechanisms of cardiovascular benefits". European Journal of Nutrition. 50 (5): 293-303. doi:10.1007/s00394-011-0192-5. ISSN 1436-6207. PMC 3489477 $2. PMID 21626413.
Konuyla ilgili yayınlar
- Barnum, Dennis (2003). "Some History of Nitrates". Journal of Chemical Education. Cilt 80. ss. 1393-. doi:10.1021/ed080p1393.
| HNO3 | He | ||||||||||||||||
| LiNO3 | Be(NO3)2 | B(NO3)-4 | RONO2 | NO-3 NH4NO3 | HOONO2 | FNO3 | Ne | ||||||||||
| NaNO3 | Mg(NO3)2 | Al(NO3)3 | Si | P | S | ClONO2 | Ar | ||||||||||
| KNO3 | Ca(NO3)2 | Sc(NO3)3 | Ti(NO3)4 | VO(NO3)3 | Cr(NO3)3 | Mn(NO3)2 | Fe(NO3)2 Fe(NO3)3 | Co(NO3)2 Co(NO3)3 | Ni(NO3)2 | CuNO3 Cu(NO3)2 | Zn(NO3)2 | Ga(NO3)3 | Ge | As | Se | BrNO3 | Kr |
| RbNO3 | Sr(NO3)2 | Y(NO3)3 | Zr(NO3)4 | Nb | Mo | Tc | Ru(NO3)3 | Rh(NO3)3 | Pd(NO3)2 Pd(NO3)4 | AgNO3 Ag(NO3)2 | Cd(NO3)2 | In(NO3)3 | Sn(NO3)4 | Sb(NO3)3 | Te | INO3 | Xe(NO3)2 |
| CsNO3 | Ba(NO3)2 | Hf(NO3)4 | Ta | W | Re | Os | Ir | Pt(NO3)2 Pt(NO3)4 | Au(NO3)3 | Hg2(NO3)2 Hg(NO3)2 | TlNO3 Tl(NO3)3 | Pb(NO3)2 | Bi(NO3)3 BiO(NO3) | Po(NO3)4 | At | Rn | |
| FrNO3 | Ra(NO3)2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La(NO3)3 | Ce(NO3)3 Ce(NO3)4 | Pr(NO3)3 | Nd(NO3)3 | Pm(NO3)3 | Sm(NO3)3 | Eu(NO3)3 | Gd(NO3)3 | Tb(NO3)3 | Dy(NO3)3 | Ho(NO3)3 | Er(NO3)3 | Tm(NO3)3 | Yb(NO3)3 | Lu(NO3)3 | |||
| Ac(NO3)3 | Th(NO3)4 | PaO2(NO3)3 | UO2(NO3)2 | Np(NO3)4 | Pu(NO3)4 | Am(NO3)3 | Cm(NO3)3 | Bk(NO3)3 | Cf | Es | Fm | Md | No | Lr | |||