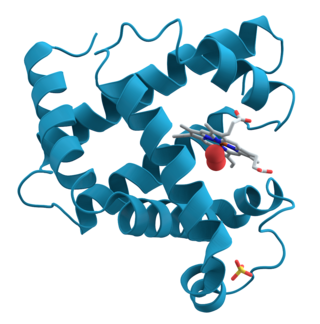
Proteinler, bir veya daha fazla uzun amino asit artık zincirini içeren büyük biyomoleküller ve makromolekül'lerdir. Proteinler organizmalar içinde, hücrelere yapı ve organizmalar sağlayarak ve molekülleri bir konumdan diğerine taşıyarak metabolik reaksiyonları katalizleme, DNA kopyalama, uyaranlara yanıt verme dahil olmak üzere çok çeşitli işlevler gerçekleştirir. Proteinler, genlerinin nükleotit dizisi tarafından dikte edilen ve genellikle faaliyetini belirleyen özel 3D yapıya protein katlanmasıyla sonuçlanan amino asit dizilimlerinde birbirlerinden farklıdır.

Oksijen atom numarası 8 olan ve O harfi ile simgelenen kimyasal elementtir. Oksijen ismi Yunanca ὀξύς (oxis - "asit", tam anlamıyla "keskin", asitlerin acı tadı kastedilir) ve -γενής (-genēs) ("üretici", tam anlamıyla "sebep olan şey") köklerinden gelmektedir, çünkü isimlendirildiği zamanlarda tüm asitlerin oksijen içerikli olduğu sanılırdı. Standart şartlar altında, elementin iki atomu bağlanarak çok soluk mavi renkte, kokusuz, tatsız, diatomik yapıdaki, O2 formülüne sahip dioksijen gazını oluşturur.

Amino asitler, proteinleri oluşturan temel yapı taşlarıdır.

Nükleik asitler, bütün canlı hücrelerde ve virüslerde bulunan, nükleotid birimlerden oluşmuş polimerlerdir. En yaygın nükleik asitler deoksiribonükleik asit (DNA) ve ribonükleik asit (RNA)'dır. İnsan kromozomlarını oluşturan DNA milyonlarca nükleotitten oluşur. Nükleik asitlerin başlıca işlevi genetik bilgi aktarımını sağlamaktır.
Hidroliz işlemi suyu oluşturan hidrojen ve oksijen elementlerinin birbirinden ayrılması ile sonuçlanan bir işlemdir. Bazı kaynaklarda hidroliz, moleküllerin su ilavesiyle daha fazla sayıda parçacık oluşturması olarak da geçer. Hidroliz, su ile bir kimyasal bağın parçalanmasıdır yani bir kimyasal reaksiyondur. Hidroliz genel olarak suyun nükleofil olduğu ikame(yer değiştirme reaksiyonu), eliminasyon(organik reaksiyon türü) ve solvasyon (çözme) reaksiyonları için kullanılır.

Molekül, birbirine bağlı gruplar halindeki atomların oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır. Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farklı sayılarda farklı atomların bağlanması sonucunda oluşabilirler. Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve 2 oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 1996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen. Molekülleri oluşturan kimyasal bağlara Moleküler bağlar denir. Bunlar kovalent, iyonik ve metalik bağlardır.
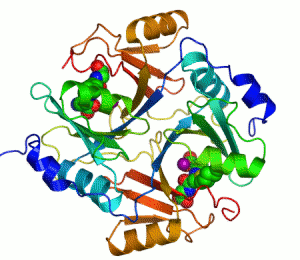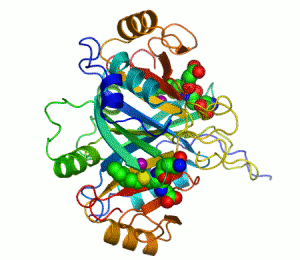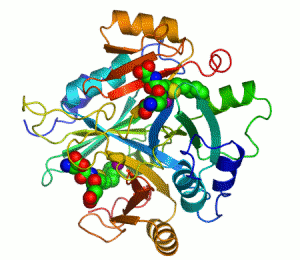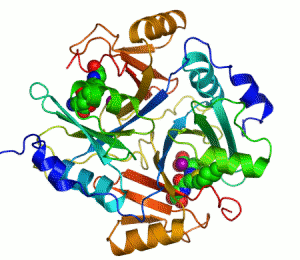
Enzimler, kataliz yapan biyomoleküllerdir. Neredeyse tüm enzimler protein yapılıdır. Enzim tepkimelerinde, bu sürece giren moleküllere substrat denir ve enzim bunları farklı moleküllere, ürünlere dönüştürür. Bir canlı hücredeki tepkimelerin neredeyse tamamı yeterince hızlı olabilmek için enzimlere gerek duyar. Enzimler substratları için son derece seçici oldukları için ve pek çok olası tepkimeden sadece birkaçını hızlandırdıklarından dolayı, bir hücredeki enzimlerin kümesi o hücrede hangi metabolik yolakların bulunduğunu belirler.

Oksijenli solunum, organik besinlerden oksijen yoluyla ATP elde etme işidir. Hücrelerdeki bazı kimyasal tepkimelerde kullanılan enerjinin oksijen kullanılarak açığa çıkarılması demektir. Biyoloji ders kitapları sık sık hücresel solunum sırasında glikoz molekülü başına 38 ATP molekülü üretildiğini söylese de sızıntılı zarların yanı sıra mitokondriyal matrikse pirüvat ve ADP hareketinin maliyetinden dolayı %100 verim olamayacağından bu sayıya asla ulaşılmaz, mevcut tahminler glikoz başına 29 ilâ 30 ATP dolayındadır.
Histidin doğada yaygın 22 aminoasitten biridir ve proteinlerin yapısında bulunur. L-Histidin ve D-Histidin olmak üzere iki farklı enantiomerik formu vardır. Beslenme açısından, genelde sadece çocuklarda, dışarıdan alınması zaruri gıda maddelerinden biridir.
RNA polimerazlar, bir DNA veya RNA molekülündeki bilgiyi RNA molekülü olarak kopyalayan bir enzimler ailesidir. Bir gende yer alan bilginin RNA molekülü olarak kopyalanma işlemi transkripsiyon olarak adlandırılır. Hücrelerde RNAP genlerin RNA zincirleri halinde okunmasını sağlar. RNA polimeraz enzimleri, tüm canlılarda ve çoğu virüste bulunur. Kimyasal bir deyişle, RNAP, bir nükleotidil transferaz enzimidir, bir RNA molekülünün üç ucunda ribonükleotitlerin polimerleşmesini sağlar.
Elektron taşıma sistemi veya elektron taşıma zinciri (İngilizce: Electron Transport System), NADH ve FADH2 gibi elektron taşıyıcılarının verdikleri elektronları ETS elemanlarında redoks tepkimelerine sokarak ATP üretimini sağlayan sistemin adıdır.Kristada bulunur.Kıvrımlı olan zar yüzeyinin genişlemesini saglar.Böylece enzimlerin etkinliklerinin artmasına olanak sağlar.Elektronlar, son elektron alıcısı oksijene varana kadar ETS elemanları boyunca taşınırlar ve enerji kaybederler. Elektronların verdiği enerji ETS elemanları tarafından protonların aktif taşınmasında kullanılır ve ETS elemanlarının üzerinde bulunduğu çift katlı fosfolipid zarının iki tarafında potansiyel fark oluşturulur. Bu potansiyel fark daha sonra ATP sentezi için kullanılır. Burada ATP sentezi H+ iyonlarının derişim farklılığına bağlı olarak dışarı pompalanır. Bu sırada ATP sentez enzimi aktifleşir ve ATP sentezlenir. ETS elemanları, ökaryotik hücrelerde mitokondri ve kloroplast organellerinde bulunur.
Biyokimyada, oksidoredüktaz, bir elektronun bir molekülden (indirgenden) bir diğerine aktarılmasını katalizleyen enzimdir. İndirgen için elektron veya hidrojen vericisi olarak da değinilir. Yükseltgen için hidrojen veya elektron alıcısı olarak da değinilir.
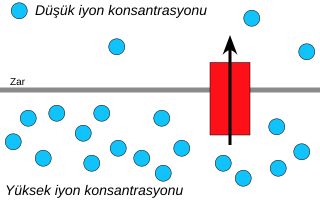
Kemiosmoz; iyonların, elektrokimyasal gradyanı azaltmak için seçici geçirgen bir zardan geçme hareketidir. Hücresel solunumdaki ATP sentezinin gerçekleşmesini sağlayan enerjinin büyük bir kısmı hidrojenlerin yaptığı bu hareketten karşılanır.

Hidrojen siyanür, HCN formüllü inorganik bir bileşiktir. Endüstriyel ölçekte üretilen HCN, polimerlerden ilaçlara kadar birçok kimyasal bileşik için oldukça değerli bir öncüdür. Büyük ölçekli uygulamalar, sırasıyla madencilik ve plastikte kullanılan potasyum siyanür ve adiponitril üretimi içindir. Hidrojen siyanür, 25 °C'de kaynayan renksiz acıbadem kokusunda bir sıvıdır. Uçucu bir sıvı olduğundan, katı siyanür bileşiklerinden daha zehirlidir.

Sitokromlar, genel olarak, zar bağlı hem grupları ihtiva eden ve öncelikle ATP üretiminden sorumlu olan elektron taşıma zincirinde elektron taşınmasından sorumlu hemoproteinlerdir.

Flavin, trisiklik heterosikl izoklooksazin tarafından oluşturulan, pteridine dayanan bir grup organik bileşiğin ortak adıdır. Biyokimyasal kaynak riboflavin vitaminidir. Flavin kısmı genellikle flavin adenin dinükleotidi (FAD) oluşturmak için bir adenosin difosfat ile birleştirilir ve diğer durumlarda, flavin mononükleotidi olarak fosforlanmış bir riboflavin biçimi olarak bulunur. Flavin, flavoproteinlerde protez grubu olarak bulunur.
Sitokrom P450 (CYP), monooksigenaz olarak işlev gören ve hemleri kofaktör olarak içeren enzimlerin oluşturduğu bir protein süperfamilyasıdır. Memelilerde bu proteinler steroidleri, yağ asitlerini ve ksenobiyotikleri okside eder ve çeşitli bileşiklerin klirensinde olduğu kadar hormon sentezinde ve çözümünde önemli yer tutarlar. Bitkilerde ise bu proteinler savunma bileşikleri, yağ asitleri ve hormonların biyosentezi için önemlidir.
NADPH oksidaz hücre dışı boşluğa bakan zara bağlı bir enzim kompleksidir. Plazma zarında ve ayrıca nötrofil beyaz kan hücreleri tarafından mikroorganizmaları yutmak için kullanılan fagozomların zarlarında bulunabilir. Kompleksin katalitik bileşeninin insan izoformları arasında NOX1, NOX2, NOX3, NOX4, NOX5, DUOX1 ve DUOX2 bulunur.
Kuantum biyolojisi, kuantum mekaniğinin ve teorik kimyanın biyolojik nesnelere ve problemlere uygulamalarının incelenmesidir. Birçok biyolojik süreç, enerjinin kimyasal dönüşümler için kullanılabilen biçimlere dönüştürülmesini içerir ve doğası gereği kuantum mekaniktir. Bu tür süreçler, kimyasal reaksiyonları, ışık emilimini, uyarılmış elektronik durumların oluşumunu, uyarma enerjisinin aktarımını ve fotosentezi, koku almayı ve hücresel solunum gibi kimyasal süreçlerde elektron ve protonların aktarımını içerir.
İlaç metabolizması, ilaçların canlı organizmalar tarafından, genellikle özel enzimatik sistemler aracılığıyla metabolik olarak parçalanmasıdır. Daha genel olarak, ksenobiyotik metabolizması, herhangi bir ilaç veya zehir gibi bir organizmanın normal biyokimyasına yabancı bileşikler olan ksenobiyotiklerin kimyasal yapısını değiştiren metabolik yollar kümesidir. Bu yollar, tüm büyük organizma gruplarında bulunan bir biyotransformasyon şeklidir ve antik kökenli olduğu düşünülmektedir. Bu reaksiyonlar genellikle zehirli bileşiklerin detoksifikasyonunu sağlar. İlaç metabolizmasının incelenmesine farmakokinetik denir.











