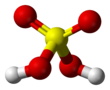
Sülfürik asit
Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır.[1] Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
| |||
 | |||
| Adlandırmalar | |||
|---|---|---|---|
Sülfürik asit | |||
Diğer adlar Vitriol yağı Hidrojen sülfat Sülfat asidi Zaç yağı | |||
| Tanımlayıcılar | |||
CAS numarası | |||
3D model (JSmol) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.763 | ||
| EC Numarası |
| ||
| E numaraları | E513 (asitliği düzenleyiciler, ...) | ||
| 2122 | |||
| KEGG | |||
PubChem CID | |||
| RTECS numarası |
| ||
| UNII | |||
| UN numarası | 1830 | ||
CompTox Bilgi Panosu (EPA) | |||
| |||
| |||
| Özellikler | |||
| Molekül formülü | H 2SO 4, bazen (HO) 2SO 2 olarak ifade edilir | ||
| Molekül kütlesi | 98,079 g/mol | ||
| Görünüm | Şeffaf, renksiz sıvı | ||
| Koku | Kokusuz | ||
| Yoğunluk | 1,84 g/cm3 (sıvı) | ||
| Erime noktası | 10,31[3] °C (50,56 °F; 283,46 K) | ||
| Kaynama noktası | 337[3] °C (639 °F; 610 K) Sülfürik asit 300 °C'nin (572 °F; 573 K) üzerinde yavaş yavaş SO 3 + H 2O'ya ayrışır | ||
| Buhar basıncı | 0,001 mmHg (20 °C)[2] | ||
| Asitlik (pKa) | pKa1 = −2,8 pKa2 = 1,99 | ||
| Konjuge baz | Bisülfat | ||
| Akmazlık | 26,7 cP (20 °C) | ||
| Yapı[4] | |||
| monoklinik kristal | |||
| C2/c | |||
a = 818,1(2) pm, b = 469,60(10) pm, c = 856,3(2) pm α = 90°, β = 111,39(3) pm°, γ = 90° | |||
Formül birimleri (Z) | 4 | ||
| Termokimya | |||
Standart molar entropi (S⦵298) | 157 J/(mol·K)[5] | ||
Standart formasyon entalpisi (ΔfH⦵298) | -814 kJ/mol[5] | ||
| Tehlikeler | |||
| GHS etiketleme sistemi: | |||
| Piktogramlar |   | ||
| İşaret sözcüğü | Tehlike | ||
| R-ibareleri | R35 | ||
| Tehlike ifadeleri | H314 | ||
| Önlem ifadeleri | P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P405, P501 | ||
| NFPA 704 (yangın karosu) | |||
| Parlama noktası | yanıcı değil | ||
Maruz kalma sınır değeri (TLV) | 15 mg/m3 (IDLH), 1 mg/m3 (TWA), 2 mg/m3 (STEL) | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) | 2140 mg/kg (sıçan, oral)[6] | ||
LC50 (medyan konsantrasyon) |
| ||
LCLo (yayınlanan en düşük) | 87 mg/m3 (hint domuzu, 2,75 sa)[6] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 1 mg/m3[2] | ||
| REL (tavsiye edilen) | TWA 1 mg/m3[2] | ||
| IDLH (anında tehlike) | 15 mg/m3[2] | ||
| AB sınıflandırması | Hazchem C[7][8] | ||
| Güvenlik bilgi formu (SDS) | External MSDS | ||
| Benzeyen bileşikler | |||
Benzeyen güçlü asitler |
| ||
Benzeyen bileşikler |
| ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
Üretimi
Çok önemli bir kimyasal madde olan sülfürik asit sanayide değme yöntemi ya da kurşun odalar yöntemi ile üretilir.[9] Bu yöntemlerde kükürt dioksit çeşitli katalizörler(vanadyum pentoksit) eşliğinde oksijenle yükseltgenerek kükürt triokside dönüştürülür ardından kükürt trioksit suyla tepkimeye sokularak sülfürik asit elde edilir. Sülfürik asit çeşitli derişimleri halinde gübre, pigment, boyar madde, patlayıcı madde, ilaçlama, inorganik tuz ve petrol arıtım ve metalurji işlemlerinde kullanılır. Ayrıca çeşitli pillerin yapımında da sülfürik asitten yararlanılır. Halk arasında "akü asidi" diye bilinir. Elektriği iletir. Suda çözündüğünde çok yüksek ısı çıkar.
Piyasada satılan sülfürik asitler çoğunlukla yüzde 78,93 ya da 98'liktir.
Kimyasal özellikler
Metal tepkimeleri
Sülfürik asit metallere sülfat iyonu vererek metal sülfat oluşumu sağlar.
- Demir ve sülfürik asit tepkimesi
- Alüminyum ve sülfürik asit tepkimesi
- Çinko ve sülfürik asit tepkimesi
Ametal tepkimeleri
Sülfürik asit kükürt ve karbon ile tepkimeye girer
Sodyum klorür ile tepkimesi
Sodyum klorür ile tepkimeye girerek hidrojen klorür üretimini sağlar.
Çeşitli maddelerle verdiği tepkimeler

Sülfürik asit bez kumaş şeker gibi maddelerle tepkime verdiğinde siyah kül benzeri bir renk açığa çıkarır.
Kullanım alanları
Sülfürik asit renksiz, yağımsı bir sıvıdır. Konsantre sülfürik asit, kütlece %96,98 oranında H2SO4 içerir. Özelliklerinden biri de, suya yakın bir madde olmasıdır. Konsantre sülfürik asit, birçok organik maddeden suyu çeker ve ısıveren (egzotermik) bir tepkime oluşturur. Bu özelliğinden dolayı, temas edildiğinde cilde büyük zararlar verebilir. Yine aynı sebepten dolayı, sülfürik asiti seyreltme işlemi çok dikkatli yapılmalıdır. 1 mol sülfürik asit bol miktarda suya eklendiğinde, yaklaşık 880 kJ enerji açığa çıkar. Konsantre sülfürik asitin içine su eklemek çok tehlikelidir. Çünkü su, yüksek ekzotermik tepkimeden dolayı asitin üstünde kabarcıklar oluşturarak, çok ani bir şekilde kaynar. H2SO4 kimya endüstrisinde en çok üretilen ve kullanılan maddelerden biridir. Tarım endüstrisinde büyük miktarlarda asit, kalsiyum fosfat Ca3(PO4)2 gibi çözünmeyen fosfat kayalarından, çözünebilir kalsiyum dihidrojen fosfat elde etmek için kullanılır. Sülfürik asit üretiminde kullanılan endüstriyel metodun adı “değme işlemi”dir. İlk adımda, sülfür ve sülfitlerin yanmasıyla kükürt dioksit oluşturulur. Sülfürik asit piyasada drenaj temizleyici ve akülerde karşımıza çıkmaktadır.
S8 (g) + 8 O2 (g) → 8 SO2 (g) (ΔH° = -2374 kJ/ç.mol)
2 H2S (g) + 3 O2 (g) → 2 SO2 (g) + 2 H2O (g) (ΔH° = -1037 kJ/mol)
Sülfür dioksit daha fazla oksijenle tepkimeye girerek sülfür trioksit oluşturur, ama bu tepkime daha yavaş gerçekleşir. Kontak işleminde sülfür dioksit ve oksijen karışımı, platin metali veya vanadyum oksit katalizörleri yüzeyine temas ederek geçer.
2 SO2 (g) + O2 (g) → 2 SO3 (g) (ΔH° = -226 kJ/mol)
Sülfürik asitin direkt çözünümü, sülfürik asit nemi oluşturur. Oluşan bu nem, suyla karıştırıldığında konsantre sülfürik asit elde edilir. Dikkat edilirse değme işlemindeki tepkimelerin ekzotermik olduğu görülür. Sülfürik asit üreten fabrikalar, açığa çıkan bu ısıdan da yararlanırlar.
Sağlık açısından riskleri
Hangi konsantrasyonda olursa olsun, gözlerle teması tehlikelidir. Derişik sülfürik asit gayet kaşındırıcı olup, deride şiddetli yanıklar meydana getirir. Temas halindeki bölge göz duşu veya seyreltik baz ile yıkanmalıdır. Su ile yıkandığı takdirde ısı açığa çıkacaktır ve termal yanıklara sebebiyet verecektir.

Dünya dışında sülfürik asit
Dünya dışında sülfürik asit venüs gezegeninde karşımıza çıkmaktadır.Venüs atmosferinde oldukça kalın sülfürik asit bulutları bulunmaktadır. Bunlar yağmur olarak venüs yüzeyine yağmaktadır.
Kaynakça
- ^ Khairallah, Amin A. Outline of Arabic Contributions to Medicine, chapter 10. Beirut, 1946.
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0577". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b Haynes, William M. (2014). CRC Handbook of Chemistry and Physics (İngilizce) (95 bas.). CRC Press. ss. 4-92. ISBN 9781482208689. Erişim tarihi: 18 Kasım 2018.
- ^ Kemnitz, E.; Werner, C.; Trojanov, S. (15 Kasım 1996). "Reinvestigation of Crystalline Sulfuric Acid and Oxonium Hydrogensulfate". Acta Crystallographica Section C Crystal Structure Communications. 52 (11): 2665-2668. doi:10.1107/S0108270196006749.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. s. A23. ISBN 978-0-618-94690-7.
- ^ a b c "Sulfuric acid". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ "NuGenTec Material Safety Datasheet-Sulfuric acid" (PDF). 15 Şubat 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 13 Nisan 2016.
- ^ "Sulfuric acid IPCS". 3 Mart 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Nisan 2016.
The substance is harmful to aquatic organisms.(ENVIRONMENTAL DATA)
- ^ "Tarım orman" (PDF). 9 Temmuz 2022 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 10 Mart 2024.
- Institut National de Recherche et de Sécurité. (1997). "Acide sulfurique". Fiche toxicologique n°30, Paris: INRS, 5 pp.
- Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- Agamanolis DP. Metabolic and toxic disorders. In: Prayson R, editor. Neuropathology: a volume in the foundations in diagnostic pathology series. Philadelphia: Elsevier/Churchill Livingstone, 2005; 413-315.