
Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.
Polivinil klorür, oldukça geniş kullanım alanı olan bir plastik polimer. Vinil klorürün polimerleştirilmesi ile elde edilir. Polietilen ve polipropilenden sonra dünyada en çok üretilen üçüncü sentetik plastik polimerdir.
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.
İnorganik kimya veya anorganik kimya; organik olmayan, yani karbon-hidrojen bağı içermeyen bileşiklerin özelliklerini ve kimyasal davranışlarını inceleyen kimya dalı. Anorganik ve organik kimyayı birleştiren organometalik bileşikler, organometalik kimya adında başka bir dalı oluşturur.

Renyum, Atom numarası 75, atom ağırlığı 186,2, yoğunluğu 21 olan, parlak beyaz renkte ve 3150 °C'de eriyen bir element. Kısaltması Re.
Klorür, nötr hâldeki klor atomunun, bir elektron alarak iyon (anyon) hâline geçtiğinde aldığı isim. Cl− olarak gösterilir. Klorür iyonu içeren maddelere de verilen bir isimdir. Bir iyon olduğundan dolayı, kendi başına doğada yer almaz; ancak bir çözeltide karşı iyonu ile yer alabilir.
Bohriyum veya eka-renyum, atom numarası 107, atom ağırlığı 264 olan, 25 °C'de katı olduğu, gümüş renginde veya gri renkte olduğu tahmin edilen yapay bir element. İsmini ünlü fizikçi Niels Bohr anısına almıştır.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.
Elektrolit, iyonların hareketi sayesinde elektriksel olarak iletken olan, ancak elektronları iletmeyen ilenler içeren bir ortamdır. Su gibi polar çözücü içinde çözülmüş çoğu çözünür tuzları, asitleri ve bazları içermektedir. Çözünüm sonrasında; madde çözücü içinde eşit olarak dağıtılan katyonlara ve anyonlara ayrılmaktadır. Katı hal elektrolitleri de mevcuttur. Tıpta elektrolit terimi, çözünen maddeyi ifade etmektedir.
Demir klorür, demir ve klor elementlerinden meydana gelen bir bileşiktir.

Banal milliyetçilik, insanlar arasında ulusal aidiyet duygusunu paylaşan milletin günlük tasvirlerini ifade eder. Terim, Michael Billig'in 1995'te yayımlanan aynı adlı kitabından türetilmiştir ve eleştirel olarak anlaşılması amaçlanmıştır. Konsept, özellikle siyasi coğrafya disiplini içerisinde, 1990'larda yayınlanmasından bu yana akademik görüşlerin sürmesi ile son derece etkili olmuştur. Günümüzde bu terim öncelikle kimlik oluşumu ve jeopolitik akademik tartışmalarda kullanılmaktadır.
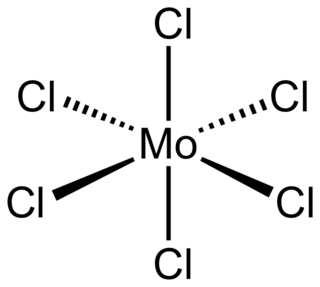
Molibden(VI) klorür, MoCl6 formülüne sahip bir inorganik bileşiktir. Siyah ve diyamanyetik olan bir katıdır. Moleküllerin kristal yapısı tungsten (VI) klorür gibi oktahedraldir.

Organoklorürler, klorlu hidrokarbonlar ya da klorokarbonlar, en az bir adet kovalent bağlanmış klor atomuna sahip organik bileşiklerdir. En basit örnekleri kloroalkanlardır. Organoklorürlerin geniş bir yapısal çeşitliliğe sahip olması onların farklı kimyasal özelliklere, isimlere ve kullanım alanlarına sahip olmasına sebep olmuştur. Bazı organoklorürlerin yararlı olmasına karşın bazıları zehirli ve çevreye zararlıdır.

Sodyum klorür, yaygın olarak 'tuz' ismiyle bilinen kimyasal formülü NaCl; 1/1 oranında sodyum ve klorür iyonları olan iyonik bileşik. Molar kütleleri sırasıyla 22.99 ve 35.45 g/moldur. 100 g NaCl, 39.34 g Na ve 60.66 g Cl içerir. Sodyum klorür, deniz suyunun tuzluluğundan ve birçok çok hücreli organizmanın hücre dışı sıvısından en çok sorumlu olan tuzdur. Yenilebilir sofra tuzu biçiminde yaygın olarak bir çeşni ve gıda koruyucusu olarak kullanılır. Birçok endüstriyel proseste büyük miktarlarda sodyum klorür kullanılır ve daha ileri kimyasal sentezler için hammadde olarak kullanılan sodyum ve klor bileşiklerinin ana kaynağıdır. Sodyum klorürün ikinci bir ana uygulaması donma sıcaklığı altındaki havalarda yolların buzunun çözülmesidir.
Bütil klorür (C4H9Cl) deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan herhangi birini ifade edebilir:
- n-Bütil klorür (bütan-1-klorür)
- sec-Bütil klorür (bütan-2-klorür)
- İzobütil klorür (1-kloro-2-metilpropan)
- tert-Bütil klorür (2-kloro-2-metilpropan)
Platin klorür deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan herhangi birini ifade edebilir:
- Platin(II) klorür
- Platin(IV) klorür
Vanadyum klorür deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan herhangi birini ifade edebilir:
- Vanadyum(II) klorür, VCl2
- Vanadyum(III) klorür, VCl3
- Vanadyum(IV) klorür, VCl4
- Vanadyum(V) klorür, VCl5








