Purkinje hücreleri
| Purkinje hücreleri | |
|---|---|
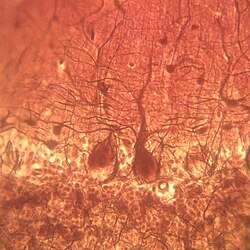 | |
| Latince isim | stratum purkinjense |
| Tanımlayıcılar | |
| JSTOR | purkinje-cells |
| Microsoft Academic | 2910921427 2778472085, 2910921427 |
| MeSH | D011689 |
| FMA | 67969 |
Purkinje hücreleri ya da Purkinje nöronları beyincikte yer alan bir sınıf Gabaerjik nöronlar. Çek anatomist Jan Evangelista Purkyně'nin 1839 yılındaki keşfi sayesinde kaşifinin ismini almıştır.
Yapısı



Bu hücreler insan beynindeki çok sayıda dendritik dikenler ile karakterize olmuş, çok karmaşık ve ayrıntılı dendritik dallara sahip en büyük sinir hücrelerinden (Betz hücreleri en büyük olmak üzere)[1] biridir. Purkinje hücreleri beyincikteki Purkinje tabakasında bulunur. Purkinje hücreleri tıpkı domino taşları gibi birbirinin önüne hizalanmış olarak bulunur. Geniş dendritik dalları, daha derin katmanlardan gelen paralel liflerin geçtiği neredeyse iki boyutlu katmanlar oluşturur. Bu paralel lifler Purkinje hücrelerindeki dendritlere nispeten zayıf uyarıcı (glutamaterjik) sinapslar yaparlar, oysa medulladaki inferior olivary nükleustan gelen tırmanma lifleri proksimal dendritlere ve hücre somasına oldukça güçlü uyarıcı girdi sağlamaktadır. Paralel lifler Purkinje nöronunun dendritik ağaçlarından 200.000 paralel life kadar dik olarak geçerler[2] ve sadece bir adet Purkinje hücresiyle Granül hücre - Purkinje hücresi sinapsı oluştururlar. Her Purkinje hücresi, hepsi tek bir tırmanan liften gelen yaklaşık 500 tırmanan lif sinapsı alır.[3] Hem sepet hücreleri hem yıldız hücreleri (serebellar moleküler tabakada bulunur) Purkinje hücrelerine inhibitör (Gabaerjik) giri sağlarlar, sepet hücreleri Purkinje hücrelerinin akson başlangıç kesimine ve yıldız hücreleri dendritlere sinaps yaparlar.
Purkinje hücreleri derin beyincik çekirdeklerine baskılayıcı (inhibitör) atımlar gönderir ve serebellar kortekste motor koordinasyon için tek bir çıktı sağlar.
Moleküler
Beyincikte bulunan Purkinje katmanında Purkinje hücre gövdeleri ve Bergmann glia bulunur ve fazlaca benzersiz gen ifade edilir.[4] Purkinjeye özgü gen işaretleri de, Purkinje-eksik farelerle vahşi farelerin transkriptomları kıyaslanarak önerilmiştir.[5] Bir örnek nakavt farelerdeki purkinje proteini 4 (PCP4), Purkinje hücrelerinde belirgin olarak sinaptik plastisitede değişkenlik ve lokomotor öğrenmede bozulma gösterirler.[6] PCP4 Purkinje hücrelerinin sitoplazmasında kalsiyum (Ca2+) ile kalmodulin (CaM) hem oluşumunu hem ayrılmasını hızlandırır, olmaması durumunda bu sinir hücrelerinin fizyolojisi bozulur.[7][8]
Gelişimi
Farelerde ve insanlarda kemik iliği hücrelerinin, beyincik Purkinje hücreleri ile ya birleştiğini ya da onları oluşturduğuna dair kanıtlar mevcuttur ve kemik iliği hücrelerinin ister doğrudan oluşturarak, ister birleşerek, merkezi sinir sisteminin hasar görmesi durumunda onarmında rol oynaması mümkündür.[9][10][11][12][13] İleri kanıtlar insan adrenal korteksinde Purkinje nöronlarının, B-lenfositlerin ve aldosteron üreten hücrelerin arasında ortak bir kök hücre atasının varlığını işaret etmektedir.
Fonksiyonu

MF: Yosunsu lifler.
DNC: Derin beyincik çekirdekleri.
İO: İnferior olive.
CF: Tırmanan lifler.
GC: Granül hücreleri.
PF: Paralel lifler.
PC: Purkinje hücreleri.
GgC: Golgi hücreleri.
SC: Yıldız hücreleri.
BC: Sepet hücreleri.
Purkinje hücreleri iki farklı elektrofizyolojik aktivite formu gösterir:
- Basit atımlar 17 – 150 Hz (Raman ve Bean, 1999) aralığında, spontan olarak ya da Purkinje hücreleri paralel fiberler, granül hücrelerinin aksonları tarafından sinaptik olarak uyarıldığında ortaya çıkarlar.
- Karmaşık atımlar yavaştır, 1–3 Hz atımlar, başlangıçta uzun süreli ve büyük genlikli bir atımın ardından izlenen yüksek frekanslı küçük genlikli aksiyon potansiyeli patlamalarıyla karakterize olmuştur. Tırmanan liflerin aktive edilmesi sebebiyle bu durum gözlenir ve dendritlerde kalsiyum aracılı aksiyon potansiyellerinin oluşunu da içerebilir. Karmaşık atım aktivitesini takip eden basit atımlar güçlü atım girdileri tarafından baskılanabilir.[14]
Purkinje hücreleri hem sodyuma bağlı hem kalsiyuma bağlı spontan tren şeklinde elektrofizyolojik aktivite gösterirler. Bu ilk olarak Rodolfo Llinas (Llinas ve Hess (1977) ve Llinas ve Sugimori (1980)) tarafından gösterilmiştir. Beyincik fonksiyonunda çok önemli rol oynayan P-tipi kalsiyum kanalları Purkinje hücrelerinden sonra, ilk defa burada rastgelindiği için bu ismi almışlardır. Purkinje hücrelerinin tırmanan lifler tarafından aktive edilmesinin, sessiz halden spontan aktivite haline geçişi ya da tersini sağlayarak bir nevi değişim düğmesi gibi davrandığını biliyoruz.[16] Bu bulgular, tırmanan lif girdilerinin özellikle anestezi halindeki hayvanlarda görüldüğü ve uyanık haldeki hayvanlarda Purkinje hücrelerinin genelde, neredeyse her zaman süregelen bir biçimde olduğu fikriyle tartışılmıştır.[17] Fakat bu son çalışmanın kendisi de tartışmalı duruma gelmiştir[18] ve Purkinje hücrelerinin değiştirme özelliği uyanık kedilerde gözlemlenmiştir.[19] Purkinje hücrelerine ait bir hesaplamalı model, hücre içi kalsiyum hesaplamasının bu değiştirme özelliğine sebep olduğunu göstermiştir.[20]
Bulgular Purkinje hücre dendritlerinin endokanabinoit salgıladığı ve bunun hem uyarıcı hem de baskılayıcı sinapsların baskılayabileceğini önermiştir.[21] Purkinje hücrelerinin iç aktivite modu sodyum-potasyum pompası ile ayarlanır ve kontrol edilir.[22] Bu da pompanın basitçe homeostatik, iyonik eğimlerde "bakıcı" molekül olmayabileceğini, bunun yerine beyinde ve beyincikte hesaplama unsuru olabileceğini gösterir.[23] Nitekim, Na+-K+ pompasında meydana gelen bir mutasyon hızlı başlangıçlı distoni parkinsonuna sebebiyet verir; semptomları beyincik hesaplamasında bir patoloji olduğunu gösterir.[24] Ayrıca, canlı farelerde Na+-K+ pompalarını bloke etme amacıyla kullanılan ouabain zehri ataksi ve distoniyi tetikler.[25] Deneysel verilerin sayısal modellemenmesinde in vivo olarak Na+-K+ pompasının uzun suskun duraklamalar (>>1> s) ürettiğini gösterir; bunun da hesaplamasal bir rolü olabilir.[20] Alkol beyincikte Na+-K+ pompasını engeller ve beyinciksel hesaplamanın ve vücut koordinasyonunun bozulmasını da muhtemelen bu şekilde olmaktadır.[26][27]
Klinik önemi
İnsanlarda Purkinje hücreleri çeşitli sebeplerden hasar görebilir: toksik maruziyet, örneğin alkol ya da lityum; otoimmün hastalıklar; spinoserebellar ataksilere sebep olan genetik mutasyonlar, Unverricht-Retezova hastalığı ya da otizm; ve genetik temeli bilinmeyen nörodejeneratif hastalıklar, örneğin serebellar tip çoklu sistem atrofisi ya da düzensiz ataksiler.
Bazı evcil hayvanlar serebelar abiotrofi ismi verilen, doğumdan kısa bir süre sonra Purkinje hücrelerinin atrofiye başladığı bir durum geliştirebilir. Ataksi, niyet titremesi, hiperaktivite, tehdit refleksinde azalma, sert ya da yüksek adımlı yürüyüş, ayak pozisyonunun farkındalığında azalma (bazen çarpık yürüyüş ya da duruş) ve uzaklığı ve boyutu algılayamama gibi semptomlara sebep olabilir.[28] Serebellar hipoplazi olarak bilinen benzer bir durum da doğumdan önce uteroda Purkinje hücrelerinin gelişememesi sebebiyle oluşur.
Ataksi telenjiektazi ve Niemann Pick hastalığı tip C gibi genetik durumlar ve beyincik temel titremesi, Purkinje hücrelerinin giderek kaybolmasına sebebiyet verir. Alzheimer hastalığında bazen spinal patoloji ve Purkinje hücre dendritlerinin kaybı görülür.[29] Purkinje hücreleri ayrıca kuduz virüsü sebebiyle de zarar görebilir, zira virüs enfeksiyon bölgesinden merkezi sinir sistemine geçer.[30]
Kaynakça
- ^ Purves D, Augustine GJ, Fitzpatrick D, Hall WC, LaMantia A, McNamara JO, and White LE (2008). Neuroscience. 4th ed. Sinauer Associates. ss. 432-4. ISBN 978-0-87893-697-7.
- ^ Tyrrell, T; Willshaw, D (29 Mayıs 1992). "Cerebellar cortex: its simulation and the relevance of Marr's theory". Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 336 (1277). ss. 239-57. doi:10.1098/rstb.1992.0059. PMID 1353267.
- ^ Wadiche, JI; Jahr, CE (25 Ekim 2001). "Multivesicular release at climbing fiber-Purkinje cell synapses". Neuron. 32 (2). ss. 301-13. doi:10.1016/S0896-6273(01)00488-3. PMID 11683999.
- ^ Kirsch, L; Liscovitch, N; Chechik, G (Aralık 2012). Ohler, Uwe (Ed.). "Localizing Genes to Cerebellar Layers by Classifying ISH Images". PLoS Computational Biology. 8 (12). ss. e1002790. doi:10.1371/journal.pcbi.1002790. PMC 3527225 $2. PMID 23284274.
- ^ Rong, Y; Wang T; Morgan J (2004). "Identification of candidate purkinje cell-specific markers by gene expression profiling in wild-type and pcd3j mice". Molecular Brain Research. 13 (2). ss. 128-145. doi:10.1016/j.molbrainres.2004.10.015.
- ^ Wei P, Blundon JA, Rong Y, Zakharenko SS, Morgan JI (2011). "Impaired locomotor learning and altered cerebellar synaptic plasticity in pep-19/PCP4-null mice". Mol. Cell. Biol. 31 (14). ss. 2838-44. doi:10.1128/MCB.05208-11. PMC 3133400 $2. PMID 21576365.
- ^ Putkey JA, Kleerekoper Q, Gaertner TR, Waxham MN (2004). "A new role for IQ motif proteins in regulating calmodulin function". J. Biol. Chem. 278 (50). ss. 49667-70. doi:10.1074/jbc.C300372200. PMID 14551202.
- ^ Kleerekoper QK, Putkey JA (2009). "PEP-19, an intrinsically disordered regulator of calmodulin signaling". J. Biol. Chem. 284 (12). ss. 7455-64. doi:10.1074/jbc.M808067200. PMC 2658041 $2. PMID 19106096.
- ^ Hess DC, Hill WD, Carroll JE, Borlongan CV (2004). "Do bone marrow cells generate neurons?". Archives of Neurology. 61 (4). ss. 483-485. doi:10.1001/archneur.61.4.483. PMID 15096394. 23 Nisan 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Weimann JM, Johansson CB, Trejo A, Blau HM (2003). "Stable reprogrammed heterokaryons form spontaneously in Purkinje neurons after bone marrow transplant". Nature Cell Biology. 5 (11). ss. 959-966. doi:10.1038/ncb1053. PMID 14562057. 23 Nisan 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Alvarez-Dolado M, Pardal R, Garcia-Verdugo JM, Fike JR, Lee HO, Pfeffer K, Lois C, Morrison SJ, Alvarez-Buylla A (2003). "Fusion of bone-marrow-derived cells with Purkinje neurons, cardiomyocytes and hepatocytes". Nature. 425 (6961). ss. 968-973. doi:10.1038/nature02069. PMID 14555960. 25 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Felizola SJ, Katsu K, Ise K, Nakamura Y, Arai Y, Satoh F, Sasano H (2015). "Pre-B lymphocyte protein 3 (VPREB3) expression in the adrenal cortex: precedent for non-immunological roles in normal and neoplastic human tissues". Endocrine Pathology. Cilt 26. ss. 119-28. doi:10.1007/s12022-015-9366-7. PMID 25861052. 25 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Kemp K, Wilkins A, Scolding N (2014). "Cell fusion in the brain: two cells forward, one cell back". Acta Neuropathologica. 128 (5). ss. 629-638. doi:10.1007/s00401-014-1303-1. PMC 4201757 $2. PMID 24899142. 23 Nisan 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Eric R. Kandel, James H. Schwartz, Thomas M. Jessell (2000). Principles of Neural Science. 4/e. McGraw-Hill. pp.837-40.
- ^ Felizola SJ, Nakamura Y, Ono Y, Kitamura K, Kikuchi K, Onodera Y, Ise K, Takase K, Sugawara A, Hattangady N, Rainey WE, Satoh F, Sasano H (Apr 2014). "PCP4: a regulator of aldosterone synthesis in human adrenocortical tissues". Journal of Molecular Endocrinology. 52 (2). ss. 159-167. doi:10.1530/JME-13-0248. PMC 4103644 $2. PMID 24403568.
- ^ Loewenstein Y, Mahon S, Chadderton P, Kitamura K, Sompolinsky H, Yarom Y, ve diğerleri. (2005). "Bistability of cerebellar Purkinje cells modulated by sensory stimulation". Nature Neuroscience. Cilt 8. ss. 202-211. doi:10.1038/nn1393.
- ^ Schonewille M, Khosrovani S, Winkelman BH, Hoebeek FE, DeJeu MT, Larsen IM, ve diğerleri. (2006). "Purkinje cells in awake behaving animals operate at the up state membrane potential". Nature Neuroscience. Cilt 9. ss. 459-461. doi:10.1038/nn0406-459.
- ^ Loewenstein Y, Mahon S, Chadderton P, Kitamura K, Sompolinsky H, Yarom Y, ve diğerleri. (2006). "Purkinje cells in awake behaving animals operate at the up state membrane potential–Reply". Nature Neuroscience. Cilt 9. s. 461. doi:10.1038/nn0406-461.
- ^ Yartsev MM, Givon-Mayo R, Maller M, Donchin O (2009). "Pausing Purkinje cells in the cerebellum of the awake cat". Frontiers in Systems Neuroscience. Cilt 3. s. 2. doi:10.3389/neuro.06.002.2009.
- ^ a b Forrest MD (2014). "Intracellular Calcium Dynamics Permit a Purkinje Neuron Model to Perform Toggle and Gain Computations Upon its Inputs". Frontiers in Computational Neuroscience. Cilt 8. s. 86. doi:10.3389/fncom.2014.00086. PMC 4138505 $2. PMID 25191262. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Kreitzer AC, Regehr WG (Mart 2001). "Retrograde inhibition of presynaptic calcium influx by endogenous cannabinoids at excitatory synapses onto Purkinje cells". Neuron. 29 (3). ss. 717-27. doi:10.1016/S0896-6273(01)00246-X. PMID 11301030.
- ^ Forrest MD, Wall MJ, Press DA, Feng J (Aralık 2012). Cymbalyuk G (Ed.). "The Sodium-Potassium Pump Controls the Intrinsic Firing of the Cerebellar Purkinje Neuron". PLoS ONE. 7 (12). ss. e51169. doi:10.1371/journal.pone.0051169. PMC 3527461 $2. PMID 23284664. 4 Mayıs 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Forrest MD (Aralık 2014). "The sodium-potassium pump is an information processing element in brain computation". Frontiers in Physiology. 5 (472). doi:10.3389/fphys.2014.00472. 19 Ocak 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Cannon C (Temmuz 2004). "Paying the Price at the Pump: Dystonia from Mutations in a Na+/K+-ATPase". Neuron. 43 (2). ss. 153-154. doi:10.1016/j.neuron.2004.07.002. PMID 15260948. 13 Aralık 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Calderon DP, Fremont R, Kraenzlin F, Khodakhah K (Mart 2011). "The neural substrates of rapid-onset Dystonia-Parkinsonism". Nature Neuroscience. 14 (3). ss. 357-65. doi:10.1038/nn.2753. PMC 3430603 $2. PMID 21297628. 17 Ağustos 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Forrest MD (Nisan 2015). "Simulation of alcohol action upon a detailed Purkinje neuron model and a simpler surrogate model that runs >400 times faster". BMC Neuroscience. 16 (27). doi:10.1186/s12868-015-0162-6. 28 Ekim 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- ^ Forrest, Michael (Nisan 2015). "the_neuroscience_reason_we_fall_over_when_drunk". Science 2.0. 25 Ağustos 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.Check date values in:
|access-date=(help) - ^ For references, see the extensive references and bibliography at the article on Cerebellar abiotrophy, linked at the beginning of this paragraph.
- ^ Mavroudis I.A.; Fotiou, DF; Adipepe, LF; Manani, MG; Njau, SD; Psaroulis, D; Costa, VG; Baloyannis, SJ (Kasım 2010). "Morphological changes of the human purkinje cells and deposition of neuritic plaques and neurofibrillary tangles on the cerebellar cortex of Alzheimer's disease". American Journal of Alzheimer's Disease & Other Dementias. 25 (7). ss. 585-91. doi:10.1177/1533317510382892. PMID 20870670.
- ^ Fekadu, Makonnen (27 Mart 2009). "Rabies encephalitis, Negri bodies within the cytoplasm of cerebellar Purkinje cell neurons". CDC/Frontal Cortex Inc. 26 Aralık 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Haziran 2013. Note: not peer-reviewed.
Dış bağlantılar
- Hücre Merkezli Veritabanı - Purkinje20 Temmuz 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- Beyincik bozuklukları 26 Ağustos 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- NİF Arama - Purkinje hücreleri ( 8 Temmuz 2013 tarihinde Wayback Machine sitesinde arşivlendi.Neuroscience Information Framework vasıtasıyla)
Konuyla ilgili yayınlar
- "Tetrodotoxin-resistant dendritic spikes in avian Purkinje cells". Proc. Natl. Acad. Sci. U.S.A. 73 (7). Temmuz 1976. ss. 2520-3. doi:10.1073/pnas.73.7.2520. PMC 430632 $2. PMID 1065905.
- "Electrophysiological properties of in vitro Purkinje cell somata in mammalian cerebellar slices". J. Physiol. Cilt 305. Ağustos 1980. ss. 171-95. doi:10.1113/jphysiol.1980.sp013357. PMC 1282966 $2. PMID 7441552. 13 Nisan 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Aralık 2017.
- "Voltage-dependent calcium conductances in mammalian neurons. The P channel". Ann. N. Y. Acad. Sci. 560 (1 Calcium Chann). 1989. ss. 103-11. doi:10.1111/j.1749-6632.1989.tb24084.x. PMID 2545128.
- Forrest, Michael (Ekim 2014). Biophysics and computations of the cerebellar Purkinje neuron. CreateSpace. ISBN 978-1502454546.