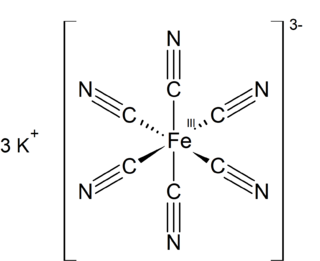
Prusya mavisi
 | |
| Adlandırmalar | |
|---|---|
Demir(II,III) hekzasiyanoferrat(II,III) | |
Diğer adlar
| |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.034.418 |
| EC Numarası |
|
| 1093743 | |
PubChem CID | |
| UNII | |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Kimyasal formül | C18Fe7N18 |
| Molekül kütlesi | 859,23 g mol−1 |
| Görünüm | Mavi opak kristaller |
| Çözünürlük (su içinde) | Çözünmez |
| Yapı | |
| Yüz-merkezli kübik, Pearson sembol cF43 | |
| Fm3m, No. 225[1] | |
| Farmakoloji | |
| V03AB31 (DSÖ) | |
| Ağızdan | |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
| Renk koordinatları | ||
|---|---|---|
| Hex | #003153 | |
| RGB | (r, g, b) | (0, 49, 83) |
| CMYK | (c, m, y, k) | ({{{c}}}, {{{m}}}, {{{y}}}, {{{k}}}) |
| HSV | (h, s, v) | (205°, 100%, 33%) |
Prusya mavisi (aynı zamanda Berlin mavisi veya yağlı boya tablolarda Parizyen veya Paris mavisi olarak bilinir), demir içeren ferrosiyanür tuzlarının oksidasyonu ile üretilen koyu mavi pigmenttir. FeIII4III4[FeII(CN)6]3 kimyasal formülüne sahiptir. Turnbull mavisi kimyasal olarak aynıdır ancak farklı reaktiflerden yapılmıştır ve çeşitli safsızlıklar nedeniyle rengi biraz farklıdır.
Prusya mavisi ilk modern sentetik pigmentti. Bileşik suda çözünmediği için çok ince kolloidal dispersiyon olarak hazırlanır. Değişken miktarlarda başka iyonlar[2] içerir ve görünüşü hassas şekilde kolloidal partiküllerin boyutuna bağlıdır.
Pigment boyalarda ve tasarım çizimlerinde kullanılan "geleneksel mavi"dir. 19. yüzyıl Japonca: aizuri-e (Japonca: 藍摺り絵) Japon tahta baskılarında öne çıkmıştır.
Tıpta, ağızdan uygulanan Prusya mavisi, örneğin talyum (I) ve sezyumun radyoaktif izotopları gibi bazı ağır metal zehirlenmelerine karşı panzehir olarak kullanılır. Bu tedavide, bileşiğin iyon değiştirme özelliklerinden ve belirli "yumuşak" metal katyonlar için çok yakınlıktan yararlanır.
Temel sağlık sisteminde ihtiyaç duyulan en önemli ilaçlar olan Dünya Sağlık Örgütü Temel İlaçlar listesindedir.[3] Prusya mavisi adını ondan türetilen prusik aside (hidrojen siyanür) vermiştir. Hidrojen siyanüre Almanca: Blausäure ("mavi asit") denir. Fransız kimyager Louis Joseph Gay-Lussac, Antik Yunan (Grekçe: kyanos, "mavi") kelimesinden gelen Prusya mavisi rengi nedeniyle adını Siyanür (İngilizce: cyanide) adını koydu.
Tarihçe

Prusya mavisi pigmenti, Mısır mavisinin sentezine ilişkin bilgi kaybının ardından yaygın olarak kullanılan ilk kararlı ve nispeten ışığa dayanıklı mavi pigment olması nedeniyle önemlidir. Avrupalı ressamlar daha önce çivit boyası, smalt ve Sur moru gibi bir dizi pigment ve Lapis lazuliden yapılan son derece pahalı ultramarin kullanmıştı. Aynı şekilde Japon ressamlar ve tahta baskı sanatçıları Avrupa'dan Prusya mavisi ithal etmeye başlayana kadar uzun ömürlü mavi pigmente erişemediler.[4]
Prusya mavisi Fe7(CN)18 (ayrıca (Fe4[Fe(CN)6]3·xH2O) muhtemelen ilk kez 1706 civarında Berlin'deki boya üreticisi Diesbach tarafından sentezlendi.[5] Çoğu tarihsel kaynak, Diesbach'ın ilk adından bahsetmez. Yalnızca Berger ondan Johann Jacob Diesbach olarak söz eder.[6] Pigmentin, Diesbach'ın kana bulanmış potasları kırmızı cochineal boya yapmak için kullandığında kazara oluştuğuna inanılır. Asıl boya potas, ferrik sülfat ve kurutulmuş kokineal gerektiriyordu. Bunun yerine kan, potas ve demir sülfat istenen kırmızı pigmentin aksine çok belirgin mavi renkli demir ferrosiyanür olarak bilinen bir bileşik oluşturmak için reaksiyona girdi.[7]
1709'da ilk tüccarı tarafından[8] Almanca: Preußisch blau ve Almanca: Berlinisch Blau olarak adlandırıldı.[9]
Pigment, pahalı Lapis lazulinin yerini aldı ve Johann Leonhard Frisch ile Prusya Bilimler Akademisi baskani Gottfried Leibniz arasında 1708 ile 1716 yılları arasında yazılan mektuplarda önemli bir konuydu.[9]
İlk kez 31 Mart 1708'de Frisch tarafından Leibniz'e yazılan bir mektupta bahsedilir. 1708'den sonra Frisch, pigmenti Avrupa'da tanıtmaya ve satmaya başladı. Ağustos 1709'da pigmente Preussisch blau adı verildi; Kasım 1709'da Almanca Berlinisch Blau adı ilk kez Frisch tarafından kullanıldı.
Frisch'in kendisi, mektuplarından anlaşılabileceği gibi, 1710'da Notitia Coerulei Berolinensis nuper inventi gazetesinde Prusya mavisinin bilinen ilk yayınının yazarıdır. Diesbach, yaklaşık 1701'den beri Frisch için çalışıyordu.

Bugüne kadar, Pieter van der Werff (Resim Galerisi, Sanssouci, Potsdam) tarafından 1709 tarihli Mesih'in Mezarı, Prusya mavisinin kullanıldığı bilinen en eski tablodur. 1710 civarında, Prusya sarayındaki ressamlar zaten pigment kullanıyordu. Aynı sıralarda, Prusya mavisi, Antoine Watteau ve daha sonra halefleri Nicolas Lancret ve Jean-Baptiste Pater'in resimlerinde kullandığı Paris'e geldi.[5][10] François Boucher, pigmenti hem maviler hem de yeşiller için yoğun bir şekilde kullandı.[11]
1731'de Georg Ernst Stahl, Prusya mavisinin ilk sentezini yayınladı.[12] Hikâye sadece Diesbach'ı değil, aynı zamanda Johann Konrad Dippel'i de içerir.
Diesbach, cochineal'den kırmızı göl pigmenti yaratmaya çalışıyordu ancak kullandığı kirli potas nedeniyle bunun yerine maviyi elde etti. Potas'ı hayvansal yağ üretmek için kullanan Dippel'den ödünç aldı. Bilinen başka hiçbir tarihsel kaynak bu bağlamda Dippel'den bahsetmez. Bu nedenle bugün bu hikâyenin güvenilirliğini yargılamak zordur. 1724'te tarif nihayet John Woodward tarafından yayınlandı.[13][14][15]
1752'de Fransız kimyager Pierre J. Macquer, Prusya mavisinin demir tuzunu ve boyayı sulandırmak için kullanılabilecek yeni bir aside indirgenebileceğini göstermek için önemli bir adım attı.[16] İlk olarak Prusya mavisinden saf biçimde yalıtılan ve 1782'de İsveçli kimyager Carl Wilhelm Scheele[17] tarafından tanımlanan yeni asite [[hidrojen siyanür|Almanca: Blausäure]] (Kelimesi kelimesine "mavi asit" demektir) adı verildi. Prusya mavisinden türetilmesi nedeniyle Prusik asit denildi.
Prusya mavisi yapma sürecinde oluşan renksiz anyon siyanür adını Yunanca lacivert kelimesinden almıştır.
1800'lerin sonlarında Radzin'nin Hasidik Rebbesi Haham Gershon Henoch Leiner, bunun gerçek techeiles boyası olduğuna inanarak tzitziyotu sepyadan yapılmış Prusya mavisi ile boyadı. Bazıları yapay üretimi nedeniyle techeiles kimliğini sorgulamış ve Haham Leiner'ın bunun farkında olsaydı boyasının techeiles olduğu pozisyonundan geri çekileceğini[18] iddia ettiler, diğerleri ise buna itiraz etti ve Haham Leiner'in geri çekilmeyeceğini iddia etti.[19]
18. yüzyılın başından itibaren Prusya mavisi, Prusya Ordusu'nun piyade ve topçu alaylarının giydiği baskın tek tip ceket rengiydi.[20] Almanca: Dunkelblau (koyu mavi), bu gölge ton sembolik önem kazandı ve Alman askerlerince, 1. Dünya savaşı bitene kadar törenlerde ve görev dışı durumlarda yeşilimsi gri sahra grisi (Almanca: Feldgrau) yerini alana kadar giyildi.[21]
Üretim
Prusya mavisi demir içeren ferrosiyanür tuzların oksidasyonu ile üretilir. Bu beyaz katıların M2Fe[Fe(CN)6] formülü vardır ki burada M+ = Na+ veya K+ 'dır. Bu malzemedeki demirin tamamı demir içerir dolayısıyla karışık değerlikle ilişkili derin renk yoktur. Bu beyaz katının hidrojen peroksit veya sodyum klorat ile oksidasyonu ferrisiyanürü üretir ve Prusya mavisi verir.[22]
"Çözünür" K[FeIIIFeII(CN)6] formu, gerçekten koloidal olan potasyum ferrosiyanür ve demirden (III) yapılabilir:
- K+ + Fe3+ + [FeII(CN)6]4- → KFeIII[FeII(CN)6]
Potasyum ferrisiyanür ve demirin (II) ‘nin benzer reaksiyonu, aynı koloidal çözelti ile sonuçlanır çünkü [FeIII(CN)6]3- ferrosiyanüre dönüştürülür.
Yukarıdaki reaksiyonlarda çok miktarda Fe3+ eklenirse "Çözünmez" Prusya mavisi üretilir:
- 4 Fe3+ + 3 [FeII(CN)6]4- → FeIII[FeIIIFeII(CN)6]3[23]
Siyanür tuzlarından hazırlanmış olmasına rağmen siyanür grupları demire sıkıca bağlı olduğu için Prusya mavisi zehirli değildir.[24] Diğer polimerik siyanometalatlar az zehirleyicililikle benzer şekilde değişmezdir.
Hem ferrosiyanür ((FeII(CN)6)4−) hem de ferrisiyanür ((FeIII(CN)6)3−), siyanür iyonlarına güçlü demir koordinasyonu nedeniyle özellikle kararlı ve zehirli olmayan polimerik siyanometalatlardır. Siyanür genel olarak krom gibi geçiş metalleriyle iyi bağlansa da, bu demir dışı koordinasyon bileşikleri demir siyanürler kadar kararlı değildir. Bu nedenle CN- iyonları salma riskini ve ardından karşılaştırmalı toksisiteyi artırır.[25]
Turnbull mavisi

Eskiden ferrisiyanür çözeltisine demir (II) tuzlarının eklenmesinin Prusya mavisinden farklı bir malzeme verdiği düşünülürdü. Ürün geleneksel olarak Turnbull mavisi (TM) olarak adlandırıldı. X-ışını kırınımı ve elektron kırınımı yöntemleri, PM ve TM yapılarının aynı olduğunu göstermiştir.[26][27] TM ve PM için renklerdeki farklılıklar, parçacık boyutunu ve safsızlık içeriğini güçlü şekilde etkileyen çökeltme yöntemlerindeki ince farklılıkları yansıtır.
Özellikleri
Prusya mavisi, mikrokristalin mavi bir tozdur. Çözünmez ancak kristalitler bir kolloid oluşturma eğilimindedir. Bu tür kolloidler ince filtrelerden geçebilir.[2]
Bilinen en eski sentetik bileşiklerden biri olmasına rağmen, Prusya mavisinin bileşimi yıllarca belirsizliğini korudu. Kesin tanımlanması üç faktör nedeniyle karmaşıktı:
- Prusya mavisi hiç çözünmez ancak aynı zamanda kolloidler oluşturma eğilimindedir.
- Geleneksel sentezler saf olmayan bileşikler sağlama eğilimindedir
- Saf Prusya mavisi bile yapısal olarak karmaşıktır ve sıradan kristalografik analizlere meydan okur.
Kristal yapı
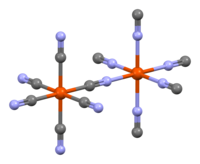
Çözünmeyen Prusya mavisinin kimyasal formülü Fe7(CN)18 . xH2O'dir. Burada x = 14–16'dır.
Yapısı, IR spektroskopisi, Mössbauer spektroskopisi, X-ışını kristalografisi ve nötron kristalografisi kullanılarak belirlendi.
X- ışını kırınımı, demir gibi daha ağır elementlerin varlığında karbonu azottan kolayca ayırt edemediğinden, bu daha hafif elementlerin konumu, spektroskopik yöntemlerle ve ayrıca demir atomu merkezlerinden mesafeleri gözlemlenerek çıkarılır.

PM, kübik kafes yapılıdır. Çözünür PM kristalleri, ara K+ iyonları içerir; çözünmeyen PM, bunun yerine dokular arası suya sahiptir. İdeal çözünmeyen PM kristallerinde, kübik çerçeve Fe(II) –karbon mesafesi 1,92 Å ve Fe (III) –nitrojen uzaklıkları 2,03 Å olacak şekilde Fe (II)–C–N–Fe (III) dizilerinden oluşturulur. Fe(CN)6 alt birimlerin yerlerinin dörtte biri boştur ve bu tür üç grup kalır. Boş azot yerleri bunun yerine Fe (III) 'e koordine edilen su molekülleri ile doldurulur.

Alçak devirli Fe (ll) merkezleri sekizyüzlü biçimde altı karbon ligandlarıyla çevrilidir. Yüksek devirli Fe (III) merkezleri sekizyüzlü(oktahedral) olarak ortalama 4,5 azot atomu ve 1,5 oksijen atomu (koordine edilmiş altı su molekülünden gelen oksijen) ile çevrilidir. Birim hücrede, yalıtılmış moleküller veya koordineli suya bağlı hidrojen olarak ek sekiz (interstisyel) su molekülü vardır.
Bileşim, kafes kusurlarının varlığından ötürü herkesin bildiği gibi değişkendir ve su molekülleri, katyon boşluklarını doldurmak için yapıya dahil edildiğinden çeşitli derecelerde hidratlanmasına izin verir. Prusya mavisinin bileşiminin değişkenliği düşük çözünürlüğüne atfedilebilir, bu ise katı ve sıvı arasında tam dengeye ulaşmak için zaman olmadan hızlı çökelmesine yol açar.[28][29]
Renk
Prusya mavisi güçlü renklidir ve yağlı boyalarla karıştırıldığında siyah ve koyu maviye yönelir. Kesin renk, partikül boyutunu belirleyen hazırlama yöntemine bağlıdır. Prusya mavisinin yoğun mavi rengi, elektronların Fe (II)'den Fe (III)'e transferinin enerjisi ile ilişkilidir. Bu tür karışık değerlikli bileşiklerin çoğu, aralıklı yük transferinden kaynaklanan görünür ışığın belirli dalga boylarını emer.Bu durumda dalga boyunda 680 nanometre civarında turuncu-kırmızı ışık emilir ve sonuçta yansıyan ışık mavi olarak görünür.
Çoğu yüksek kroma pigmentleri gibi Prusya mavisi bilgisayar ekranında doğru şekilde görüntülenemez. PM indirgenme ile maviden renksize değişir yani ise elektrokromiktir. Bu değişikliğin nedeni Prusya mavisinin rengine neden olan aralık yük transferinin ortadan kaldırılmasıyla oluşan Fe (III)'ün Fe (II)'ye indirgenmesidir.
Kullanım
Pigment
Prusya mavisi, kolay yapıldığı, ucuzluğu, zehirsizliği ve yoğun renkliliği nedeniyle pek çok uygulamada kullanılır. Buluşundan hemen sonra pigment olarak benimsendi ve neredeyse hemen her yağlı boya, sulu boya ve boyamada yaygın olarak kullanıldı.[30] Baskın olarak pigmentlerde kullanılır: siyah ve mavimsi mürekkeplerde kullanılmak üzere yılda yaklaşık 12,000 ton Prusya mavisi üretilir. Diğer çeşitli pigmentler de bu malzemeyi içerir.[22] Mühendis mavisi ve siyanotipler üzerinde oluşan pigment, onlara ortak isim taslaklarını verir. Bazı boya kalemleri bir zamanlar Prusya mavisi ile boyandı (daha sonra gece mavisi olarak yeniden etiketlendi). Aynı zamanda boyalarda popüler bir pigmenttir. Benzer şekilde Prusya mavisi çamaşırı mavileştirmenin temelidir.
Avrupa Birliği Nanomalzemeler Gözlemevi'ne göre, Prusya mavisinin nanopartikülleri bazı kozmetik bileşenlerinde pigment olarak kullanılmaktadır.
İlaç
Prusya mavisinin tek değerlikli metalik katyonları (Me+) dahil etme yeteneği, belirli toksik ağır metallerin ayırma maddesi olarak yararlı yapar. Farmasötik dereceli Prusya mavisi, özellikle talyum (Tl+) veya radyoaktif sezyum (134Cs+,137Cs+) yutmuş kişiler için kullanılır. Uluslararası Atom Enerjisi Ajansı'na (IAEA) göre yetişkin bir erkek ciddi bir zarar görmeden günde en az 10 gram Prusya mavisi yiyebilir.
ABD Gıda ve İlaç Dairesi (FDA), bazı zehirlenme vakalarında "500 mg Prusya mavisi kapsüllerin, onaylı Yeni İlaç Başvuru koşullarında üretildiğinde güvenli ve etkili tedavi bulunabileceğini" belirlemiştir.[31][32]
Radyogardaz (çözünür kapsüllerdeki Prusya mavisi[33]), 137Cs+ 'nin (sezyum-137) enterohepatik dolaşımına müdahale ederek 137Cs+ 'nin bağırsaktan, dolayısıyla kan dolaşımından çıkarılması için kullanılan ticari bir üründür.[34] Dahili kalma (ve maruz kalma) süresini yaklaşık üçte iki oranında azaltır.[2]
Goiânia kazasında zehirlenenlerden 137Cs+ 'i emmek için özellikle kullanıldı.
Demir lekesi
Prusya mavisi, kemik iliği örneklerinde olduğu gibi biyopsi örneklerinde demir varlığını saptamak için patologlar tarafından çok yaygın kullanılan bir histopatoloji boyasıdır.
Mucidi Alman patolog Max Perls'den (1843-1881) sonra "Perls Prusya mavisi " denilen asıl boyanın formülü dokuyu boyamak için ayrı ayrı potasyum ferrosiyanür ve asit çözeltileri kullandı (bunlar artık tam boyamadan önce birlikte kullanılır).
Dokudaki demir birikintileri daha sonra yerinde mor Prusya mavisi boyasını boyar ve mavi veya mor tortular olarak görselleştirilir.[35]
 Histopatoloji, lipofusin pigmentli bir hepatositin yanında önemli hemosiderin birikimi olan bir Kupffer hücresi'ni göstermektedir. H&E lekesi.
Histopatoloji, lipofusin pigmentli bir hepatositin yanında önemli hemosiderin birikimi olan bir Kupffer hücresi'ni göstermektedir. H&E lekesi.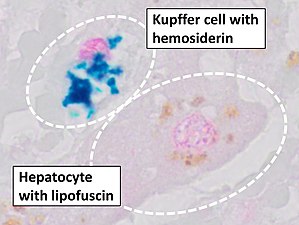 Hemosiderin pigmentini mavi olarak vurgulayan Prusya mavisi boyama.
Hemosiderin pigmentini mavi olarak vurgulayan Prusya mavisi boyama. Prusya mavisi lekeleri
Prusya mavisi lekeleri
Makineciler ve kalıpçılar tarafından kullanılşı
Yağ esaslı Prusya mavisi Mühendis Mavisi, yüzey plakalarını ve elle kazımada yatak vb metal yüzeyleri düzeltmekte kullanılan geleneksel bir malzemedir. Referans yüzeye ince bir kat, kurumayan macun sürülür ve iş parçasının pürüzlü yerlerine aktarılır. Daha sonra kalıpçı işaretlenmiş pürüzlü yerleri eğeleyerek, taşlayarak vb şekilde düzeltir. Prusya mavisi, birçok zemin pigmentinin yapabileceği gibi çok hassas referans yüzeylerini aşındırmayacağından tercih edilir.
Analitik kimyada kullanılışı
Prusya mavisi, toplam fenoller için Prusya mavisi testinde oluşturulur. Örneklere ve fenolik standartlara asidik ferrik klorür ve fenoller tarafından ferrosiyanüre indirgenen ferrisiyanür verilir. Demir klorür ve ferrosiyanür reaksiyona girerek Prusya mavisi oluşturur. 700 nm'de numunelerin emilimin standartlara karşılaştırılması, toplam fenol veya polifenollerin belirlenmesine izin verir.[36][37]
Evde kullanımı
Prusya mavisi Mrs. Stewart's Bluing gibi bazı çamaşır mavileştirme preperatlarında vardır.[38]
Pil malzemeleri
Prusya mavisi (PM), elektrokimyasal enerji depolama ve dönüştürme uygulamaları için 1978'den beri incelenmektedir.[39] Elektrokimyasal aktif Prusya mavisi benzeri oluşturmak için PM'deki Fe metal merkezlerini Mn, Co, Ni, Zn, vb. gibi farklı metal iyonlarıyla değiştirmek mümkündür. PM/PM benzerleri ve türevleri, lityum-iyon pil, sodyum iyon pil ve potasyum-iyon pil'de tersinir alkali iyon ekleme ve çıkarma için elektrot malzemeleri olarak kullanılabilir.
Ayrıca bakınız
- Kobalt mavisi - Mavi pigment
- Kristal viyole – Histolojik leke olarak ve Gram'ın bakterileri sınıflandırma yönteminde kullanılan triarilmetan boya
- Han moru ve Han mavisi – Çinde geliştirilen Sentetik baryum bakır silikat pigmentleri
- Gece mavisi– Mavinin koyu tonu
Dış bağlantılar
- FDA'nın Prusya mavisi sayfası 10 Temmuz 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- CDC'nin Prusya mavisi sayfası
- Ulusal Kirletici Envanteri - Siyanür bileşikleri bilgi formu
- Heyltex Corporation Radiogardase distribütörleri (Prusya mavisi çözünmez kapsüller) 21 Şubat 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- Sarah Lowengard, The Creation of Color in Eighteenth Century Europe Columbia University Press, 2006'da "Prusya Mavisi" 31 Ocak 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- Prusya mavisi 2 Ocak 2016 tarihinde Wayback Machine sitesinde arşivlendi., ColourLex
- Kraft (2008). "On the discovery and history of Prussian blue" (PDF). Bulletin for the History of Chemistry. 33 (2): 61-67. 17 Mayıs 2017 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 16 Nisan 2021.
Kaynakça
- ^ International Tables for Crystallography, Vol. A (2016 bas.). ISBN 978-0-470-68575-4.
- ^ a b c Chemistry of Transition Metal Cyanide Compounds: Modern Perspectives. Progress in Inorganic Chemistry. 45. 1997. ss. 283-391. doi:10.1002/9780470166468.ch4. ISBN 9780470166468.
- ^ "WHO Model List of Essential Medicines" (PDF). World Health Organization. October 2013. 23 Nisan 2014 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 22 Nisan 2014.
- ^ The Secret Lives of Colour. Londra: John Murray. 2016. ss. 189-191. ISBN 9781473630819. OCLC 936144129.
- ^ a b Bartoll, Jens. "The early use of prussian blue in paintings" (PDF). 9th International Conference on NDT of Art, Jerusalem Israel, 25–30 May 2008. 20 Eylül 2009 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 22 Ocak 2010.
- ^ Berger, J. E. (c.1730) Kerrn aller Fridrichs=Städtschen Begebenheiten. Staatsbibliothek zu Berlin – Preußischer Kulturbesitz, Handschriftenabteilung, Ms. Boruss. quart. 124.
- ^ Finlay, Victoria (2014). The Brilliant History of Color in Art. J. Paul Getty Museum. ss. 86-87. ISBN 978-1606064290.
- ^ The Brilliant History of Color in Art. J. Paul Getty Museum. 2014. ss. 86-87. ISBN 978-1606064290.
- ^ a b Frisch, J. L. (1896) Briefwechsel mit Gottfried Wilhelm Leibniz L. H. Fischer (ed.), Berlin, Stankiewicz Buchdruck, reprint Hildesheim/New York: Georg Olms Verlag, 1976
- ^ Bartoll, J. (2007). "Early Prussian Blue. Blue and green pigments in the paintings by Watteau, Lancret and Pater in the collection of Frederick II of Prussia". Techné. 25: 39-46. 16 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Nisan 2021.
- ^ Mulherron (2001). "Prussian Blue, Boucher and Newton: the Material, Practice and Theory of Rococo painting". Object. no. 3: 68-93. 16 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Nisan 2021.
- ^ Stahl, G. E. (1731) Experimenta, Observationes, Animadversiones CCC Numero, Chymicae et Physicae. Berlin. pp. 281–283 16 Nisan 2021 tarihinde Wayback Machine sitesinde arşivlendi..
- ^ Woodward, J. (1724–1725). "Praeparatio coerulei Prussiaci es Germanica missa ad Johannem Woodward." [Preparation of Prussian blue sent from Germany to John Woodward...]. Philosophical Transactions of the Royal Society of London. 33 (381): 15-17. doi:10.1098/rstl.1724.0005.
- ^ Brown, John (1724–1725). "Observations and Experiments upon the Foregoing Preparation". Philosophical Transactions. 33 (381): 17-24. doi:10.1098/rstl.1724.0006. 16 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Nisan 2021.. The recipe was subsequently published in Geoffroy, Étienne-François (1727) "Observations sur la Preparation de Bleu de Prusse ou Bleu de Berlin," Mémoires de l'Académie royale des Sciences année 1725. Paris. pp. 153–172.
- ^ Lowengard, Sarah (2008) Chapter 23: Prussian Blue 31 Ocak 2020 tarihinde Wayback Machine sitesinde arşivlendi. in The Creation of Color in Eighteenth-Century Europe. New York, New York: Columbia University Press. 0231124546.
- ^ Macquer, Pierre-Joseph (1752) "Éxamen chymique de bleu de Prusse," 15 Mart 2021 tarihinde Wayback Machine sitesinde arşivlendi. Mémoires de l'Académie royale des Sciences année 1752 ... (Paris, 1756), pp. 60–77. This article was reviewed in "Sur le bleu de Prusse," 18 Nisan 2021 tarihinde Wayback Machine sitesinde arşivlendi. Histoire de l'Académie royale des Sciences... (1752), (Paris, 1756), pp. 79–85.
- ^ Scheele, Carl W. (1782) "Försök, beträffande det färgande ämnet uti Berlinerblå" 15 Mart 2021 tarihinde Wayback Machine sitesinde arşivlendi. (Experiment concerning the coloring substance in Berlin blue), Kungliga Svenska Vetenskapsakademiens handlingar (Royal Swedish Academy of Science's Proceedings), 3: 264–275 (in Swedish). Reprinted in Latin as: "De materia tingente caerulei berolinensis" 15 Mart 2021 tarihinde Wayback Machine sitesinde arşivlendi. in: Carl Wilhelm Scheele with Ernst Benjamin Gottlieb Hebenstreit (ed.) and Gottfried Heinrich Schäfer (trans.), Opuscula Chemica et Physica (Leipzig ("Lipsiae"), (Germany): Johann Godfried Müller, 1789), vol. 2, pages 148–174.
- ^ bkz. Tekhelet#Sepia officinalis
- ^ "Has the long lost chilazon, source of the biblical blue techeiles dye been rediscovered?". 8 Nisan 2008. 8 Nisan 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Mayıs 2020.
- ^ Haythornthwaite, Philip (1991) Frederick the Great's Army – Infantry. Bloomsbury USA. p. 14. 1855321602
- ^ Bull, Stephen (2000) World War One: German Army. Brassey's. pp. 8–10. 1-85753-271-6
- ^ a b Völz, Hans G. et al. (2006) "Pigments, Inorganic" in Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim. DOI:10.1002/14356007.a20_243.pub2.
- ^ Egon Wiberg, Nils Wiberg, Arnold Frederick Holleman: Inorganic chemistry 16 Nisan 2021 tarihinde Wayback Machine sitesinde arşivlendi., p. 1444. Academic Press, 2001; Google books
- ^ Journal of Toxicology, Suicide Attempt by Ingestion of Potassium Ferricyanide
- ^ Jonathan R. Thurston, Scott E. Waters, Brian H. Robb, Michael P. Marshak (March 2022). "Organic and Metal-Organic RFBs". Encyclopedia of Energy Storage. 2: 423-435. doi:10.1016/B978-0-12-819723-3.00082-2. ISBN 9780128197301.
- ^ Ozeki (1984). "Photoacoustic spectra of prussian blue and photochemical reaction of ferric ferricyanide". Analytical Chemistry. 56 (14): 2819. doi:10.1021/ac00278a041.
- ^ Izatt (1970). "Calorimetric study of Prussian blue and Turnbull's blue formation". Inorganic Chemistry. 9 (9): 2019. doi:10.1021/ic50091a012. 16 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Nisan 2021.
- ^ a b Kaynak hatası: Geçersiz
<ref>etiketi;Herrenisimli refler için metin sağlanmadı (Bkz: ) - ^ Lundgren (1988). "Observations on the composition of Prussian blue films and their electrochemistry". Inorganic Chemistry. 27 (5): 933. doi:10.1021/ic00278a036.
- ^ Berrie, Barbara H. (1997). "Prussian Blue". In Artists' Pigments. A Handbook of their History and Characteristics, E. W. FitzHugh (ed.). Washington, DC: National Gallery of Art. 0894682563.
- ^ "Questions and Answers on Prussian Blue". 10 Temmuz 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Mart 2020.
- ^ "Questions and Answers on Calcium-DTPA and Zinc-DTPA (Updated)". U.S. Food & Drug Administration. 21 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Mart 2020.
- ^ Radiogardase: Package insert with formula 20 Mart 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Heyltex Corporation – Toxicology 12 Kasım 2007 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Formula for Perls Prussian blue stain 20 Ağustos 2020 tarihinde Wayback Machine sitesinde arşivlendi.. Accessed April 2, 2009.
- ^ "Tannin Chemistry" (PDF). 26 Ağustos 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 19 Aralık 2009. (1.41 MB)Accessed December 19, 2009
- ^ Stabilization of the Prussian blue color in the determination of polyphenols. Horace D. Graham, J. Agric. Food Chem., 1992, volume 40, issue 5, pages 801–805, DOI:10.1021/jf00017a018
- ^ "The Right Chemistry: Columbo, your laundry and liquid bluing". Montreal Gazette. 22 Ocak 2016. 11 Eylül 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Şubat 2017.
- ^ Neff, Vernon D. (1 Haziran 1978). "Electrochemical Oxidation and Reduction of Thin Films of Prussian Blue". Journal of the Electrochemical Society (İngilizce). 125 (6): 886-887. Bibcode:1978JElS..125..886N. doi:10.1149/1.2131575. ISSN 1945-7111. 11 Mayıs 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Mayıs 2023.