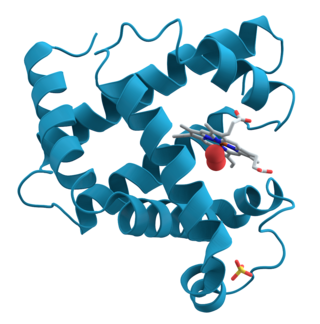
Proteinler, bir veya daha fazla uzun amino asit artık zincirini içeren büyük biyomoleküller ve makromolekül'lerdir. Proteinler organizmalar içinde, hücrelere yapı ve organizmalar sağlayarak ve molekülleri bir konumdan diğerine taşıyarak metabolik reaksiyonları katalizleme, DNA kopyalama, uyaranlara yanıt verme dahil olmak üzere çok çeşitli işlevler gerçekleştirir. Proteinler, genlerinin nükleotit dizisi tarafından dikte edilen ve genellikle faaliyetini belirleyen özel 3D yapıya protein katlanmasıyla sonuçlanan amino asit dizilimlerinde birbirlerinden farklıdır.
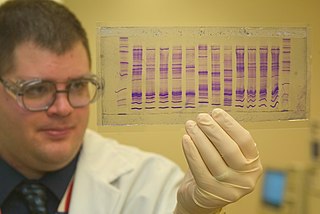
DNA dizilemesi, bir DNA molekülündeki nükleotit bazlarının sırasının belirlenmesidir.
Biyolojide dizi analizi bir DNA veya protein dizisini bir bilgisayar kullanarak, biyoenformatik yöntemlerle incelenmesidir. Dizi analizi ana hatlarıyla aşağıdaki konuları kapsar:
- İki veya daha çok dizinin karşılaştırılarak benzerliklerini bulunması
- Bir dizinin içinde belli özelliğe sahip nokta veya bölgelerin bulunması. Örneğin, dizi motifleri, okuma çerçeveleri, intron ve ekson sınırları ve gen düzenleyici elemanlar.
- Genom haritalaması
- Homolog dizilerin karşılaştırılarak filojenik ağaç kurmak.
- Protein yapı tahmini

Protein fosforilasyonu, bir proteine bir fosfat grubu (PO4) eklenmesidir. Protein fosforilasyonu pek çok hücresel süreçte önemli bir rol oynar.

Gen ifadesinin düzenlenmesi ya da gen ifadesinin denetimi, hücrelerin ve virüslerin genlerindeki bilgiyi gen ürünlerine çevirmesini kapsayan süreçler için kullanılan bir terimdir. İşlevsel bir genin ürünleri RNA veya protein olabilir; bilinen mekanizmaların en temeli protein kodlayan genlerin düzenlenmesidir. Gen ifadesinin, DNA-RNA transkripsiyonundan, proteinin translasyon sonrası değişimlerine kadar olan herhangi bir adımı değiştirilip, ayarlanabilmektedir.
Biyoenformatikte dizi hizalaması, DNA, RNA veya protein dizilerini düzenleyerek benzer bölgelerin tespit edilmesidir. Bu bölgelerin benzer olması, diziler arasında işlevsel, yapısal veya evrimsel bir ilişki olduğu anlamına gelir. Hizalanmış nükleotit veya aminoasit kalıntı dizileri tipik olarak bir matriksin satırları olarak gösterilir. Kimyasal kalıntıları temsil eden harflerin arasına boşluklar konarak ardışık sütunlarda yer alan aynı veya benzer harflerin bir hizada olması sağlanır.
Protein saflaştırması, karmaşık bir karışımdan tek bir tip proteini izole etmek için izlenen bir seri süreçtir. İlgi duyulan bir proteinin işlevi, yapısı ve diğer proteinlerle etkileşiminin karakterizasyonu için protein saflaştırması şarttır. Başlangıç malzemesi genelde bir biyolojik doku veya mikrobiyal kültürdür. Saflaştırma sürecinin çeşitli adımları sonucunda, protein içinde hapsolduğu ortamdan kurtarılır, karışımda bulunan protein olan ve protein olmayan kısımlar birbirinden ayrılır ve nihayet arzulanan protein tüm diğer proteinlerden ayrıştırılır. Bir proteinin diğer tüm proteinlerden ayrıştırmak, protein saflaştırmasının en zahmetli yanıdır. Ayrıştırma adımlarında proteinlerdeki büyüklük, fizikokimyasal özellikler, bağlanma afinitesi ve biyolojik etkinlik gibi unsurlardaki farklılıklardan yararlanılır.

Peptit ve proteinlerin birincil yapısı, bu moleküllerin yapı birimleri olan amino asitlerin doğrusal sırası veya daha genel olarak, bir proteini oluşturan atomlar arasındaki kovalent bağların spesifikasyonudur.

Kütle spektrometrisi, İngilizce: Mass spectrometry (MS), kimyasal türleri iyonize edip oluşan iyonları Kütle-yük oranını esas alarak sıralayan bir analitik teknik. Daha basit terimler ile, bir kütle spektrumu bir numunen içindeki kütleleri ölçer. Kütle spektrometrisi birçok farklı alanda kullanılır ve kompleks karışımlara uygulandığı kadar saf numunelere de uygulanır.

Matthias Mann, kütle spektrometrisi ve proteomik alanlarında çalışan bilim insanı.

Kütle spektrometrisinde, matris destekli lazer desorpsiyon/iyonizasyonu (MALDI), minimum parçalanma ile büyük moleküllerden iyonlar oluşturmak için bir lazer enerjisi emici matris kullanan bir iyonizasyon tekniğidir. Daha geleneksel iyonizasyon yöntemleriyle iyonize edildiğinde kırılgan olma ve parçalanma eğiliminde olan biyomoleküllerin ve büyük organik moleküllerin analizinde uygulanmıştır. Gaz fazında büyük moleküllerin iyonlarını elde etmenin nispeten yumuşak bir yolu olması bakımından elektrosprey iyonizasyonuna (ESI) benzer, ancak MALDI tipik olarak çok daha az sayıda çok-yüklü iyon üretir.

Protein kütle spektrometrisi, kütle spektrometrisinin proteinlerin incelenmesine uygulanmasını ifade eder. Kütle spektrometrisi, proteinlerin doğru kütle tespiti ve karakterizasyonu için önemli bir yöntemdir ve birçok kullanımı için çeşitli yöntemler ve araçlar geliştirilmiştir. Uygulamaları arasında proteinler ve translasyon sonrası modifikasyonlarının tanımlanması, protein komplekslerinin, alt birimlerinin ve fonksiyonel etkileşimlerinin aydınlatılması veproteomikteki proteinlerin küresel ölçümü yer alır. Aynı zamanda proteinlerin çeşitli organellerdeki konumlarını belirlemek ve farklı proteinler ile membran lipidleri arasındaki etkileşimleri belirlemek için de kullanılabilir.
Kütle spektrometrisinde, de novo peptid dizilimi, bir peptid amino asit dizisinin ardışık kütle spektrometrisinden belirlendiği yöntemdir.
Biyo-bilişimde, bir peptid kütle parmak izi veya peptid kütle haritası, analiz edilen sindirilmiş bir proteinden gelen bir peptit karışımının bir kütle spektrumudur. Kütle spektrumu, proteini tanımlamaya hizmet edebilecek bir model olması anlamında bir parmak izi görevi görür. 1993 yılında geliştirilen peptid kütle parmak izi oluşturma yöntemi, bir proteinin izole edilmesinden, onu tek tek peptitlere ayrıştırılmasından ve bir tür kütle spektrometresi aracılığıyla peptitlerin kütlelerinin belirlenmesi adımlarından oluşur. Bir kez oluşturulduktan sonra, bir peptit-kütle parmak izi, ilgili protein ve hatta genomik diziler için veri tabanlarında arama yapmak için kullanılabilir. Bu da ilgili proteini kodlayan genlerin açıklanması için bu tekniği güçlü bir araç haline getirir.

Peptid kütle parmak izi alma, protein tanımlama için analitik bir tekniktir, burada ilgilenilen bilinmeyen protein ilk olarak daha küçük peptitlere bölünür ve bunların mutlak kütleleri MALDI-TOF veya ESI-TOF gibi bir kütle spektrometresi ile doğru bir şekilde ölçülebilir. Yöntem, 1993 yılında birkaç grup tarafından bağımsız olarak geliştirildi. Peptit kütleleri, bilinen protein dizilerini içeren bir veritabanı veya hatta genom ile karşılaştırılır. Bu, organizmanın bilinen genomunu proteinlere çeviren, daha sonra teorik olarak proteinleri peptidlere ayıran ve her bir proteinden peptidlerin mutlak kütlelerini hesaplayan bilgisayar programları kullanılarak sağlanır. Daha sonra, bilinmeyen proteinin peptitlerinin kütleleri, genomda kodlanmış her bir proteinin teorik peptit kütleleri ile karşılaştırılır. En iyi eşleşmeyi bulmak için sonuçlar istatistiksel olarak analiz edilir.
Alt-üst proteomik, kütle spektrometresi ile analizden önce proteinlerin proteolitik sindirim aracılığı ile proteinleri tanımlamak, amino asit dizilerini ve translasyon sonrası modifikasyonlarını karakterize etmek için yaygın kullanılan bir yöntemdir. Proteomikte kullanılan bu yönteme alternatif olarak mevcüt başlıca iş akışına üst-alt proteomik denir; bu yöntemde yekpare haldeki proteinler sindirim ve/veya parçalanmadan önce kütle spektrometresi içinde veya 2D elektroforez ile saflaştırılır. Esasen, alt-üst proteomik, belirli bir hücre, doku vb. numunenin protein yapısını belirlemenin nispeten basit ve güvenilir bir yoludur.
Kütle spektrometrisi, iyonların kütle-yük oranını ölçmek için bilimsel bir tekniktir. Genellikle gaz veya sıvı kromatografisi gibi kromatografik tekniklerle birleştirilir ve küçük molekülleri ve proteinleri (proteomik) tanımlamak ve karakterize etmek için kullanılabileceği analitik kimya ve biyokimya alanlarında yaygın olarak benimsenmiştir. Tipik bir kütle spektrometrisi deneyinde üretilen büyük hacimli veriler, bilgisayarların veri depolama ve işleme amacıyla kullanılmasını gerektirir. Yıllar içinde, farklı kütle spektrometre üreticileri, bu tür verileri işlemek için çeşitli özel veri formatları geliştirdiler ve bu da akademik bilim adamlarının verilerini doğrudan değiştirmelerini zorlaştırıyor. Bu sınırlamayı gidermek ve kamu sektöründe veri manipülasyonunu ve yeniliği kolaylaştırmak için yakın zamanda birkaç açık, XML tabanlı veri formatı geliştirilmiştir.

Elektron transfer ayrışması, ardışık kütle spektrometrisinin (MS/MS) aşamaları arasında bir kütle spektrometresinde çok yüklü gaz makromoleküllerin parçalanmasına yönelik bir yöntemdir. Elektron yakalama ayrışmasına benzer şekilde ETD, büyük, çok yüklü katyonların parçalanmasına onlara elektronlaraktararak neden olur. ETD, dizi analizi için polimerler, proteinler ve peptidler gibi biyolojik moleküller ile yaygın olarak kullanılır. Bir elektronun aktarılması, peptid omurgasının c- ve z-iyonlarına bölünmesine neden olurken, translasyon sonrası modifikasyonlar değişmez. Teknik yalnızca daha yüksek yük sahibi peptid veya polimer iyonları (z>2) için iyi çalışır. Bununla birlikte, çarpışmaya bağlı ayrışmaya (CID) göre ETD, daha uzun peptitlerin veya hatta proteinlerin tümünün parçalanması açısından avantajlıdır. Bu durum, tekniği üst-alt proteomik için önemli kılar. Yöntem, Virginia Üniversitesi' nden Hunt ve arkadaşları tarafından geliştirildi.

2-DE veya 2-D elektroforez olarak kısaltılan iki boyutlu jel elektroforezi, proteinleri analiz etmek için yaygın olarak kullanılan bir jel elektroforezi biçimidir. Protein karışımları, 2D jellerde iki boyutta iki özellik ile ayrılır. 2-DE ilk olarak 1975 yılında O'Farrell ve Klose tarafından bağımsız olarak rapor edildi.

Analiz, karmaşık bir konuyu veya maddeyi daha iyi anlamak için daha küçük parçalara ayırma sürecidir. Teknik, matematik ve mantık çalışmalarında Aristoteles'ten önce uygulanmıştır.













