Alkali metaller periyodik tablonun birinci grubunda yer alan metallerdir. Fransiyum dışında hepsi, yumuşak yapıda ve parlak görünümdedir.

Potasyum, bir kimyasal elementtir. Simgesi K ve atom numarası 19 dur. Potasyum adını izole edildiği Potas olarak da bilinen potasyum karbonattan almıştır. Potasyum yumuşak, gümüş-beyaz renkli alkali bir metaldir. Doğada deniz suyunda ve pek çok mineralde diğer elementlere bağlı olarak bulunur. Havada hızla oksitlenir ve suya karşı da çok aktiftir. Potasyum, pek çok açıdan sodyuma kimyasal olarak benzese de yaşayan organizmalarda, özellikle de hayvan hücrelerinde, sodyumdan farklı muamele görür. Kandaki seviyesinin düşük olmasına hipokalemi, yüksek olmasına hiperkalemi denir.

Lityum, sembolü Li atom numarası 3 olan kimyasal elementtir. Periyodik tabloda 1. grupta alkali metal olarak bulunur ve yoğunluğu en düşük olan metaldir. Lityum, yüksek reaktifliğinden dolayı doğada saf hâlde bulunmaz. Yumuşak ve gümüşümsü beyaz metaldir. Havada bulunan oksijenle reaksiyona giren lityum, lityum oksit (Li2O) oluşturur. Bu oksitlenme reaksiyonunu engellemek için yağ içinde saklanır. Hava ve su tarafından hızlı bir şekilde oksitlenip kararır ve lekelenir. Lityum metali doldurulabilir pillerde (örnek olarak cep telefonu ve kamera pili) ve ağırlığa yüksek direniş göstermesi sebebiyle alaşım olarak hava taşıtlarında kullanılır. Li+ iyonunun nörolojik etkilerinden dolayı, lityumlu bileşikler farmakolojik olarak sakinleştiricilerde kullanılır.
Turnusol kâğıdı, kimyada kullanılan ayıraçlardan bir tanesidir. Çözeltilerdeki asit ve bazları ayırt etmekte kullanılır. Turnusol, asitle temas ettiğinde kırmızı, bazla temas ettiğinde mavi renk verir. Turnusol belirli likenlerden (kuzukulağı) elde edilen, içeriğinde orsein bulunan ve suda çözünen bir boyadır. Çözelti olarak veya bir filtre kâğıdına emdirilerek kullanılır. Bu kâğıda pH belirteci denir ve maddelerin asitliğini ölçmek için kullanılır. Mavi turnusol kâğıdı asidik ortamlarda kırmızıya ve kırmızı turnusol kâğıdı bazik ortamlarda maviye döner. Renk değişimi 4,5-8,3 pH aralığında menekşe tonlarında olur (25 °C'de). Turnusolün aktif maddesi eritrolitmindir. Düşük pH değerli maddeler asit olarak ve yüksek değerliler alkali olarak adlandırılır. Sadece asit ve bazlar değil, bazı çözünen tuzlar da turnusol kâğıdını mavi veya kırmızıya dönüştürür. Kuvvetli asit ve zayıf bazdan oluşan tuzlar asidik, zayıf asit ve kuvvetli bazdan oluşan tuzlar bazik özellik gösterdiğinden turnusolü boyarlar (hidroliz).

Potasyum nitrat, formülü KNO3 olan bir potasyum bileşiğidir. Güherçile olarak da bilinen bileşik doğal hâlde kayaçlarda ve mağaralarda oluşan beyaz renkli kabuksu yapıda bulunur.

Kristalleştirme veya kristalizasyon, katı bir maddenin uygun bir çözücü içinde çözünmesi sonrasında çöktürülmesi yoluyla katı ve sıvı fazlarının birbirinden ayrılmasını sağlayan işlem.
Saf su, laboratuvarlarda kullanılan su; organik ve inorganik maddelerden arındırılmış damıtık (distile).

Potasyum hidroksit ya da potasyum hidrat bir kimyasal bileşik. Akkor derecede uçucu olan, 360 °C'de eriyen, suda ısı açığa çıkararak çözünen, beyaz renkte katı bir maddedir. Alkalik bir baz olan potasyum hidroksidin geniş bir kullanım alanı vardır. Endüstride arap sabunu üretiminde, pillerde elektrolit olarak ve gübre yapımında kullanılır.

Potasyum klorür kimyasal bir bileşiktir. KCl formülü ile gösterilir. Potasyum ve klor elementlerinin birleşmesi ile oluşur. Saf hali, kokusuzdur. Beyaz kristallerden oluşur. Bu kristallerde yüzey merkezli küp şeklinde istiflenerek dizilirler.

Sodyum nitrat formülü NaNO3 olan kimyasal bileşiktir. Güherçile'den ayırmak için Şili güherçilesi (bu ülkede büyük miktarda yığınlar halinde bulunması nedeniyle bu ad verilmiştir) adı da verilen bu beyaz renkli kristal tuz, potasyum nitrata oranla suda çok fazla çözünmektedir. Havadan nem çeker.

Mavi, çakır veya gök, resim boyamada ve geleneksel renk teorisi ve RGB renk modelindeki üç ana renkler pigmentlerinden biridir. Görünür ışığın tayfı üzerinde menekşe ve yeşil arasında uzanır. Göz yaklaşık 450 ile 495 nanometre arasında baskın dalga boyu olan ışığı gözlemlerken maviyi algılar. Çoğu mavi, diğer renklerin hafif bir karışımını içerir; gök mavisi biraz yeşil içerirken lacivert biraz menekşe içerir. Açık gündüz gökyüzü ve derin deniz Rayleigh saçılması olarak bilinen optik bir etki nedeniyle mavi görünür. Tyndall etkisi adı verilen bir optik etki, mavi gözler 'i açıklar. Havadan perspektif adı verilen başka bir optik etki nedeniyle uzaktaki nesneler daha mavi görünür. Karşıt rengi turuncu'dur.

Potasyum sülfat, formülü K2SO4 olan, yanmaz, suda çözünebilen beyaz kristal yapıda bir potasyum tuzudur. Genellikle potasyum ve kükürt kaynağı olarak gübrelerde kullanılır.
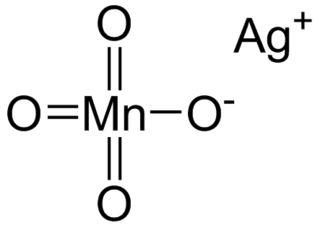
Gümüş permanganat kimyasal formülü AgMnO4 olan bir kimyasal bileşiktir. Gümüş permanganat monoklinik kristal sistemine ait mor renkli kristallere sahiptir. Isıtmayla ya da suyla karıştırıldığında parçalanır. Yüksek sıcaklıkta ısıtma patlamaya yol açabilir. Gümüş permanganat, gümüş nitrat ve potasyum permanganat arasındaki reaksiyonla elde edilebilir:
- AgNO3 + KMnO4 → AgMnO4 + KNO3
Baeyer ayıracı (Bayer ayıracı), organik kimyada kullanılan KMnO4 (potasyum permanganat) çözeltisine denir. Bu ayraç alkenlerle (etilenik bileşilerin) bazik ortamda tepkime vererek alkenleri diollere dönüştürür. Tepkime sonucunda çözeltinin menekşe rengi kaybolur. Ayrıca bu tepkime alkenlerin tanınma tepkimesidir.

Ortoklaz; dik açı biçiminde ayrıtları olan, billurları parça hâlinde bulunan bir çeşit potasyum feldspat, genellikle büyük kristallerdir. Net potasyum madde türüdür. Albitom ile bir katı çözelti oluşturur.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.
Permanganik asit, HMnO4 formülüne sahip bir inorganik bileşiktir. Bu güçlü oksoasit, dihidrat olarak izole edilmiştir. Permanganat tuzlarının konjugat asididir. Çok az sayıda yayın konusu olup, karakterizasyonu ve kullanımları çok sınırlıdır.
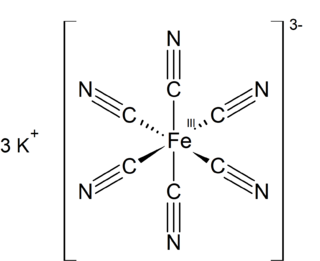
Potasyum ferrisiyanür K3[Fe(CN)6] formülü ile gösterilen inorganik bileşiktir. Bu parlak kırmızı tuz, oktahedral olarak koordine edilmiş [Fe(CN)6]3− iyonu içerir. Suda çözünür ve çözeltisi bir miktar yeşil-sarı flüoresans gösterir. 1822 yılında Leopold Gmelin tarafından keşfedilmiştir ve başlangıçta ultramarin boyalarının üretiminde kullanılmıştır.

Potasyum Florür, KF formülüne sahip bir kimyasal bileşik ve bir alkil halojenürdür. Hidroflorik asitten sonra imalat ve kimya uygulamaları için florür iyonunun birincil kaynağıdır. Hidroflorik asit gücünde olmasa da camı aşındırır.
Potasyum dikromat, K
2Cr
2O
7, çeşitli laboratuvar ve endüstriyel uygulamalarda en yaygın olarak oksitleyici madde olarak kullanılan yaygın bir inorganik kimyasal reaktiftir. Tüm altı değerlikli krom bileşiklerinde olduğu gibi sağlığa akut ve kronik olarak zararlıdır. Çok parlak, kırmızı-turuncu renge sahip kristal iyonik bir katıdır. Bu tuz, endüstriyel açıdan daha uygun olan sodyum dikromat tuzunun aksine, nemden arındırılmadığı için laboratuvarlarda popülerdir.