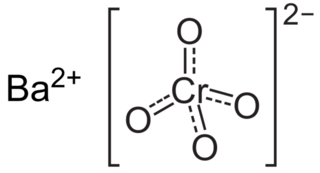Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Potasyum, bir kimyasal elementtir. Simgesi K ve atom numarası 19 dur. Potasyum adını izole edildiği Potas olarak da bilinen potasyum karbonattan almıştır. Potasyum yumuşak, gümüş-beyaz renkli alkali bir metaldir. Doğada deniz suyunda ve pek çok mineralde diğer elementlere bağlı olarak bulunur. Havada hızla oksitlenir ve suya karşı da çok aktiftir. Potasyum, pek çok açıdan sodyuma kimyasal olarak benzese de yaşayan organizmalarda, özellikle de hayvan hücrelerinde, sodyumdan farklı muamele görür. Kandaki seviyesinin düşük olmasına hipokalemi, yüksek olmasına hiperkalemi denir.

Potasyum permanganat, koyu menekşe renkte kristal yapılı bir tuz (KMnO4). Klorun potasyum manganata etkisiyle elde edilir.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.

Kalsiyum kromat (CaCrO4) parlak sarı renkli bir katıdır. Genellikle dihidrat halinde olur. Ancak kromatit olarak bilinen çok nadir bulunan doğal (mineral) formu, susuzdur. Çok zehirlidir.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.

Kloröz asit, HClO2 formülüne sahip bir inorganik bileşiktir. Zayıf bir asittir. Klor, bu asitte +3 oksidasyon durumuna sahiptir. Saf madde dengesiz, hipokloröz aside (Cl oksidasyon hali + 1) ve klorik aside (Cl oksidasyon hali + 5) orantısızdır:
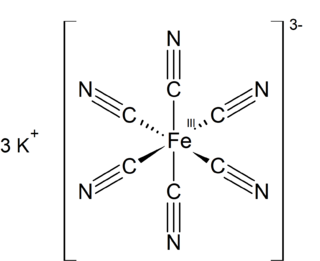
Potasyum ferrisiyanür K3[Fe(CN)6] formülü ile gösterilen inorganik bileşiktir. Bu parlak kırmızı tuz, oktahedral olarak koordine edilmiş [Fe(CN)6]3− iyonu içerir. Suda çözünür ve çözeltisi bir miktar yeşil-sarı flüoresans gösterir. 1822 yılında Leopold Gmelin tarafından keşfedilmiştir ve başlangıçta ultramarin boyalarının üretiminde kullanılmıştır.

Buz çözme, yani diğer adıyla anti Icıng yüzeydeki kar, buz veya donu temizleme işlemidir. Buzlanmayı önleme, sadece buzdan arınmakla kalmayan, aynı zamanda yüzeyde kalan ve belirli bir süre boyunca buzun yeniden oluşmasını geciktiren veya mekanik olarak çıkarmayı kolaylaştırmak için buzun yüzeye yapışmasını önleyen kimyasal maddelerin uygulanmasıdır.

Krom turuncusu Pb2CrO5 kimyasal formülüne sahip bir karma oksittir. Bir kurşun(II) tuzunun alkali bir kromat çözeltisi ile veya krom sarısının (PbCrO4) kuvvetli bazik çözelti ile muamele edilerek yapılabilir.

Krom sarısı kurşun(II) kromat (PbCrO4)’tır. Krokoit minerali şeklinde doğal olarak bulunsa da maden cevheri hiçbir zaman boya pigmenti olarak kullanılmadı. Fransız kimyager Louis Vauquelin yeni bir element olarak kromu keşfettikten sonra, 1797 yılında kurşun kromat laboratuvarda sentezlendi ve ondokuzuncu yüzyılın ikinci on yılın başında bir pigment olarak kullanıldı.

Sodyum kromat Na2CrO4 formülüne sahip bir inorganik bileşiktir. Tetra-, hekza- ve dekahidratlar oluşturabilen sarı higroskopik bir katı olarak bulunur. Cevherlerinden krom özütlemesinde bir ara maddedir.
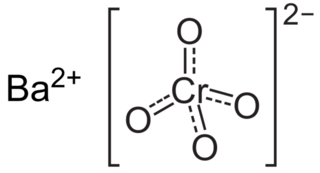
Baryum kromat, BaCrO4 formülüne sahip sarı renkli, kum gibi toz bir maddedir. Bilinen bir oksitleyici maddedir ve baryum iyonlarının bir sonucu olarak ısıtıldığında yeşil bir alev üretir.

Sodyum bikromat Na2Cr2O7 formülüne sahip bir inorganik bileşiktir. Ancak, genellikle tuz dihidrat Na2Cr2O7•2H2O olarak kullanılır. Neredeyse tüm krom cevheri, sodyum bikromata dönüştürülerek işlenir ve neredeyse krom bazlı bütün bileşikler ve maddeler bu tuzdan hazırlanır. Reaktivite ve görünüm açısından, sodyum bikromat ve potasyum bikromat çok benzerdir. Bununla birlikte sodyum tuzu, suda potasyum tuzundan yaklaşık yirmi kat daha fazla çözünür(0 °C’de 49 g/L) ve eşdeğer ağırlığı da daha düşüktür ki bu da genellikle istenen bir durumdur.

Kurşun(II) tiyosiyanat,Pb(SCN)2 formülüne sahip bir bileşik daha doğrusu bir tuzdur. Beyaz kristalimsi bir katıdır, ancak ışığa maruz kaldığında sararır. Suda az çözünür ve kaynatıldığında bazik bir tuz olan (Pb(CNS)2*Pb(OH)2'ye dönüştürülebilir. Soğutulduğunda tuz kristalleri oluşabilir. Kurşun tiyosiyanat, yutulması halinde kurşun zehirlenmesine neden olabilir ve birçok madde ile olumsuz reaksiyona girebilir. Küçük patlayıcılar, kibritler ve boyamalarda kullanılır.

Kurşun monoksit olarak da adlandırılan kurşun(II) oksit, PbO moleküler formülüne sahip inorganik bileşiktir. PbO iki polimorfda oluşur: tetragonal kristal yapıya sahip litarj ve ortorombik kristal yapıya sahip massikot. PbO için modern uygulamalar çoğunlukla kurşun bazlı endüstriyel cam ve, bilgisayar bileşenlerini de kapsayan endüstriyel seramiklerdir. Amfoterik bir oksittir.
Kromik asit terimi genellikle, katı krom trioksit de dahil olmak üzere çeşitli bileşikler içerebilen bir dikromata konsantre sülfürik asit eklenerek yapılan bir karışım için kullanılır. Bu tür kromik asit, cam için bir temizleme karışımı olarak kullanılabilir. Kromik asit ayrıca trioksitin anhidrit olduğu H2CrO4 moleküler türlerine de atıfta bulunabilir. Kromik asit, +6 (veya VI) oksidasyon durumunda krom içerir. Güçlü ve aşındırıcı bir oksitleyici ajandır.
Simya çalışmaları sayesinde daha sonra belirli kimyasal bileşikler veya bileşik karışımları olarak sınıflandırılan birçok kimyasal madde üretilmiştir.
Potasyum dikromat, K
2Cr
2O
7, çeşitli laboratuvar ve endüstriyel uygulamalarda en yaygın olarak oksitleyici madde olarak kullanılan yaygın bir inorganik kimyasal reaktiftir. Tüm altı değerlikli krom bileşiklerinde olduğu gibi sağlığa akut ve kronik olarak zararlıdır. Çok parlak, kırmızı-turuncu renge sahip kristal iyonik bir katıdır. Bu tuz, endüstriyel açıdan daha uygun olan sodyum dikromat tuzunun aksine, nemden arındırılmadığı için laboratuvarlarda popülerdir.