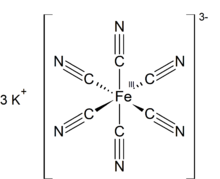Siyanür, bir karbon ve ona üçlü bağ ile bağlanmış bir azot içeren C≡N grubuna sahip kimyasal bileşiklere verilen addır. Bu grup aynı zamanda siyano grubu olarak da bilinir. Organik ve inorganik çeşitleri bulunan siyanürler özellikle endüstride kullanılmaları için üretilmektedir. İnorganik siyanüre örnek olarak çok zehirli potasyum siyanür, organik siyanüre örnek olarak da düşük toksisiteli asetonitril verilebilir. Her siyanür yüksek oranda zehirli değildir.

Gümüş, elementlerin periyodik tablosunda simgesi Ag olan, beyaz, parlak, değerli bir metalik element. Atom numarası 47, atom ağırlığı 107,87 gramdır. Erime noktası 961,9 °C, kaynama noktası 1950 °C ve özgül ağırlığı da 10,5 g/cm³'tür. Çoğu bileşiklerinde +1 değerliklidir. Günümüzde Dünya'da 55 yıllık gümüş rezervi kaldığı tahmin ediliyor. Yeni gümüş rezervleri keşfedilmezse 2078 yılında Dünya'daki gümüş rezervlerinin tükenebileceği tahmin ediliyor. En çok gümüş üretimi yapan ülkeler Meksika, Çin, Peru Şili ve Avustralya'dır.

Demir oksitler, demir ve oksijenden oluşan kimyasal bileşiklerdir. Sadece birkaç demir oksit tanınır. Hepsi siyah manyetik katılardır. Genellikle stokiyometrik değildirler. Oksihidroksitleri, belki de en iyi bilineni pas olan ilgili bir bileşik sınıfıdır.

Potasyum nitrat, formülü KNO3 olan bir potasyum bileşiğidir. Güherçile olarak da bilinen bileşik doğal hâlde kayaçlarda ve mağaralarda oluşan beyaz renkli kabuksu yapıda bulunur.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.

Akridin, C13H9N, heterosiklik bir organik bileşiktir. Akridin terimi ayrıca C13N üçlü halkasını içeren bileşiklere değinmek için kullanılır.

Hidrojen siyanür, HCN formüllü inorganik bir bileşiktir. Endüstriyel ölçekte üretilen HCN, polimerlerden ilaçlara kadar birçok kimyasal bileşik için oldukça değerli bir öncüdür. Büyük ölçekli uygulamalar, sırasıyla madencilik ve plastikte kullanılan potasyum siyanür ve adiponitril üretimi içindir. Hidrojen siyanür, 25 °C'de kaynayan renksiz acıbadem kokusunda bir sıvıdır. Uçucu bir sıvı olduğundan, katı siyanür bileşiklerinden daha zehirlidir.

Potasyum ferrosiyanür formülü K4[Fe(CN)6] • 3H2O olan bir kimyasal bileşiktir. Potasyum ferrosiyanür metal kompleks bileşiğinin [Fe(CN)6]4− potasyum tuzudur. Bu tuz limon sarısı monoklinik kristallerden oluşmuştur.

Alüminyum klorür (AlCl3), alüminyum ve klorürün temel bileşiği. Rengi genel olarak beyazdır fakat Demir(III) klorür ile etkileşime girdiğinde sarı bir renk alır. Katı erime ve kaynama noktası düşüktür. Genel olarak alüminyum metallerin üretiminde kullanılır. Ayrıca kimya endüstrisinin diğer alanlarında da yüksek miktarda kullanılır. Bileşik sıklıkla Lewis asiti olarak anılır.

Kobalt mavisi kobalt (II) oksit ile alüminyum oksit ile 1200 °Cde yapılan mavi bir pigmenttir. Kimyasal olarak, kobalt mavisi pigmenti, kobalt (II) oksit-alüminyum oksit veya kobalt (II) alüminattır (CoAl2O4). Kobalt mavisi (demir siyanür esaslı), Prusya mavisinden daha hafif ve yoğundur. Oldukça kararlıdır ve tarihsel olarak seramikte (özellikle Çin porseleni, mücevherat ve boya renklendiricilerde) bir renklendirici olarak kullanılmıştır. Şeffaf cam silika esaslı kobalt pigmenti smalt ile renklendirilir.

Kalay(II) klorür ya da stanit klorür, SnCl2 formülüne sahip, beyaz kristal halinde bir katıdır. Kararlı bir dihidrat oluşturur, ancak sulu çözeltileri, özellikle sıcaksa, hidrolize uğrama eğilimindedir. SnCl2 yaygın bir şekilde indirgeyici madde (bir asit çözeltisi içinde) olarak ve kalay kaplamada elektrolitik banyolarda kullanılır. Kalay (II) klorür, diğer kalay klorür (kalay(IV) klorür (SnCl4) ile karıştırılmamalıdır.

Çinko siyanür, Zn(CN)2 formüllü ile gösterilen bir inorganik bileşiktir. Esas olarak çinko kaplamada kullanılan beyaz renkli bir katıdır, ancak organik bileşiklerin sentezi için daha özel uygulamalara da sahiptir.

Kimyada, oktahedral moleküler geometri, bir oktahedronun köşelerini tanımlayan, merkezi bir atom etrafında simetrik olarak düzenlenmiş altı atomlu bileşiklerin veya atom gruplarının veya ligandların şeklini tanımlar. Oktahedronun sekiz yüzü vardır, dolayısıyla octa ön ekini alır. Oktahedron, Platonik katılardan biridir, ancak oktahedral moleküller tipik olarak merkezlerinde bir atom içerir ve ligand atomları arasında bağ yoktur. Mükemmel bir oktahedron Oh nokta grubuna aittir. Oktahedral bileşiklerin örnekleri arasında kükürt hekzaflorür SF6 ve molibden hekzakarbonil Mo (CO)6 gösterilebilir. "Oktahedral" terimi, kimyagerler tarafından, merkezi atoma olan bağların geometrisine odaklanarak ve ligandların kendi aralarındaki farklılıkları dikkate almadan biraz gevşek bir şekilde kullanılır. Örneğin, N-H bağlarının oryantasyonu nedeniyle matematiksel anlamda oktahedral olmayan [Co(NH3)6]3+, oktahedral olarak adlandırılır.

Prusya mavisi (aynı zamanda Berlin mavisi veya yağlı boya tablolarda Parizyen veya Paris mavisi olarak bilinir), demir içeren ferrosiyanür tuzlarının oksidasyonu ile üretilen koyu mavi pigmenttir. FeIII4III4[FeII(CN)6]3 kimyasal formülüne sahiptir. Turnbull mavisi kimyasal olarak aynıdır ancak farklı reaktiflerden yapılmıştır ve çeşitli safsızlıklar nedeniyle rengi biraz farklıdır.
Demir (III) klorür FeCl
3 formüllü inorganik bir bileşiktir. Kristal bir katı olmasının yanı sıra görüş açısına bağlı olarak farklı renklerle gözlemlenebilir; koyu yeşil, mor-kırmızı. Sulu formu da katı formu da fiziksel görünüm olarak koyu kahverengi rengindedir.
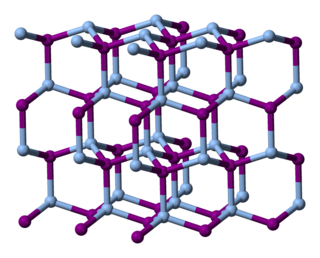
Gümüş iyodür, AgI formülüne sahip bir inorganik bileşiktir. Bileşik parlak sarı bir katıdır, ancak numuneler neredeyse her zaman gri bir renk veren metalik gümüş safsızlıkları içerir. Gümüş bulaşması, AgI'nin yüksek düzeyde ışığa duyarlı olması nedeniyle ortaya çıkar. Bu özellik gümüş esaslı fotoğrafçılık'ta kullanılır. Gümüş iyodür ayrıca antiseptik olarak ve bulut tohumlama için de kullanılır.
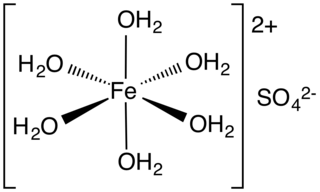
Demir (II) sülfat veya demir sülfat FeSO4•xH2O formülüne sahip bir dizi tuz anlamına gelir. Bu bileşikler en yaygın olarak heptahidrat (x = 7) olarak bulunursa da x için birkaç değer bilinmektedir. Hidratlı form tıp alanında demir eksikliğini tedavi etmek ve ayrıca endüstriyel uygulamalar için kullanılır. Antik çağlardan beri, Zaç-ı Kıbrıs ve yeşil vitriyol (vitriyol, sülfat için eski bir isimdir) olarak bilinen, mavi-yeşil heptahidrat (7 molekül su içeren hidrat) bu maddenin en yaygın şeklidir. Tüm demir (II) sülfatlar suda çözünerek oktahedral moleküler geometriye sahip ve paramanyetik olan aynı akua kompleksi [Fe(H2O)6]2+ verir.

Uranil nitrat, UO2(NO3)2.n H2O formülüne sahip, suda çözünür sarı renkli bir uranyum tuzudur. Hekza-, tri- ve dihidratlar bilinmektedir. Bileşik esas olarak nükleer yakıtların hazırlanmasında bir ara madde olarak kullanılma potansiyeliyle ilgi çekmiştir.