Polimer bazlı pil
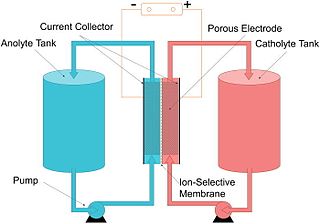
Polimer bazlı pil, dökme metaller yerine organik malzemeler kullanır.[1] Metal bazlı piller, sınırlı kaynaklar, olumsuz çevresel etki ve yaklaşan ilerleme sınırı nedeniyle zorluklar yaşamaktadır. Redoks aktif polimerler, sentezlenebilmeleri, kapasiteleri, esneklikleri, hafiflikleri, düşük maliyetleri ve düşük toksisiteleri nedeniyle cazip seçeneklerdir.[2]
Araştırmalar, polimerik malzemelerin kullanıldığı pillerde verimliliğin nasıl artırılacağını ve zorlukların nasıl azaltılacağını araştırdı. İletken, iletken olmayan ve radikal polimerler dahil olmak üzere birçok polimer türü araştırılmaktadır. Bir metal elektrot ve bir polimerik elektrota sahip pillerin test edilmesi ve mevcut metal bazlı pillerle karşılaştırılması daha kolaydır, ancak hem polimer katot hem de anot içeren piller de güncel bir araştırma odağıdır. Metal/polimer elektrot kombinasyonları dahil olmak üzere polimer bazlı piller, polimerik aktif malzemelerin aksine çoğunlukla polimerik bir elektrolit içeren lityum polimer pil gibi metal-polimer pillerden ayırt edilmelidir.
Organik polimerler düşük sıcaklıklarda işlenebilir ve bu da maliyetleri düşürür. Ayrıca daha az karbondioksit üretirler.[3]
Tarih
Organik pil alanında çok fazla araştırma yapılmaktadır.
1982'de "Plastik-Metal Piller: Elektrikli araba için yeni vaatler"[4] başlıklı bir makalede "İki farklı organik polimerin pillerde olası kullanımı araştırılıyor" ve verdiği demo'nun 1976'da başlayan çalışmalara dayandığı belirtiliyordu.
NEC, 2001 yılında Waseda Üniversitesi'ne başvurdu ve organik pillere odaklandı. 2002'de NEC araştırmacısı, Piperidinoxyl Polymer teknolojisi üzerine bir makale ve 2005'te modifiye edilmiş bir PTMA, (poli(2,2,6,6-tetrametilpiperidiniloksi-4-il meth-akrilat)) bazlı bir organik radikal pil (ORB) sundular.[5]
2006 yılında, Brown Üniversitesi polipirole dayalı bir teknolojiyi duyurdu.[1] Waseda, 2007 de "çözünür polimer, asılı nitroksit radikal gruplarına sahip polinorboren"e dayalı yeni bir ORB teknolojisini duyurdu.
2015 yılında araştırmacılar verimli, iletken, elektron taşıyan bir polimer geliştirdiler. Keşif, transistörler ve güneş pilleri için kullanılmış olan bir naftalin - bitiyofen polimeri ile "konjuge redoks polimeri" tasarımını kullandı.
Lityum iyon katkısıyla önemli ölçüde elektronik iletkenlik sağlandı ve bu 3.000 şarj/deşarj döngüsü boyunca sabit kalmıştı. Delikleri ileten polimerler bir süredir mevcuttu.
Polimer pil, bir organik malzeme için en yüksek güç yoğunluğunu sergiler, 6 saniye içinde %80 oranında şarj edilebilir di. Ancak enerji yoğunluğu inorganik pillere göre daha düşük kaldı.[3]
Elektrokimya
Polimer tabanlı pildeki reaksiyon da farklı redoks potansiyellerine sahip bir pozitif ve negatif elektrot arasındadır. Bir elektrolit, bu elektrotlar arasında yükleri taşır. Bir maddenin uygun bir pil aktif maddesi olabilmesi için, kimyasal ve termodinamik olarak tersinir bir redoks reaksiyonuna katılabilmesi gerekir. Metallerin değerlik yüküne dayanan metal tabanlı pillerin karşılığında, polimer tabanlı pillerin redoks işlemi organik materyaldeki yük durumunun değişmesine dayanır.[6] Yüksek enerji yoğunluğu için elektrotların benzer özgül enerjilere sahip olması gerekir.[6]
Aktif maddelerin sınıflandırılması
Organik malzeme p-tipi, n-tipi veya b-tipi olabilir. Şarj sırasında p-tipi malzemeler oksitlenerek katyon üretirken, n-tipi malzemeler indirgenerek anyon üretir. B tipi organikler, şarj veya deşarja bağlı, oksitlenebilir veya indirgenebilir malzemelerdir.[6]
Şarj ve deşarj
Li-ion pilde Li+ iyonları interkalasyon nedeniyle yavaşça yayılır ve şarj veya deşarj sırasında ısı üretebilir. Bununla birlikte, polimer bazlı piller, daha verimli bir şarj/deşarj işlemine sahiptir, bu da gelişmiş teorik hız performansı ve daha fazla döngü sağlar.[3]
Şarj
Polimer bazlı bir pilin şarj edilmesiyle ilgili sınırlayıcı faktörler, metal bazlı pillerden farklıdır ve organik katodun tamamen oksidasyonunu, organik anodun tamamen indirgenmesini veya elektrolit tüketimini içerir.[3]
Deşarj
Deşarjda, elektrolit polimerden salınan iyonları taşırken, elektronlar harici olarak anottan katoda giderler. Bu süreç ve dolayısıyla hız performansı, elektrolit iyon hareketi ve reaksiyonun elektron transfer hızı sabiti k0 ile sınırlıdır.
Bu elektron aktarım hızı sabiti, tipik olarak 10−1 cm s−1 mertebesinde yüksek değerlere sahip olan polimer bazlı piller için avantaj sağlar. Organik polimer elektrotlar şekilsiz ve şişkindir, bu da daha yüksek iyonik difüzyon hızına katkıda bulunur.[3] Bununla birlikte, farklı polimerler, farklı reaksiyon hızlarına sahiptir. Bir nitroksil radikali yüksek bir reaksiyon hızına sahipken, organodisülfatlar, bağlar kırıldığı ve yeni bağlar oluştuğu için önemli ölçüde daha düşük oranlara sahiptir.[7]
Piller teorik kapasitelerine göre değerlendirilir. Bu değer şu şekilde hesaplanabilir:
Formülde m, aktif maddenin toplam kütlesi, n, aktif maddenin molar kütlesi başına aktarılan elektronların sayısı, M, aktif maddenin molar kütlesi ve F, Faraday sabitidir.[8]
Şarj ve deşarj testi
Çoğu polimer elektrot, karşılaştırma kolaylığı nedeniyle metal-organik bir pilde test edilir. Test düzeneğinde, metal anot görevi görürken katot olarak n- veya p-tipi polimer elektrotlar kullanılır. N-tipi organik test edilirken, bu metal-polimer pil montaj üzerine şarj edilir ve deşarj sırasında metal oksitlenirken n-tipi malzeme indirgenir. Bir metal-polimer testinde p-tipi organikler için pil, montaj sırasında zaten boşalmıştır. İlk şarj sırasında, organik oksitlenirken elektrolit tuz katyonları indirgenir ve polimerik anoda mobilize edilir. Boşaltma sırasında, metal katyonuna oksitlenirken polimer indirgenir.[3]
Aktif madde türleri
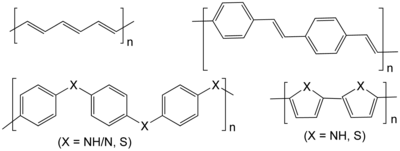
İletken polimerler
İletken polimerler, konjuge bir polimer omurgası üzerindeki katkı iyonlarıyla iletkenliğe sahip elektrokimyasal iletkenliğe sahip aktif bir malzemelerdir.[9][2] İletken polimerler, kükürt iletken polimerler haricinde, asılı gruplara sahip olmanın aksine, redoks aktif grubu ile gömülüdür.[2] İletkenlikleri ve redoks aktiviteleri nedeniyle ideal elektrot malzemeleridir ve büyük miktarlarda aktif olmayan iletken dolgu maddeleri gerektirmezler.[10] Bununla birlikte, aynı zamanda, düşük kulombik verimliliğe sahip olma eğilimindedirler ve zayıf döngüsellik ve kendi kendine deşarj sergilerler.[7] Polimerin yüklü merkezlerinin zayıf elektronik ayrımı nedeniyle, konjuge polimerlerin redoks potansiyelleri, katkı seviyelerine bağlı olarak şarj ve deşarj üzerine değişir. Bu karmaşıklığın bir sonucu olarak, iletken polimer pillerin deşarj profili (hücre voltajına karşı kapasite) eğimli bir eğriye sahiptir.[3]
İletken polimerler, polimer monomer birimi başına bir yük idealine ulaşamayan yüksek yük seviyeleri nedeniyle kararlı değillerdir. Stabilize edici katkı maddeleri eklenebilir, ancak bunlar spesifik kapasiteyi azaltır.[3]
Askılı gruplara sahip konjuge olmayan polimerler
Konjuge polimerlerin birçok dezavantajı, redoks aktif asılı gruplara sahip polimerlerin araştırılmasını gerektirdi. Keşfedilen gruplar arasında karboniller, karbazoller, organosülfür bileşikleri, viologen ve şarj ve deşarj üzerine yüksek reaktiviteye ve kararlı voltaja sahip diğer redoks-aktif moleküller bulunur.[2] Bu polimerler, lokalize redoks bölgeleri ve şarj/deşarj üzerinde daha sabit redoks potansiyeli nedeniyle konjuge polimerlere göre bir avantaj sunar.[3]
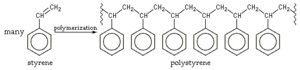
Karbonil kolye grupları
Karbonil bileşikleri yoğun bir şekilde incelendi. Karbonil gruplarına sahip polimerler, çok değerlikli anyonlar oluşturabilir. Stabilizasyon sübstitüentlere bağlıdır; komşu karboniller enolat oluşumu ile stabilize edilir, aromatik karboniller yükün delokalizasyonu ile stabilize edilir ve kinoidal karboniller aromatiklik ile stabilize edilir.[3]

Organokükürt grupları
Kükürt, dünyanın en bol bulunan elementlerinden biri olmasıyla avantajlıdır. Küçük moleküllü organosülfür aktif malzemeleri, bir polimere dahil edilme yoluyla kısmen çözülen zayıf stabilite sergiler. Disülfit polimerlerinde elektrokimyasal yük, disülfit bağının tersinir iki elektronlu oksidasyonu ile oluşturulan bir tiyolat anyonunda depolanır. Tiyoeterlerde elektrokimyasal depolama, nötr bir tiyoeterin +2 yüklü bir tiyoetere iki elektronlu oksidasyonu ile sağlanır. Bununla birlikte organosülfür bileşikleri zayıf döngülenebilirlik sergiler.[3]
Radikal gruplar

Organik radikal pillerdeki polimer elektrotlar, yüksüz durumda eşleşmemiş bir elektrona sahip kararlı organik radikal asılı gruplarla elektrokimyasal olarak aktiftir.[11] Nitroksit radikalleri en yaygın olarak uygulananlardır, ancak fenoksil ve hidrazil grupları da sıklıkla kullanılır.[3] Bir nitroksit radikali tersine çevrilebilir şekilde oksitlenebilir ve polimer p-katkılı veya indirgenerek n-katkılamaya neden olabilir. Yüklendikten sonra radikal bir oksoamonyum katyonuna oksitlenir ve katotta radikal bir aminooksil anyonuna indirgenir.[12] Bu işlemler deşarj üzerine tersine çevrilir ve radikaller yeniden üretilir.[11] Kararlı şarj ve deşarj için, radikalin hem radikal hem de katkılı formu kimyasal olarak kararlı olmalıdır.[12] Bu piller, radikalin kararlılığına ve basit bir elektron transfer reaksiyonuna atfedilen mükemmel döngüsellik ve güç yoğunluğu sergiler. Tekrarlanan döngüden sonra kapasitede hafif bir düşüş, elektrotun direncini artıran şişmiş polimer parçacıklarının birikmesinden kaynaklanmaktadır. Radikal polimerler önemli ölçüde yalıtkan olduğundan, genellikle teorik özgül kapasiteyi düşüren iletken katkı maddeleri eklenir. Neredeyse tüm organik radikal piller, deşarj sırasında iletken polimer pillere göre bir avantaj olan neredeyse sabit bir voltaja sahiptir.[11] Polimer omurgası ve çapraz bağlama teknikleri, polimerin elektrolit içindeki çözünürlüğünü en aza indirecek ve böylece kendi kendine boşalmayı en aza indirecek şekilde ayarlanabilir.[11]
Kontrol ve performans
Temel polimer elektrot tiplerinin performans özeti karşılaştırması [13]
| polimer tipi | elektrot malzemesi (elektrolit doping türleri) | İlk Tersinir Kapasite (mAh g −1 ) | Çalışma Gerilimi | Döndürülebilirlik (mAh g −1 ) |
|---|---|---|---|---|
| eşlenik | PANİ (CLO 4 - ve Li + ) | 75.7 | 3.90-2.0 | 80 döngüden sonra 75,7 |
| PPy (SO 4 2- ) | 52.2 | |||
| PPP (PF 6 - ve Li + ) | 80 (p-doping) 400 (n-katkılama) | 4.6-3.0 3.0-0.0 | 100 döngüden sonra 70 90 döngüden sonra 580 | |
| organosülfür | PDMcT 4 | 240 | 3.8-1.8 | 10 döngüden sonra 10 |
| tiyoeter | PTBDT 5 | 240 | 4.2-1.4 | 20 döngüden sonra 560 |
| nitroksil radikali | PTMA (Li + ve PF 6 - ) | 77 | 4.0-3.0 | 500 döngüden sonra 68 |

İletken polimerler deşarj sırasında, pratik uygulamalarını engelleyen eğimli bir voltaj eğrisine sahiptir. Bu eğimli eğri, morfoloji, boyut, reaksiyon sırasında polimer zinciri içindeki yük itmelerinden veya polimerlerin amorf durumundan kaynaklanabilecek elektrokimyasal kararsızlığı gösterir.
Polimer morfolojisinin etkisi
Polimer elektrotların elektrokimyasal performansı, polimer boyutu, morfolojisi ve kristallik derecesinden etkilenir.[14] Bir polipirol (PPy)/Sodyum iyon hibrit pilde, 2018'de yapılan bir çalışma, mikron altı parçacık zincirlerinden oluşan kabartılmış yapıya sahip polimer anodun, çok daha yüksek bir performans gösterdiğini gösterdi. (34,8 mAh g'ye karşılık 183 mAh g−1) [15]
Mikron altı polipirol anotun yapısı, parçacıklar arasında artan elektrik temasına izin verdi ve elektrolit, polimerik aktif malzemeye daha fazla nüfuz edebildi. Ayrıca, amorf polimerik aktif malzemelerin kristal muadillerinden daha iyi performans gösterdiği de bildirilmiştir. 2014 yılında, kristal oligopirenin 42,5 mAh g−1 boşaltma kapasitesi sergilediği, amorf oligopirenin ise 120 mAh g−1 gibi daha yüksek bir kapasiteye sahip olduğu gösterildi. Ayrıca, kristal versiyon eğimli bir şarj ve deşarj voltajına ve Cl04 - 'ün yavaş difüzyonu nedeniyle önemli ölçüde aşırı potansiyele maruz kaldı. Amorf oligopiren, şarj ve deşarj sırasında bir voltaj platosuna ve ayrıca önemli ölçüde daha az aşırı potansiyele sahipti.[16]
Moleküler ağırlık kontrolü
Polimerlerin moleküler ağırlığı, kimyasal ve fiziksel özelliklerini ve dolayısıyla polimer elektrodun performansını etkiler. 2017 yılında yapılan bir araştırmada moleküler ağırlığın poly(TEMPO methacrylate) (PTMA)'nın elektrokimyasal özellikleri üzerindeki etkisi değerlendirildi.[17] Monomer başlatıcı oranı 50/1'den 1000/1'e yükseltilerek beş farklı boyut elde edildi. Moleküler ağırlık ne kadar yüksekse, polimerler o kadar yüksek spesifik deşarj kapasitesi ve daha iyi döngülenebilirlik sergiledikleri için moleküler ağırlığa güçlü bir bağımlılık kurulmuştur. Bu etki, moleküler ağırlık ile elektrolit içindeki çözünürlük arasındaki karşılıklı ilişkiye bağlandı.[17]
Avantajlar
Polimer bazlı pillerin birçok avantajı vardır. Elektrokimyasal reaksiyonlar daha basittir ve polimerlerin yapısal ve sentez çeşitliliği esneklik sağlar.[2][3] Yeni inorganik malzeme türlerinin bulunması zorken, organik polimerler çok daha kolay sentezlenebilir.[7] Diğer bir avantaj, polimer elektrot malzemelerinin daha düşük redoks potansiyellerine sahip olabilmeleri, ancak inorganik malzemelere göre daha yüksek bir enerji yoğunluğuna sahip olmalarıdır.
Ve organikler için redoks reaksiyon kinetiği inorganiklerden daha yüksek olduğu için, daha yüksek bir güç yoğunluğu ve hız performansına sahiptirler. İnorganik malzemelerle karşılaştırıldığında organik malzemelerin doğal esnekliği ve hafifliği nedeniyle, polimerik elektrotlar basılabilir, dökülebilir ve buhar biriktirilebilir, bu da daha ince ve daha esnek cihazlarda uygulanmasına olanak tanır. Ayrıca, çoğu polimer düşük maliyetle sentezlenebilir veya biyokütleden ekstrakte edilebilir ve hatta geri dönüştürülebilirken, inorganik metallerin bulunabilirliği sınırlıdır ve çevreye zararlı olabilir.[7]
Organik küçük moleküller de bu avantajların çoğuna sahiptir, ancak elektrolit içinde çözünmeye daha yatkındırlar. Polimerik organik aktif maddeler daha zor çözünür ve bu nedenle üstün döngülenebilirlik sergiler.[7]
Zorluklar
Bu anlamda küçük organik moleküllerden daha üstün olmasına rağmen, polimerler hala elektrolitlerde çözünürlük sergilerler ve pil stabilitesi, elektrotlar arasında dolaşabilen çözünmüş aktif malzeme tarafından tehdit edilir, bu da azalan döngüselliğe ve kendi kendine deşarja yol açar. Bu sorun, redoks-aktif birimi polimerik omurgaya dahil ederek azaltılabilir, ancak bu teorik özgül kapasiteyi azaltabilir ve elektrokimyasal polarizasyonu artırabilir.[3][7] Diğer bir zorluk ise, iletken polimerlerin yanı sıra, çoğu polimerik elektrotun elektriksel olarak yalıtkan olması ve bu nedenle iletken katkı maddeleri gerektirmesi ve pilin toplam kapasitesini düşürmesidir. Polimerler düşük bir kütle yoğunluğuna sahipken, daha büyük bir hacimsel enerji yoğunluğuna sahiptirler ve bu da güç verilen cihazların hacminde bir artış gerektirecektir.[7]
Emniyet
2009 yılında yapılan bir araştırma, hidrofilik bir radikal polimerin güvenliğini değerlendirdi: Sulu elektrolit içeren bir radikal polimer pilin toksik olmadığını, kimyasal olarak kararlı olduğunu ve patlayıcı olmadığını ve bu nedenle geleneksel metal bazlı pillere göre daha güvenli bir alternatif olduğunu buldu.[3][18] Sulu elektrolitler, toksik olabilen ve HF asidi oluşturabilen organik elektrolitlere göre daha güvenli bir seçenek sunar. Bir radikal polimer elektrodun şarj sırasındaki bir elektronlu redoks reaksiyonu çok az ısı üretir ve bu nedenle termal kaçak riskini azaltır.[3] Tüm polimerik elektrotların güvenliğini tam olarak anlamak için daha ileri çalışmalar gereklidir.
Ayrıca bakınız
Kaynakça
- ^ a b "Brown engineers build a better battery with plastic". PhysOrg.com. 13 Eylül 2006. 16 Ekim 2006 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Kasım 2011. Kaynak hatası: Geçersiz
<ref>etiketi: "PhysOrg" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ a b c d e "Redox-Active Polymers for Energy Storage Nanoarchitectonics". Joule. 1 (4): 739-768. December 2017. doi:10.1016/j.joule.2017.08.018. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) Kaynak hatası: Geçersiz<ref>etiketi: ":2" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ a b c d e f g h i j k l m n o p "Researchers discover N-type polymer for fast organic battery". R&D. 6 Nisan 2015. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) Kaynak hatası: Geçersiz<ref>etiketi: ":0" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ Daniel Ruby (February 1982). "Plastic-Metal Batteries: New promise for the electric car". Popular Science. ss. 89-91.
- ^ Takeo Suga (2005). "Organic Radical Battery" (PDF). The Electrochemical Society Interface. 16 Mart 2006 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 3 Kasım 2011. Yazar
|ad1=eksik|soyadı1=(yardım); Yazar eksik|soyadı2=(yardım) - ^ a b c "Polymer-Based Organic Batteries". Chemical Reviews. 116 (16): 9438-9484. 24 Ağustos 2016. doi:10.1021/acs.chemrev.6b00070. ISSN 0009-2665. PMID 27479607. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) Kaynak hatası: Geçersiz<ref>etiketi: "Muench_2016" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ a b c d e f g "Organic small molecules and polymers as an electrode material for rechargeable lithium ion batteries". Journal of Materials Chemistry A. 6 (41): 19885-19911. 2018. doi:10.1039/C8TA04906H. ISSN 2050-7488. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) Kaynak hatası: Geçersiz<ref>etiketi: "Bhosale_2018" adı farklı içerikte birden fazla tanımlanmış (Bkz: ) - ^ "Development of Active Organic and Polymeric Materials for Batteries and Solar Cells: Introduction to Essential Characterization Techniques". Advanced Energy Materials. 5 (24): 1500858. December 2015. doi:10.1002/aenm.201500858. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Electrically conductive polymers as rechargeable battery electrodes". Solid State Ionics. 28-30: 983-989. September 1988. doi:10.1016/0167-2738(88)90316-5. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "The rise of organic electrode materials for energy storage". Chemical Society Reviews. 45 (22): 6345-6404. 2016. doi:10.1039/C6CS00173D. ISSN 0306-0012. PMID 27273252. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ a b c d "Powering up the Future: Radical Polymers for Battery Applications". Advanced Materials (İngilizce). 24 (48): 6397-6409. 18 Aralık 2012. doi:10.1002/adma.201203119. PMID 23238940. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ a b "Environmentally benign batteries based on organic radical polymers". Pure and Applied Chemistry. 81 (11): 1961-1970. 15 Ekim 2009. doi:10.1351/PAC-CON-08-12-03. ISSN 1365-3075. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Nanostructured Conjugated Polymers: Toward High-Performance Organic Electrodes for Rechargeable Batteries". ACS Energy Letters (İngilizce). 2 (9): 1985-1996. 8 Eylül 2017. doi:10.1021/acsenergylett.7b00494. ISSN 2380-8195. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Polymer Electrode Materials for Sodium-ion Batteries". Materials (İngilizce). 11 (12): 2567. 17 Aralık 2018. doi:10.3390/ma11122567. ISSN 1996-1944. PMC 6315866 $2. PMID 30562972. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "The excellent cycling stability and superior rate capability of polypyrrole as the anode material for rechargeable sodium ion batteries". RSC Advances (İngilizce). 6 (3): 2345-2351. 2016. doi:10.1039/C5RA22607D. ISSN 2046-2069. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Non-crystalline oligopyrene as a cathode material with a high-voltage plateau for sodium ion batteries". Journal of Power Sources (İngilizce). 254: 73-79. May 2014. doi:10.1016/j.jpowsour.2013.12.104. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ a b "The impact of the molecular weight on the electrochemical properties of poly(TEMPO methacrylate)". Polymer Chemistry (İngilizce). 8 (11): 1815-1823. 2017. doi:10.1039/C7PY00151G. ISSN 1759-9954. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "A rechargeable battery based on hydrophilic radical polymer electrode and its green assessment". Green Chemistry Letters and Reviews (İngilizce). 2 (3): 169-174. September 2009. doi:10.1080/17518250903251775. ISSN 1751-8253. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım)