Amino asitler, proteinleri oluşturan temel yapı taşlarıdır.

Karbonhidrat, karbon (C), hidrojen (H) ve oksijen (O) atomlarından oluşan, genellikle hidrojen-oksijen atomu oranı (suda) 2:1 olan bir biyomoleküldür ve dolayısıyla ampirik (deneysel) formülü Cm(H2O)n şeklindedir. m, n'den farklı da olabilir olmaya da bilir. Ancak, tüm karbonhidratlar bu kesin stokiyometrik tanıma uymaz (örneğin üronik asitler, fukoz gibi deoksi şekerler) ve bu tanıma uyan tüm kimyasallar otomatik olarak karbonhidratlar (örneğin formaldehit ve asetik asit) olarak sınıflandırılmaz.

Aldehitler, yapılarında karbonil grubuna bağlı bir hidrojenin olduğu organik bileşiklerdir. Düşük karbonlu aldehitler polar moleküller olup düşük ve yoğun fazlarda hidrojen bağı içermezler. Aynı karbon sayılı ketonlara göre kaynama noktası aldehitlerde daha yüksektir.

Alkol, karbon atomuna doğrudan bir -OH (hidroksil) grubunun bağlı olduğu organik bileşiklere verilen genel ad. Genel formülü CnH2n+1OH olan mono alkoller, alkollerin önemli bir sınıfıdır. Bunlardan etanol (C2H5OH), alkollü içeceklerde bulunan türüdür. Genellikle alkol kelimesi ile etanol kastedilir ki yeni fermente olmuş birada etanol oranı %3-5 arasında iken şarapta %12-15 arasındadır.
Kimya ve biyokimyada, yağ asidi, genelde uzun, alifatik kuyruklu bir karboksilik asittir. Uzun karboksilik yağ asitlerinden 4 karbonlu ve daha uzun zincirlileri yağ asidi olarak sayılır; doğal yağları (trigliseritleri) oluşturan yağ asitlerinden söz ederken ise bunların en az 8 karbonlu olduğu varsayılabilir. Çoğu doğal yağ asitlerinin çift sayılı karbon atomu vardır, çünkü bunların biyolojik sentezlerinde iki karbon atomlu asetat kullanılır.

Talyum, periyodik element tablosunda 3A grubunda yer alan, atom numarası 81, atom ağırlığı 204,39 olan metal elementi.

Lantan, La sembolü ile bilinen, atom no: 57 ve atom ağırlığı: 138.92 olan kimyasal element.

Karboksilik asitler karboksil grubu olan organik asitlerdir, -C(=O)OH formülüne sahiptirler, bu genelde -COOH veya CO2H olarak da yazılır. Karboksilik asitler Bronsted asitleridir, yani proton vericileridir. Karboksilik asitlerin tuz ve anyonlarına karboksilat denir. Karboksilik asitler, esterlerle fonsiyonel grup izomeridirler. Karboksilik asitlerin en basit dizisi alkanoik asitlerdir, R-COOH formülüyle gösterilirler, R bir hidrojen atomu veya bir alkil grubuna karşılık gelir. Bileşiklerde birden fazla karboksilik asit grubu bulunabilir.
Dikarboksilik asitler, iki karboksilik asit fonksiyonel grubu ile ornatılmış organik bileşiklerdir. Dikarboksilik asit için moleküler formüllerde bu gruplar çoğu zaman HOOC-R-COOH olarak yazılır, burada R genelde bir alkil, alkenil veya alkinil gruptur. Dikarboksilik asitler naylon ve polietilen tereftalat gibi kopolimerler hazırlamak için kullanılırlar.

Formik asit, HCOOH, tek karbonlu karboksilik asittir. Metanoik asit olarak da bilinir. Formik asit, karbonil karbonuna bağlı alkil grubu içermemesiyle en basit karboksilli asit özelliği taşır. Hem aldehit hem de karboksilik asit özelliğine sahiptir.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Salen, organometalik kimyada ve koordinasyon kimyasında kullanılan bir bileşiktir. İsmi salisilik aldehit ve etilendiamin kelimelerinin birleşmesinden meydana gelen bir kısaltmadır, çünkü bu bileşiklerin birleşmesi ile oluşmaktadır.
Eritroz, C4H8O4 formülüne sahip bir tetrozdur. Bu bileşiğin her molekülünde bir aldehit grubu bulunmaktadır. Bu nedenle eritroz bir aldozdur. Maddenin doğal izomerinin adı D-eritroz'dur.

Astrokimya, dünya dışında bulunan kimyasal elementleri, kimyasal maddeleri ve bu maddelerin birbirine etkisini tahribatını genellikle Güneş Sistemi'nden daha geniş alanlarda özellikle moleküler gaz bulutlarında inceleyen bir bilim. Bu nedenle astrokimya, astronomi ve kimya bilimlerinin birleşmesidir. Güneş sistemi genişliğindeki incelemelere "kozmokimya" denmektedir.
Organik reaksiyonlar, organik maddelerin tepkimelerine verilen genel addır.
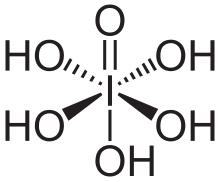
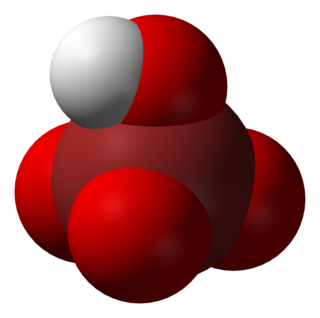
Periyodik asit iyotun en yüksek oksoasitidir. Bütün periodatlar gibi iki form halinde var olur: H5IO6 formülü ile gösterilen ortoperiyodik asit ve HIO4 formüllü ile gösterilen metaperiyodik asit.

Auramin O florensan boya olarak kullanılan bir diarilmetan boya. Saf halinde sarı iğne kristalleri olarak görünür. Suda ve etanolde oldukça iyi çözünür..
Perbromik asit, HBrO4 formülüne sahip bir inorganik bileşiktir. Bir brom oksoasitidir. Perbromik asit kararsızdır ve periyodik asit hazırlandıkça klorun perklorik asitten yer değiştirmesi ile oluşturulamaz; sadece perbromat iyonunun protonlanması ile yapılabilir.
Karboksilik asitlerden 3C'a sahip olan propiyonik asit içerdiği hidrojen bağları ile güçlü olup kaynama noktası diğer fonksiyonel gruplardan (sırasıyla) Alkol-Keton-Aldehit-Eter büyüktür. Propionik asit CH3CH2CO2H kimyasal formülüne sahip doğal olarak oluşan bir karboksilik asittir. Vücut kokusuna benzeyen keskin ve hoş olmayan bir kokuya sahip bir sıvıdır. CH3CH2CO2− anyonu ile propiyonik asidin tuzları ve esterleri, propiyonatlar veya propanoatlar olarak bilinir.

İdoz, bir heksoz, yani altı karbonlu bir monosakkarittir. Bir aldehit grubuna sahiptir ve bir aldozdur. Doğada bulunmaz ancak içerdiği üronik asit ve iduronik asit önemlidir. Glikozaminoglikanlar olan dermatan sülfat ve heparan sülfatın bir bileşenidir. Birinci ve üçüncü hidroksil grupları, ikinci ve dördüncü konum hidroksillerine zıt bir konumda düzenlenir. İdoz, D- ve L- 'nin aldol kondenzasyonu ile elde edilebilir. L-idoz, D - glukozun bir epimeridir.