
Fotosentez, bitkiler ve diğer canlılar tarafından, ışık enerjisini organizmaların yaşamsal eylemlerine enerji sağlamak için daha sonra serbest bırakılabilecek kimyasal enerjiye dönüştürmek için kullanılan bir işlemdir. Bu kimyasal enerji, karbondioksit ve sudan sentezlenen şekerler gibi karbonhidrat moleküllerinde depolanır.

Fermantasyon, hücre içinde oksijen yokluğunda meydana gelen metabolik bir faaliyet olarak ‘NAD+'yi yeniden oluşturmak için glikozun glikoliz yoluyla kısmi oksidasyonunu takip eden metabolik adımlar’ şeklinde tanımlanmaktadır. Fermantasyon anaerobik şartlarda, yani oksidatif fosforilasyon olamadığı durumlarda, glikoliz yoluyla ATP üretimini sağlayan önemli bir biyokimyasal süreçtir. Biyokimyanın fermantasyonla ilgilenen dalı zimolojidir.

Glikoliz, glikozun enzimlerle pirüvik asite (pirüvat) kadar yıkılması olayıdır. Bütün canlılarda glikoliz reaksiyonları aynı şekilde gerçekleşir çünkü olaylar için tüm canlılarda aynı enzimler görevlidir. Başlangıçta glikozu aktifleştirmek için 2 ATP harcanır. Reaksiyonlar sırasında 4 ATP(Adenozin tri fosfat) oluşturulur. 2 NADH meydana gelir. Oluşan NADH'lar oksijenli solunumda elektron taşıma sistemine aktarılır ve her birinden üçer ATP elde edilir. Oksijensiz solunumda ise NADH'lar son ürün evresinde tekrar yükseltgenerek bir sonraki glikoliz olayında kullanılır. Kısacası glikolizde substrat düzeyinde fosforilasyonla 4 ATP üretilir. Ve 2ATP harcandığı için net kazanç 2 ATP 'dir. Ancak oluşan 2NADH iyonundan dolaylı olarak 6 ATP(Adenozin tri fosfat)ETS'den kazanılır.

'Adenozin trifosfat, hücre içinde bulunan çok işlevli bir nükleotittir. İngilizce Adenosine Triphosphateden ATP olarak kısaltılır. En önemli işlevi hücre içi biyokimyasal reaksiyonlar için gereken kimyasal enerjiyi taşımaktır. Fotosentez ve hücre solunumu sırasında oluşur. ATP bunun yanı sıra RNA sentezinde gereken dört monomerden biridir. Ayrıca ATP, hücre içi sinyal iletiminde protein kinaz reaksiyonu için gereken fosfatın kaynağıdır. 3 tane fosfattan oluşur.

Yadımlama veya katabolizma, enerjice zengin ve büyük moleküllü moleküllerin daha küçük moleküllere parçalanması olayı ve bu işlemler sürecidir. Yani metabolizmanın yıkım aşamaları olarak da genellenebilir. Katabolizma kapsamında besin maddeleri niteliğinde olan uzun moleküllerin hücre içinde enzimlerin katalizörlüğünde parçalanarak, molekül bağlarında depolanmış enerji açığa çıkarılıp kullanılır.
Oksidatif fosforilasyon, canlılarda enerji kaynağı olarak kullanılan ATP sentezinde kullanılan yollardan biridir. Fosforilasyon olarak da adlandırılan ATP sentezi başlıca dört yoldan gerçekleştirilir.
- Oksidatif fosforilasyon
- Substrat düzeyinde fosforilasyon
- Fotofosforilasyon (fotosentezde)
- Kemofosforilasyon (kemosentezde)

Oksijenli solunum, organik besinlerden oksijen yoluyla ATP elde etme işidir. Hücrelerdeki bazı kimyasal tepkimelerde kullanılan enerjinin oksijen kullanılarak açığa çıkarılması demektir. Biyoloji ders kitapları sık sık hücresel solunum sırasında glikoz molekülü başına 38 ATP molekülü üretildiğini söylese de sızıntılı zarların yanı sıra mitokondriyal matrikse pirüvat ve ADP hareketinin maliyetinden dolayı %100 verim olamayacağından bu sayıya asla ulaşılmaz, mevcut tahminler glikoz başına 29 ilâ 30 ATP dolayındadır.

Etanol fermantasyonu, solunumda oksijen kullanmayan canlılar için bir fermantasyon biçimidir.

Laktik asit fermantasyonu, oksijen yetersizliğinde bazı bakteri ve hayvan hücrelerinde görülen bir fermantasyon biçimidir.

Nikotinamid adenin dinükleotid (NAD+) hücrelerde bulunan önemli bir koenzimdir. Elektron taşıyarak indirgenme potansiyelinin moleküller arasında aktarılmasında rol oynar.

Krebs döngüsü, trikarboksilik asit döngüsü veya sitrik asit döngüsü, canlı hücrelerin besinleri yükseltgeyerek enerji elde etmesini sağlayan ve bütün yaşam biçimlerinde önemli bir yer tutan kimyasal süreçlerin son aşamasıdır. TCA devri olarak da bilinir. 1937'de Hans Adolf Krebs tarafından açıklığa kavuşturulan tepkimelerin hayvan, bitki, mikroorganizma ve mantar gibi birçok hücre türünde oluştuğu saptanmıştır.
Anaerobik solunum veya oksijensiz solunum, oksijen (O2) yerine ETS elemanlarının kullanılıp oksidasyon (yükseltgenme) sonucu ATP elde edilmesidir. Aerobik solunum (Oksijenli solunum) ile temel farkı, oksijen kullanılmamasıdır. Fermantasyon ile karıştırılmamalıdır. Anaerobik solunum yapan mikroorganizmalarda elektron taşıma zincirinin sonunda elektron alıcısı olarak oksijen yerine sülfat (SO4), nitrat (NO3) veya kükürt (S) kullanılır. Moleküler oksijenin elektron alma isteğine oranla bu maddelerin elektron alma isteği daha az olduğundan oksijeniz solunumda ortama verilen enerji de oksijenli solunumdan daha düşüktür.
Seçmeli anaerobik canlı veya fakültatif anaerobik canlı, eğer oksijen varsa aerobik solunum ile ATP yapan, yoksa fermantasyon yoluna geçebilen bir canlı. Buna karşın zorunlu anaeroblar oksijen varlığında ölürler.

C4 karbon tutulumu mekanizması veya C4 bitkileri kara bitkilerinin fotosentezinde karbondioksiti bağlayan ve şeker oluşturan C3 karbon tutulumu mekanizması ve CAM bitkileri mekanizmaları gibi işleyen biyokimyasal mekanizmalardan biridir.

Mayalar ökaryot, tek hücreli, fungi (mantarlar) alemi içerisinde sınıflandırılan mikroorganizmalardır. Kökenleri 300 milyon yıl öncesine kadar uzanmaktadır ve bilinen en az 1500 türü bulunmaktadır. Tanımlanmış tüm mantar türlerinin tahminen %1'i mayalardır. Mayalar çok hücreli atalardan evrimleşmiş, tek hücreli organizmalardır, fakat bazı türleri, pseudohif olarak bilinen, birbirine zincirleme eklenen tomurcuklanmış hücre dizileri oluşturarak, çok hücreli organizma benzeri özellikler gösterme yeteneğine sahiptirler. Maya hücreleri, türe ve çevresel ortama göre, genellikle 3–4 µm (mikrometre) olsalar da, 40 µm'ye kadar varan farklı boyutlarda olabilirler.
Biyokimyada metabolik yolak veya metabolik patika, hücre içinde meydana gelen bir dizi kimyasal tepkimedir; Bunlar toplu olarak metabolizmayı oluştururlar. Her bir yolakta belli bir kimyasal bileşik, enzimler tarafından değişime uğrar. Bazı metabolik yolaklarda pek çok bileşik ve enzim yer aldığı için bunlar çok karmaşık olabilir. Hücrelerde pek çok yolak bulunur, bunlar ortak bileşiklerde kesiştikleri için karmaşık ağlar oluşturabilirler, bunlara metabolik ağ denir. Metabolik yolaklar organizmalarda homeostaz sağlamakta rol oynar.
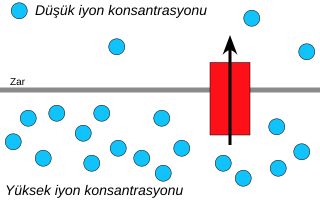
Kemiosmoz; iyonların, elektrokimyasal gradyanı azaltmak için seçici geçirgen bir zardan geçme hareketidir. Hücresel solunumdaki ATP sentezinin gerçekleşmesini sağlayan enerjinin büyük bir kısmı hidrojenlerin yaptığı bu hareketten karşılanır.

Hidrojen siyanür, HCN formüllü inorganik bir bileşiktir. Endüstriyel ölçekte üretilen HCN, polimerlerden ilaçlara kadar birçok kimyasal bileşik için oldukça değerli bir öncüdür. Büyük ölçekli uygulamalar, sırasıyla madencilik ve plastikte kullanılan potasyum siyanür ve adiponitril üretimi içindir. Hidrojen siyanür, 25 °C'de kaynayan renksiz acıbadem kokusunda bir sıvıdır. Uçucu bir sıvı olduğundan, katı siyanür bileşiklerinden daha zehirlidir.

Şarap yapımında fermantasyon süreci üzüm suyunu alkollü içeceğe dönüştürür. Fermentasyon sırasında, maya meyve suyunda bulunan şekeri etanol ve karbon dioksit'e dönüştürür. Şarapçılık'ta fermantasyonun başlangıcında şıradadaki oksijen seviyesinin yanı sıra fermantasyon sıcaklığı ve hızı da önemli hususlardır. Sıkışmış fermantasyon ve birkaç şarap hata gelişme riski de bu aşamada oluşabilir ki bu "birincil fermantasyon" için 5 ila 14 gün arasında ve potansiyel olarak ikincil fermantasyon için 5 ila 10 gün daha sürebilir. Fermantasyon, Riesling gibi birçok beyaz şarapta yaygın olan paslanmaz çelik tanklarda, açık ahşap fıçıda, şarap fıçısında ve birçok köpüklü şarap'ın üretiminde olduğu gibi şarap şişesinin içinde de yapılabilir.
Enzim aktivatörleri, enzimlere bağlanan ve onların aktivitelerini artıran moleküllerdir. Bu moleküller enzim inhibitörlerinin tam tersi olarak görev yapar ve çoğunlukla allosterik düzenlemeler yoluyla metabolizmanın kontrol edilmesini sağlarlar. Bu şekilde işlev gören bir enzim aktivatörü olan fruktoz 2,6-bisfosfat, fosfofruktokinaz 1'i aktive eder ve glukagon hormonuna yanıt olarak glikolizin artmasına neden olur. Bazı durumlarda, eğer bir substrat bir enzimin katalitik alt birimine bağlanırsa, enzimin diğer alt birimlerinde hem substrat afinitesinde hem de katalitik aktivitede artışa yol açarak bir aktivatör olarak işlev görebilir.















