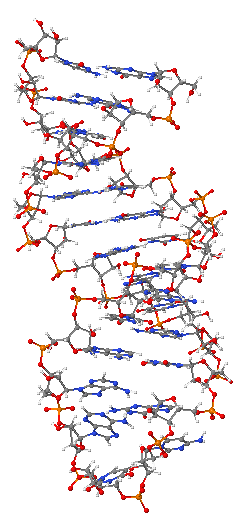
Oligonükleotit
Oligonükleotitler, genetik test, araştırma ve adli tıpta geniş bir uygulama alanına sahip olan kısa DNA veya RNA molekülleri, oligomerleridir. Laboratuvarda katı faz kimyasal sentezi ile[1] yaygın olarak yapılan bu küçük nükleik asit bitleri, herhangi bir kullanıcı tanımlı diziye sahip tek sarmallı moleküller olarak üretilebilir ve bu nedenle yapay gen sentezi polimeraz zincir reaksiyonu (PCR) DNA dizileme moleküler klonlama ve moleküler problar için hayati öneme sahiptir. Doğada oligonükleotitler genellikle gen ekspresyonunun düzenlenmesinde (örneğin mikroRNA) işlev gören küçük RNA molekülleri olarak bulunur veya daha büyük nükleik asit moleküllerinin parçalanmasından türetilen bozunma ara maddeleri olarak bulunur.
Oligonükleotitler, tüm molekülü oluşturan nükleotit artıkları dizisi ile karakterize edilir. Oligonükleotitin uzunluğu genellikle "-mer" ile gösterilir (Yunanca meros'tan "kısım"). Örneğin, altı nükleotitden (nt) oluşan bir oligonükleotit bir heksamer iken 25 nt'den biri genellikle "25-mer" olarak adlandırılır. Oligonükleotitler, daha yüksek sıralı çiftler veya daha az sıklıkla melezler oluşturmak için kendi tamamlayıcı oligonükleotitleri DNA veya RNA'ya sekansa özgü bir şekilde kolayca bağlanır. Bu temel özellik, oligonükleotitlerin spesifik DNA veya RNA sekanslarını tespit etmek için problar olarak kullanılması için bir temel görevi görür. Oligonükleotitleri kullanan prosedürlerin örnekleri arasında DNA mikro dizileri Southern blot ASO analizi floresan in situ hibridizasyon (FISH) PCR ve yapay genlerin sentezi yer alır.
Oligonükleotitler, farklı farmakolojik etkiler elde etmek için omurgada veya 2' şeker konumunda modifiye edilebilen 2'-deoksiribonükleotitlerden (oligodeoksiribonükleotitler) oluşur. Bu modifikasyonlar, oligonükleotitlere yeni özellikler kazandırır ve onları antisens terapisinde anahtar bir unsur haline getirir.[2][3]
Sentezi
Oligonükleotitler, doğal veya kimyasal olarak modifiye edilmiş nükleositlerin yapı blokları korumalı fosforamiditleri veya daha az ölçüde nükleozidik olmayan bileşikler kullanılarak kimyasal olarak sentezlenir. Oligonükleotit zincir düzeneği, "sentetik döngü" olarak adlandırılan rutin bir prosedürü takip ederek 3 'ila 5' yönünde ilerler. Tek bir sentetik döngünün tamamlanması, büyüyen zincire bir nükleotit kalıntısının eklenmesi ile sonuçlanır. Her sentetik aşamadan% 100'den az verim ve yan reaksiyonların meydana gelmesi, işlemin verimliliğinin pratik sınırlarını belirler. Genel olarak oligonükleotit dizileri genellikle kısadır (13-25 nükleotit uzunluğunda).[4] Sentetik oligonükleotitlerin maksimum uzunluğu, 200 nükleotit kalıntısını hemen hemen geçmez. Ürünleri istenen sekansla izole etmek için HPLC ve diğer yöntemler kullanılabilir.
Kimyasal modifikasyonlar
Kimyasal olarak kararlı kısa oligonükleotitlerin oluşturulması, ASO tedavilerinin geliştirilmesindeki en erken zorluktu. Doğal olarak oluşan oligonükleotitler, nükleotitleri parçalayan ve her hücre tipinde bol miktarda bulunan bir enzim olan nükleazlar tarafından kolayca parçalanır.[5] Kısa oligonükleotit sekansları ayrıca, in vivo bozunmalarına katkıda bulunan zayıf iç bağlanma afinitelerine sahiptir.[6]
Omurga modifikasyonları
nükleotitlerin nükleosit organotiofosfat (PS) analogları, oligonükleotitlere bazı yararlı özellikler verir. PS omurgalarının nükleotitlere verdiği temel yararlı özellikler, her nükleotitin diastereomer tanımlanması ve oligonükleotit sentezinde faydalı olan fosforotioat nükleotitleri içeren reaksiyonları kolayca takip etme kabiliyetidir.[7] Oligonükleotitlere yapılan PS omurga modifikasyonları, onları enzimler tarafından istenmeyen bozunmaya karşı korur.[8] nükleotit omurgasının modifiye edilmesi, çoğu nükleotitde görece kolaylık ve doğrulukla elde edilebildiği için yaygın olarak kullanılmaktadır.[7]
Şeker halkası modifikasyonları
Oligonükleotitlerin tıbbi uygulamaları için yararlı olan başka bir modifikasyon, 2'şeker modifikasyonlarıdır. 2'pozisyonundaki şekerin modifiye edilmesi, oligonükleotitlerin spesifik olarak antisens oligonükleotit terapilerinde hedef bağlanma yeteneklerini geliştirerek oligonükleotitlerin etkinliğini arttırır. Ayrıca spesifik olmayan protein bağlanmasını azaltarak spesifik proteinleri hedeflemenin doğruluğunu artırır. En yaygın kullanılan modifikasyonlardan ikisi 2'-O-metil ve 2'-O-metoksietildir.[6]
Antisens oligonükleotitler
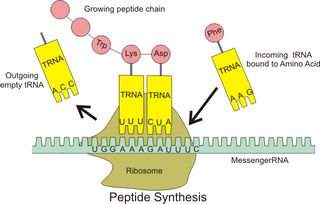
Antisens oligonükleotitler, seçilen bir diziye tamamlayıcı olan tek DNA veya RNA zincirleridir.[4] Antisens RNA durumunda, hibridizasyon adı verilen bir işlemle onlara bağlanarak belirli haberci RNA zincirlerinin protein translasyonunu önlerler.[9] Antisens oligonükleotitler, spesifik bir tamamlayıcı (kodlayan veya kodlamayan) RNA'yı hedeflemek için kullanılabilir. Bağlanma meydana gelirse, bu hibrit, RNaz H enzimi tarafından parçalanabilir.[9] RNaz H, RNA'yı hidrolize eden bir enzimdir ve bir antisens oligonükleotit uygulamasında kullanıldığında, mRNA ifadesinin% 80-95 oranında aşağı regülasyonu ile sonuçlanır.[4]
Morfolino antisens oligonükleotitlerinin, artık gelişimsel biyolojide standart bir teknik olan ve değiştirilmiş gen ekspresyonunu ve gen fonksiyonunu incelemek için kullanılan omurgalılarda gen nakavtları için kullanımı, ilk olarak Janet Heasman tarafından Xenopus kullanılarak geliştirildi.[10] FDA onaylı Morpholino ilaçları arasında eteplirsen ve golodirsen bulunur. Antisens oligonükleotitler, hücre hatlarında influenza virüsü replikasyonunu inhibe etmek için de kullanılmıştır.[11][12]
Tek bir mutant proteinin sonucu olan nörodejeneratif hastalıklar, yüksek seçicilikle çok spesifik RNA dizilerini hedefleme ve modifiye etme yeteneklerinden dolayı antisens oligonükleotit terapileri için iyi hedeflerdir. Huntington hastalığı, Alzheimer hastalığı, Parkinson hastalığı ve amyotrofik lateral skleroz (ALS) dahil olmak üzere birçok genetik hastalık, yanlış RNA dizilerine neden olan ve toksik fizyolojik etkiye sahip yanlış çevrilmiş proteinlerle sonuçlanan DNA değişiklikleriyle ilişkilendirilmiştir.[13]
Analitik teknikler
Kromatografi
Alkilamidler, kromatografik sabit fazlar olarak kullanılabilir.[14] Bu fazlar, oligonükleotitlerin ayrılması için araştırılmıştır.[15]
Kütle spektrometrisi
MALDI kütle spektrometresinde oligonükleotit analizi için bir matris olarak 5-metoksisalisilik asit ve spermin karışımı kullanılabilir.[16]
DNA mikrodizisi
DNA mikro dizileri, oligonükleotitlerin yararlı bir analitik uygulamasıdır. Standart cDNA mikrodizileriyle karşılaştırıldığında, oligonükleotit bazlı mikrodiziler, hibridizasyona göre daha kontrollü özgüllüğe ve alternatif olarak eklenmiş veya poliadenile dizilerin varlığını ve yaygınlığını ölçme kabiliyetine sahiptir.[17] DNA mikrodizilerinin bir alt tipi, oligonükleotitlerin yüksek yoğunlukta bağlandığı substratlar (naylon, cam vb.) Olarak tanımlanabilir.[18] Yaşam bilimleri içinde DNA mikrodizilerinin bir dizi uygulaması vardır.
Kaynakça
- ^ Yang J, Stolee JA, Jiang H, Xiao L, Kiesman WF, Antia FD, Fillon YA, Ng A, Shi X (Ekim 2018). "Solid-Phase Synthesis of Phosphorothioate Oligonucleotides Using Sulfurization Byproducts for in Situ Capping". The Journal of Organic Chemistry. 83 (19): 11577-11585. doi:10.1021/acs.joc.8b01553. PMID 30179468.
- ^ Weiss, B., ed. (1997). Antisense Oligodeoxynucleotides and Antisense RNA : Novel Pharmacological and Therapeutic Agents. Boca Raton, Florida: CRC Press
- ^ Weiss B, Davidkova G, Zhou LW (1999). "Antisense RNA gene therapy for studying and modulating biological processes". Cellular and Molecular Life Sciences. 55 (3): 334-58. doi:10.1007/s000180050296. PMID 10228554.
- ^ a b c Dias N, Stein CA (Mart 2002). "Antisense oligonucleotides: basic concepts and mechanisms". Molecular Cancer Therapeutics. 1 (5): 347-55. PMID 12489851. 5 Ağustos 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Kasım 2020.
- ^ Frazier KS (Ocak 2015). "Antisense oligonucleotide therapies: the promise and the challenges from a toxicologic pathologist's perspective". Toxicologic Pathology. 43 (1): 78-89. doi:10.1177/0192623314551840. PMID 25385330.
- ^ a b DeVos SL, Miller TM (Temmuz 2013). "Antisense oligonucleotides: treating neurodegeneration at the level of RNA". Neurotherapeutics. 10 (3): 486-97. doi:10.1007/s13311-013-0194-5. PMC 3701770 $2. PMID 23686823.
- ^ a b Eckstein F (Nisan 2000). "Phosphorothioate oligodeoxynucleotides: what is their origin and what is unique about them?". Antisense & Nucleic Acid Drug Development. 10 (2): 117-21. doi:10.1089/oli.1.2000.10.117. PMID 10805163.
- ^ Stein CA, Subasinghe C, Shinozuka K, Cohen JS (Nisan 1988). "Physicochemical properties of phosphorothioate oligodeoxynucleotides". Nucleic Acids Research. 16 (8): 3209-21. doi:10.1093/nar/16.8.3209. PMC 336489 $2. PMID 2836790.
- ^ a b Crooke ST (Nisan 2017). "Molecular Mechanisms of Antisense Oligonucleotides". Nucleic Acid Therapeutics. 27 (2): 70-77. doi:10.1089/nat.2016.0656. PMC 5372764 $2. PMID 28080221.
- ^ Heasman J, Kofron M, Wylie C (Haziran 2000). "Beta-catenin signaling activity dissected in the early Xenopus embryo: a novel antisense approach". Developmental Biology. 222 (1): 124-34. doi:10.1006/dbio.2000.9720. PMID 10885751.
- ^ Kumar P, Kumar B, Rajput R, Saxena L, Banerjea AC, Khanna M (Kasım 2013). "Cross-protective effect of antisense oligonucleotide developed against the common 3' NCR of influenza A virus genome". Molecular Biotechnology. 55 (3): 203-11. doi:10.1007/s12033-013-9670-8. PMID 23729285.
- ^ Kumar B, Khanna M, Kumar P, Sood V, Vyas R, Banerjea AC (Mayıs 2012). "Nucleic acid-mediated cleavage of M1 gene of influenza A virus is significantly augmented by antisense molecules targeted to hybridize close to the cleavage site". Molecular Biotechnology. 51 (1): 27-36. doi:10.1007/s12033-011-9437-z. PMID 21744034.
- ^ Smith RA, Miller TM, Yamanaka K, Monia BP, Condon TP, Hung G, Lobsiger CS, Ward CM, McAlonis-Downes M, Wei H, Wancewicz EV, Bennett CF, Cleveland DW (Ağustos 2006). "Antisense oligonucleotide therapy for neurodegenerative disease". The Journal of Clinical Investigation. 116 (8): 2290-6. doi:10.1172/JCI25424
 . PMC 1518790 $2. PMID 16878173.
. PMC 1518790 $2. PMID 16878173. - ^ Buszewski B, Kasturi P, Gilpin RK, Gangoda ME, Jaroniec M (Ağustos 1994). "Chromatographic and related studies of alkylamide phases". Chromatographia. 39 (3–4): 155-61. doi:10.1007/BF02274494.
- ^ Buszewski B, Safaei Z, Studzińska S (Ocak 2015). "Analysis of oligonucleotides by liquid chromatography with alkylamide stationary phase". Open Chemistry. 13 (1). doi:10.1515/chem-2015-0141
 .
. - ^ Distler AM, Allison J (Nisan 2001). "5-Methoxysalicylic acid and spermine: a new matrix for the matrix-assisted laser desorption/ionization mass spectrometry analysis of oligonucleotides". Journal of the American Society for Mass Spectrometry. 12 (4): 456-62. doi:10.1016/S1044-0305(01)00212-4. PMID 11322192.
- ^ Relógio A, Schwager C, Richter A, Ansorge W, Valcárcel J (Haziran 2002). "Optimization of oligonucleotide-based DNA microarrays". Nucleic Acids Research. 30 (11): e51. doi:10.1093/nar/30.11.e51. PMC 117213 $2. PMID 12034852.
- ^ Gong P, Harbers GM, Grainger DW (Nisan 2006). "Multi-technique comparison of immobilized and hybridized oligonucleotide surface density on commercial amine-reactive microarray slides". Analytical Chemistry. 78 (7): 2342-51. doi:10.1021/ac051812m. PMID 16579618.