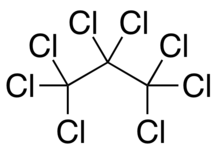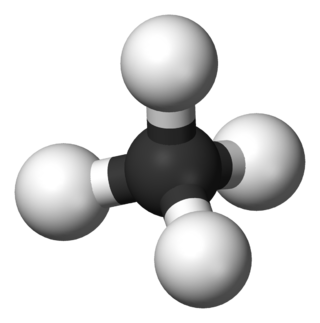
Hidrokarbon, sadece karbon ve hidrojen atomlarından oluşan kimyasal bileşiklerin genel adı.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.

Alkanlar, (diğer bir deyişle Parafinler) sadece karbon (C) ve hidrojen (H) elementlerinin bulunduğu ve bu elementlerin birbirleriyle tekli bağ yaptığı doymuş alifatik organik bileşiklerin genel ismidir. Alkanlar birbirlerini 1 karbon ve 2 hidrojen ile takip eden bir homolog seri oluştururlar. Örneğin tek karbonlu metan, CH4 formülüne sahipken, çift karbonlu etan C2H6 kapalı formülüne sahiptir. Alkanlarda tüm atomlar tekli bağlarla birbirlerine bağlandığı ve Karbon atomunu bağlayabileceği en fazla Hidrojen atomunu bağladığından dolayı doymuş bileşikler kategorisine girerler. Doymuş hidrokarbonlardan olan alkanlar, CnH2n+2 n=1,2,3,.... genel formülüne sahiptir. Burada n'in 3 veya 3'ten büyük olması hâlinde sikloalkan denilen halkalı yapılar oluşabilmektedirler.

Alkenler yapılarında en az bir tane karbon-karbon (C=C) çift bağı içeren organik bileşiklerdir. Alkenlerin yapısında karbon-karbon çift bağı bulunduğundan ve bu karbonların yapabileceği en fazla hidrojenle bağ yapmamış olduğundan alkenler doymamış bileşikler kategorisine girerler. Alkenlerin yapısında sadece bir karbon-karbon çift bağının bulunması durumunda homolog seriler oluşturur. Bu homolog serilerin genel formülü CnH2n şeklindedir. Burada n-in en az 2 olma şartı vardır. Aşağıda en basit alken olan eten, yaygın ismiyle etilenin, çeşitli modellemelerle çizilmiş şekillerinin yanı sıra alkenlerin çeşitli şekillerdeki yazılış şekilleri de bulunmaktadır.

Grafit ya da karataş yumuşak, yağlı, kâğıt üzerinde iz bırakan, gri-siyah renkli katı bir maddedir. Grafit, yağ haline getirilip makinelerde, çalışan parçaların birbirine sürtünürken aşınmasını azaltmak ya da engellemek amacıyla yağlayıcı olarak kullanılır. Adını, yazı yazmakta kullanılmasından almaktadır; "grafit" Yunanca grafein köküne, mineralleri belirtmekte kullanılan -it ekinin eklenmesiyle elde edilmiş bir sözcüktür. Kurşun kalemlerin içindeki uç, içine kil katılarak sertleştirilmiş grafittir.

Benzen, aren veya aromatik hidrokarbonlar olarak adlandırılan organik bileşikler sınıfının en basit üyesidir. Renksiz, yanıcı, kaynama noktası 80,1 °C, erime noktası 5,5 °C olan bir sıvıdır. Moleküler formülü C6H6'dır. Benzen, endüstriyel bakımdan değerli olduğu gibi yapısı bakımından da kimya çalışmalarında önemlidir. Kan hücrelerini öldürme etkisi olduğundan kanser yapıcı bileşikler arasına girer.

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.

Glisin (kısaltılmışı Gly ya da G) formülü NH2CH2COOH olan apolar bir aminoasittir. Glisin kodonları GGU, GGC, GGA, GGG cf. genetik koddur. Yapısal olarak proteinlerde bulunan 20 aminoasit arasında en basit olanıdır. Yan zinciri sadece bir hidrojen atomundan ibarettir. Glisindeki α-karbon atomu da bir hidrojene bağlı olduğu için, glisin optik olarak aktif değildir, diğer bir deyişle optik izomeri bulunmamaktadır.

Eterler, iki organik kısmın bir oksijen atomu üzerinden birbirine bağ yapmış organik moleküllerdir. Eterlerin genel formülü R-O-R' şeklindedir. Buradaki R ve R' aynı olabileceği gibi farklı organik kısımlar da olabilirler.

Diklorometan (DCM) ya da metilen klorür CH2Cl2 formülüne sahip bir organik bileşiktir. Renksiz, uçucu bir sıvıdır ve hoş kokuludur. Su ile karışmasa da biraz polardır ve birçok organik çözücüde çözünür. Çözücü olarak kullanılır.

Adamantan (İngilizce: adamantane); formülü C10H16, erime noktası 269 °C olan, hidrokarbonlarda iyi çözünen, hafif kâfur kokulu, renksiz kristal yapılı bir maddedir. Sikloalkan yapıda olan elmasımsı bir maddedir. Adamantan moleküllerinin karbon atomlarının uzaysal düzeni elmas kristalleri ile aynı yapıya sahiptir. Adamantan molekülleri "koltuk" konfigürasyonunda düzenlenmiş, birbirine bağlı dört sikloheksan halkasından oluşur. Adamantan molekülleri "kayık" konfigürasyonunda da bulunabilir.

Karbon tetraklorür ya da tetraklorometan, CCl4 formülüne sahip bir klorokarbon. Kokusu Kloroforma benzeyen, renksiz, yanıcı olmayan, sudan ağır bir sıvıdır. Suda çözünmezken birçok organik çözücü içinde çözünür. Geçmişte soğutucu gazların üretiminde, yangın söndürücülerde lav lambalarında, temizlik malzemesi ve kurt düşürücü olarak yaygın bir şekilde kullanılmıştır.
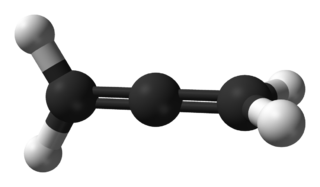
Propadien H2C=C=CH2 formülüne sahip organik bileşik. İki komşu C=C çift bağına sahip en basit bileşik ve allendir. MAPP gazının bir bileşeni olarak kaynak için yakıt olarak kullanılır.

İyot monoklorür ICl formülü ile gösterilen bir interhalojen bileşiktir. Oda sıcaklığına yakın eriyen kırmızı-kahverengi renge sahip bir kimyasal bileşiktir. İyot ve klorun elektronegatifliği arasındaki fark nedeniyle, ICl oldukça kutupsaldır ve I+ kaynağı olarak davranır.
İzopentan (C5H12),metilbütan ya da 2-metilbütan, beş karbon atomuna sahip bir dallanmış zincirli alkandır. İzopentan, oda sıcaklığında ve basıncında aşırı uçucu ve aşırı yanıcı bir sıvıdır. Aynı zamanda standart sıcaklık ve basınçta en az yoğun olan sıvıdır. Normal kaynama noktası oda sıcaklığından sadece birkaç derece yüksektir ve izopentan sıcak bir günde kolayca kaynamakta ve buharlaşmaktadır. İzopentan yaygın olarak sıvı azot ile birlikte -160 °C sıvı banyo sıcaklığına ulaşmak için kullanılır. Doğal gaz tipik olarak %1 veya daha az izopentan içerir.

Hekzaklorobütadien, C
4Cl
6 formülüne sahip, klorlu alifatik bir diendir. Oda sıcaklığında terebentin benzeri bir kokuya sahip, renksiz bir sıvıdır. En yaygını diğer klorlu bileşikler için çözücü olarak kullanılması olmak üzere özel uygulamaları bulunur.
Halometan bileşikleri, bir veya daha fazla hidrojen atomunun halojen atomları (flor, klor, brom veya iyot) ile değiştirildiği metan (CH4) türevleridir. Halometanlar hem özellikle deniz ortamlarında doğal olarak bulunurlar hem de özellikle soğutucu akışkanlar, çözücüler, itici gazlar ve fumigantlar olarak insan yapımıdır. Kloroflorokarbonlar da dâhil olmak üzere birçoğu, yüksek rakımlarda bulunan ultraviyole ışığa maruz kaldıklarında aktif hâle geldikleri ve Dünya'nın koruyucu ozon tabakasını incelttikleri için geniş ilgi gördü.

Küban,  formülüne sahip sentetik bir hidrokarbon bileşiğidir ve bir küpün köşelerinde düzenlenmiş sekiz karbon atomundan ve her bir karbon atomuna bağlı bir hidrojen atomundan oluşur. Katı kristal bir madde olan küban, Platonik hidrokarbonlardan biridir ve prizmanların bir üyesidir. İlk olarak 1964 yılında Philip Eaton ve Thomas Cole tarafından sentezlendi. Bu çalışmadan önce Eaton, "gerekli 90 derecelik bağ açıları" nedeniyle kübanın sentezlenmesinin imkânsız olacağına inanıyordu. Kübik şekil, karbon atomlarının, bir tetrahedral karbonun 109.45°'lik açısıyla karşılaştırıldığında oldukça gergin olan, alışılmadık derecede keskin bir 90°'lik bağlanma açısı benimsemesini gerektirir. Bir kez oluşturulduktan sonra küban, kolayca bulunabilen ayrışma yollarının olmaması nedeniyle kinetik olarak oldukça kararlıdır. Oktahedral simetriye sahip en basit hidrokarbondur.
formülüne sahip sentetik bir hidrokarbon bileşiğidir ve bir küpün köşelerinde düzenlenmiş sekiz karbon atomundan ve her bir karbon atomuna bağlı bir hidrojen atomundan oluşur. Katı kristal bir madde olan küban, Platonik hidrokarbonlardan biridir ve prizmanların bir üyesidir. İlk olarak 1964 yılında Philip Eaton ve Thomas Cole tarafından sentezlendi. Bu çalışmadan önce Eaton, "gerekli 90 derecelik bağ açıları" nedeniyle kübanın sentezlenmesinin imkânsız olacağına inanıyordu. Kübik şekil, karbon atomlarının, bir tetrahedral karbonun 109.45°'lik açısıyla karşılaştırıldığında oldukça gergin olan, alışılmadık derecede keskin bir 90°'lik bağlanma açısı benimsemesini gerektirir. Bir kez oluşturulduktan sonra küban, kolayca bulunabilen ayrışma yollarının olmaması nedeniyle kinetik olarak oldukça kararlıdır. Oktahedral simetriye sahip en basit hidrokarbondur.

Perklorometil merkaptan, CCl3SCl formülüne sahip organosülfür bileşiğidir. Esas olarak boyalar ve fungisitlerin (captan, folpet) üretiminde bir ara madde olarak kullanılır. Ticari numunelersarımsı renkte olmasına rağmen saf bileşik renksiz bir yağdır. Suda çözünmez fakat organik çözücülerde çözünür. Kötü, dayanılmaz, keskin bir kokusu vardır. Perklorometil merkaptan orijinal adıdır, sistematik adı triklorometansülfenil klorür olmalıdır çünkü bileşik bir merkaptan değil, bir sülfenil klorürdür.