
Kobalt kimyasal bir element'tir. Sembol'ü Co ve atom numarası 27'dir. Nikel gibi kobalt da, doğal meteorik demir alaşımlarında bulunan küçük birikintiler dışında, yer kabuğunda yalnızca kimyasal olarak birleşik formda bulunur. İndirgeyici eritme yoluyla üretilen serbest element sert, parlak, gümüş rengi bir metal'dir.

ANFO, madencilik ile inşaat sektöründe yaygın ve sıklıkla kullanılan, karışım halinde hazırlanan amonyum nitrat tabanlı bir patlayıcı türüdür.
Elektrokimya, kimya biliminin bir alt dalı olup elektronik bir iletken ile iyonik bir iletken (elektrolit) arayüzeyinde gerçekleşen reaksiyonları inceler. Elektrokimyada amaç kimyasal enerji ve elektrik enerjisi arasındaki değişimi incelemektir.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.
Titanyum grubu veya 4. grup periyodik tabloda yer alan bir kimyasal elementler grubudur. Modern IUPAC adlandırma sistemine göre periyodik tablonun 4. grubu titanyum (Ti), zirkonyum (Zr), hafniyum (Hf) and rutherfordiyum (Rf) elementlerini kapsar. Grup periyodik tablonun d bloku içinde yer alır. 4. grupta yer alan üç element titanyum (Ti), zirkonyum (Zr) ve hafniyum (Hf) doğal olarak bulunur buna karşın rutherfordiyum (Rf) radyoaktiftir. Rutherfordiyumun bütün izotopları radyoaktiftir ve laboratuvarda üretilirler, hiçbiri doğada bulunmaz. Şimdiye kadar süperçarpıştırıcılarda yapılan hiçbir deneyde grubun bir sonraki üyesi Unpentkuadyum (Upq) elemtinin sentezi gerçekleştirilemedi. 8. periyot elementlerinin sonlarında yer alan üyelerinden biri olduğundan Upq elementinin yakın bir gelecekte sentezlenmesi pek mümkün görünmemektedir.

Paslanmaz çelik, bileşiminde minimum %10,5 ve üzeri krom ve %1,2'den az karbon içeren ve korozyona karşı dayanıklılığı ile bilinen bir çelik alaşımıdır.

Amonyum klorür ya da daha çok bilinen adıyla Nişadır, formülü NH4Cl olan bir kimyasal bileşiktir. Suda yüksek oranda çözünen, beyaz kristallere sahip bir tuzdur. Amonyum klorür çözeltileri hafif asidiktir. Doğada mineral halde bazı volkan bacalarının etrafında bulunan haline sal amonyak denir. Bazı tür meyan ballarında bir aroma maddesi olarak kullanılır. Nişadır, hidroklorik asit ve amonyak arasında gerçekleşen reaksiyonla sonucu oluşur.

Aktinyum(III) oksit, az görülen radyoaktif element olan aktinyumun metalik oksitlenmesiyle oluşan bir bileşiktir. Aktinyum(III) oksitin formülü Ac2O3'tür. Bu oksit aktinyum oksalatın 1000-1100 derecede kızdırılmasıyla elde edilir. Lantan(III) oksit ile benzerlik gösterir. Hegzagonal ve kristal bir yapıya sahiptir. Yükseltgenme seviyesi +3'tür. Yoğunluğu 9.2g/ml, erime noktası 1977 °C dir. Görünümü beyazdır. Bu element Ac2O (Asetik anhidrit) ile karışmamalıdır. Buradaki Ac asetil grubunda bulunmaktadır. Diğer adları aktinyum seskioksit ile diaktinyum trioksittir.
Alkalin pil, çinko ve manganez dioksit (Zn / MnO2) arasındaki reaksiyona bağlı olarak birincil pil türüdür.

Çinko-karbon pil uygun bir elektrolit aracılı çinko ve manganez dioksit arasındaki elektrokimyasal tepkimelerden bir çinko metal elektrodu ile bir karbon çubuk arasında 1,5 volt potansiyel sağlayan kuru bir pildir. Genellikle uygun bir şekilde negatif potansiyele sahip anot görevi gören bir çinko kutu içinde, buna karşın atıl karbon çubuğu pozitif katotta paketlenir. Genel amaçlı piller muhtemelen bazı çinko klorür çözeltisi ile karıştırılmış amonyum klorür sulu bir macunu elektrolit olarak kullanılabilir. Ağır iş tiplerinde öncelikle çinko klorürden oluşan bir macun kullanılır.
İyot pentaoksit I2O5 formülü ile gösterilen kimyasal bileşiktir. Bu iyot oksit, iyot asidinin anhidriti ve iyotun tek kararlı oksididir. 200 °C'de kuru hava akımında iyodik asidi kurutmak suretiyle üretilir:
- 2HIO3 → I2O5 + H2O

Biyokütleden sıvıya, termokimyasal bir yolla biyokütleden yapılmış sentetik hidrokarbon yakıtların üretilmesi için çok aşamalı bir işlemdir. Böyle yakıtlara grassolin denir.

Kurşun monoksit olarak da adlandırılan kurşun(II) oksit, PbO moleküler formülüne sahip inorganik bileşiktir. PbO iki polimorfda oluşur: tetragonal kristal yapıya sahip litarj ve ortorombik kristal yapıya sahip massikot. PbO için modern uygulamalar çoğunlukla kurşun bazlı endüstriyel cam ve, bilgisayar bileşenlerini de kapsayan endüstriyel seramiklerdir. Amfoterik bir oksittir.

Henry Louis Le Chatelier, 19. yüzyılın sonlarında ve 20. yüzyılın başlarında yaşamış Fransız kimyagerdir. Değişen koşulların kimyasal dengedeki sistemler üzerindeki etkisini tahmin edebilmek için kimyagerler ve kimya mühendisleri tarafından kullanılan Le Chatelier ilkesini geliştirdi.

Gıda kimyası gıdada bulunan başlıca bileşenleri, gıdayı oluşturan renkleri, tatları ve meydana gelen reaksiyonlar gibi pek çok farklı konuları ele almaktadır.
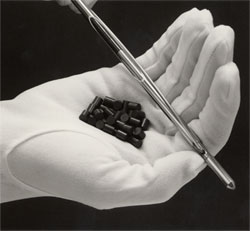
Uranyum Dioksit, diğer adıyla uranya kimyasal formülü UO2 olan maddedir. Neredeyse siyah renkli veya koyu kahverengi, radyoaktif ve kristal yapıda olan bir madde olup doğal olarak uraninit ve kleveyit minerallerinde bulunmaktadır. Nükleer santrallerde plütonyum ve uranyum dioksit karışımı yakıt çubuklarında kullanılmaktadır. Sarı ve siyah renkli seramiklerde 1960 yılına kadar kullanılmışlardır. Stoksiyometrik özelliklerine bağlı olarak erime sıcaklığı değişkendir.
Kalsinasyon, katı kimyasal bileşiklerin ısıl işlemine atıfta bulunur; bu sayede bileşik, genellikle safsızlığı veya uçucu maddeleri uzaklaştırmak ve/veya termal ayrışmaya maruz kalmak amacıyla, ortamdaki sınırlı oksijen kaynağı altında erimeden yüksek sıcaklığa yükseltilir.

Adını Octave Leopold Boudouard'dan alan Boudouard reaksiyonu, belirli bir sıcaklıkta karbon monoksit ve karbon dioksitin kimyasal denge karışımının redoks reaksiyonudur. Karbon monoksitin karbondioksit ve grafite orantısız hale gelmesi veya bunun tersidir:
- 2CO
 CO2 + C
CO2 + C
 CO2 + C
CO2 + C












