
Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Trinitrotoluen (TNT) veya daha özel olarak 2,4,6-trinitrotoluen, C6H2(NO2)3CH3 formülüne sahip bir kimyasal bileşiktir. Bu sarı katı bazen kimyasal sentezde bir reaktif olarak kullanılsa da, daha çok uygun kullanım özelliklerine sahip bir patlayıcı madde olarak bilinmektedir. TNT'nin patlayıcı verimi, bombaların standart karşılaştırmalı kuralı ve patlayıcıların yıkıcılığı olarak kabul edilir. Kimyada, TNT yük transfer tuzları üretmek için kullanılır.

Azot ya da nitrojen, simgesi N olan bir element olup atom numarası 7'dir. Renksiz, kokusuz, tatsız ve inert bir gazdır. Azot, dünya atmosferinin yaklaşık %78'ini oluşturur ve tüm canlı dokularında bulunur. Azot ayrıca, amino asit, amonyak, nitrik asit ve siyanür gibi önemli bileşikler de oluşturur.

Alkol, karbon atomuna doğrudan bir -OH (hidroksil) grubunun bağlı olduğu organik bileşiklere verilen genel ad. Genel formülü CnH2n+1OH olan mono alkoller, alkollerin önemli bir sınıfıdır. Bunlardan etanol (C2H5OH), alkollü içeceklerde bulunan türüdür. Genellikle alkol kelimesi ile etanol kastedilir ki yeni fermente olmuş birada etanol oranı %3-5 arasında iken şarapta %12-15 arasındadır.

Üre (Latince Urea Pura), organik bir bileşik. Formülü H2N-CO-NH2'dir. Karbonik asidin diamidi olan üre aynı zamanda karbamik asidin de amidi olduğundan karbamid adı ile de bilinir.

Patlayıcı madde, hararet veya şok tesiri ile kimyasal değişikliğe uğrayan, yüksek derecede ısı, çok hacimde gaz meydana getiren, katı, sıvı veya gaz hâlindeki kimyasal maddelerdir.

Nitrogliserin nitrik asit esterinin oluşumuna uygun koşullar altında, en çok beyaz dumanlı nitrik asit ile gliserinin nitrolanmasıyla üretilen yoğun, renksiz, yağlı, patlayıcı sıvıdır. Kimyasal olarak, madde nitro bileşiğinden ziyade bir organik nitrat bileşiği olmasına rağmen, geleneksel adı genellikle daha fazla kullanılır. 1847'de icat edilen nitrogliserin, inşaat, yıkım ve madencilik endüstrilerinde kullanılan çoğunlukla dinamit gibi patlayıcı maddelerin üretiminde aktif bir bileşen olarak kullanılmaktadır. 1880'lerden beri, nitrogliserin ordu tarafından aktif bir bileşen ve kordit ve balistit gibi bazı katı itici yakıtlarda nitroselüloz için jelatinleştirici olarak kullanılmıştır.

Karabarut, kükürt, odun kömürü ve potasyum nitratın bir karışımıdır. Kükürt kullanılmadan yapılabilirse de, bu şekilde yapılan karabarut, kükürt kullanılarak yapılan kadar güçlü olmaz. Çok hızlı yanarak karbondioksit, su ve azottan ibaret sıcak bir gaz hacmi ve potasyum sülfürden oluşan katı bir artık bırakır. Yanma özelliklerinden dolayı ortaya çıkan sıcaklık ve gaz hacmi, barutun ateşli silahlarda itici yakıt ve havai fişeklerde piroteknik bileşim olarak kullanımına yol açmıştır. Modern ateşli silahlarda karabarut yerine dumansız barut kullanılır. Antika ateşli silahlarda çoğunlukla karabarut kullanılır.

RDX, gerçek adı siklotrimetilen-trinitramin olup saf RDX 204 °C'de eriyen ve 1.816 g/cm³ yoğunlukta olan bir patlayıcıdır. Bu patlayıcı için kullanılan RDX kısaltması, İngiliz menşeli olduğundan Royal Demolition Explosive kelimelerini ifade etmektedir. Patlayıcıların kısaltma halindeki isimleri genellikle kimyasal içeriklerinin kısaltması veya baş harfleri kullanılarak oluşturulmakla birlikte, II. Dünya Savaşı'nda patlayıcının kompozisyonunun Almanlar tarafından deşifre edilememesi için İngilizler tarafından bu şekilde kısaltılmıştır.

ANFO, madencilik ile inşaat sektöründe yaygın ve sıklıkla kullanılan, karışım halinde hazırlanan amonyum nitrat tabanlı bir patlayıcı türüdür.
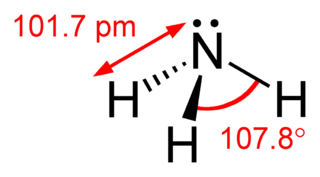
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir. OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.

Kimyada amid sözcüğü iki anlama sahiptir: - Birinci anlamıyla amid, bir azot atomuna (N) bağlı bir karbonil grubu bulunduran bir organik fonksiyonel grup veya bu gruba sahip bir bileşiktir. - İkinci anlamıyla amid, bir azot anyonudur.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Gümüş nitrat en önemli gümüş tuzudur. Renksiz ağır kristallerden oluşur. Tıpta dağlamak maksadıyla kullanılır ve antibakteriyel özelliği vardır. Bu özelliğinden dolayı siğil tedavisinde sıkça kullanılır. Ayrıca deriyi ve organik maddeleri karartmada tercih edilir. Deriyi kararttığından cehennem taşı ismini almıştır. Suda ve alkolde kolayca çözündüğünden birçok gümüş bileşiklerinin elde edilmesinde ilkel madde olarak kullanılır. En çok kullanıldığı yerler, başta fotoğrafçılık olmak üzere mürekkepler, saç boyası yapımı ve gümüş kaplamacılığıdır.bileşenleri gümüş ve nitrik asittir. Sentezi ise örnekteki formüle göre yapılır:
- Ag + 2 HNO3 → AgNO3 + NO2 + H2O
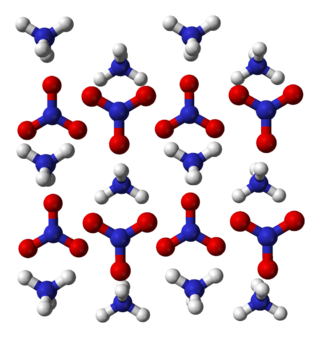
Amonyum nitrat, amonyum ve nitrat iyonlarından oluşan, NH4NO3 formülüne sahip yüksek patlayıcı bir kimyasal bileşiktir. Higroskopik özellikte ve beyaz kristal bir katı olarak hidrat oluşturmasa da suda çok çözünür. Ağırlıklı olarak, tarımda yüksek azotlu gübre olarak kullanılmaktadır. 2017 yılında küresel üretimi 21.6 milyon ton olarak tahmin edildi.
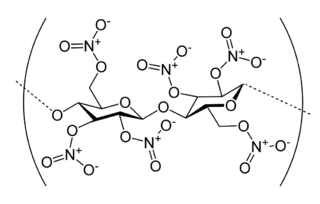
Nitroselüloz selülozun nitrik asite veya nitrik asit ve başka bir asit (genellikle hidroklorik asit veya sülfürik asit karışımına veyahut başka güçlü bir nitrolama maddesine maruz bırakılıp, nitrolanmayla oluşan oldukça yanıcı bir bileşiktir. İlk önemli kullanım alanlarından biri, ateşli silahlarda itici yakıt olarak barutun yerini alan pamuk barutu olarak kullanılmasıdır. Ayrıca madencilik ve diğer uygulamalarda barutun yerini alarak düşük güçte patlayıcı madde olarak kullanıldı.
Nitrolama bir nitro grubunun organik kimyasal bileşik içine sokulması için genel bir kimyasal proses sınıfıdır. İfade daha genel olarak, ayrıca nitrogliserin sentezinde olduğu gibi alkoller ve nitrik asit arasında farklı nitrat esterleri oluşturma işlemine yanlış olarak uygulanır. Nitro bileşiklerinin ve nitratların ortaya çıkan yapısı arasındaki fark nitro bileşiklerindeki azot atomunun doğrudan oksijen olmayan bir atoma genel olarak da karbon veya başka azot atomuna bağlanmasıdır. Oysaki organik nitratlar olarak da adlandırılan nitrat esterlerinde, azot bir oksijen atomuna genellikle dolayısıyla da bir karbon atomu 'na bağlanır.

Magnezyum nitrat Mg(NO3)2(H2O)x formülüne sahip inorganik bileşikleri ifade eder. Formüldeki, x = 6, 2 ve 0 olabilir. Hepsi beyaz renkli katılardır. Susuz madde higroskopiktir, havada bekletildiğinde hızlı bir şekilde hekzahidrat oluşturur. Bütün tuzları hem suda hem de etanolde çok çözünür.
Nitrometan, bazen basitçe "nitro" olarak adlandırılan ve kimyasal formülü CH3NO2 olan bir organik bileşiktir. En basit organik nitro bileşiğidir. Ekstraksiyonlar, reaksiyon ortamı ve temizleme solventi gibi çeşitli endüstriyel uygulamalarda çözücü olarak yaygın bir şekilde kullanılan polar bir sıvıdır. Organik sentezde bir ara ürün olarak pestisit, patlayıcı, lif ve kaplama üretiminde yaygın olarak kullanılır. Nitrometan çeşitli Tap Fuel kalkış yarışı gibi motor sporlarında ve Radyo-kontrollü uçaklarda, tel kumanda kontrollü ve serbest uçuş model uçaklardaki minyatür içten yanmalı motorlarda yakıt katkı maddesi olarak kullanılır.

Uranil nitrat, UO2(NO3)2.n H2O formülüne sahip, suda çözünür sarı renkli bir uranyum tuzudur. Hekza-, tri- ve dihidratlar bilinmektedir. Bileşik esas olarak nükleer yakıtların hazırlanmasında bir ara madde olarak kullanılma potansiyeliyle ilgi çekmiştir.
















