Nitrogliserin
 | |
 | |
 | |
| Adlandırmalar | |
|---|---|
Tercih edilen IUPAC adı Propan-1,2,3-tril trinitrat | |
Diğer adlar 1,2,3-Tris(nitrooksi)propan | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| 1802063 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.219 |
| EC Numarası |
|
| 165859 | |
IUPHAR/BPS | |
| KEGG | |
| MeSH | Nitrogliserin |
PubChem CID | |
| UNII | |
| UN numarası | 0143, 0144, 1204, 3064, 3319 |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
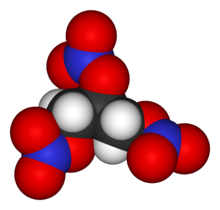
| Kimyasal formül | C3H5N3O9 |
| Molekül kütlesi | 227,09 g mol−1 |
| Görünüm | Renksiz sıvı |
| Yoğunluk | 1,6 g⋅cm3 (15 °C’de) |
| Erime noktası | 14 °C (57 °F; 287 K) |
| Kaynama noktası | 50 °C (122 °F; 323 K) Patlar |
| Çözünürlük (su içinde) | Çok az[1] |
| Çözünürlük | Aseton, eter, benzen, alkol[1] |
| log P | 2,154 |
| Yapı | |
| |
| |
| Termokimya | |
Standart formasyon entalpisi (ΔfH⦵298) | −370 kJ⋅mol−1 |
Standart yanma entalpisi (ΔcH⦵298) | −1,529 MJ⋅mol−1 |
| Farmakoloji | |
| C01DA02 (DSÖ) C05AE01 (DSÖ) | |
| Damardan, ağızdan, dil altından, topikal | |
| Farmakokinetik: | |
| <1% | |
| Karaciğer | |
| 3 dakika | |
| Hukuki durum |
|
| Patlayıcı verileri | |
| Şok duyarlılığı | Yüksek |
| Sürtünme duyarlılığı | Yüksek |
| Patlama hızı | 7700 m⋅s1 |
| REFaktörü | 1,50 |
| Tehlikeler | |
| İş sağlığı ve güvenliği (OHS/OSH): | |
| Ana tehlikeler | Patlayıcı, zehirli |
| GHS etiketleme sistemi: | |
| Piktogramlar |     |
| İşaret sözcüğü | Tehlike |
| Tehlike ifadeleri | H202, H205, H241, H301, H311, H331, H370 |
| Önlem ifadeleri | P210, P243, P250, P260, P264, P270, P271, P280, P302+P352, P410 |
| NFPA 704 (yangın karosu) | |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | C 0,2 ppm (2 mg/m3) [deri][2] |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
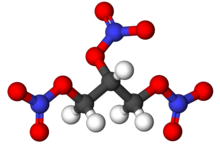
Nitrogliserin (NG, trinitrogliserin, TNG, nitro, gliseril trinitrat, 1,2,3-trinitroksipropan) nitrik asit esterinin oluşumuna uygun koşullar altında, en çok beyaz dumanlı nitrik asit ile gliserinin nitrolanmasıyla üretilen yoğun, renksiz, yağlı, patlayıcı sıvıdır. Kimyasal olarak, madde nitro bileşiğinden ziyade bir organik nitrat bileşiği olmasına rağmen, geleneksel adı genellikle daha fazla kullanılır. 1847'de icat edilen nitrogliserin, inşaat, yıkım ve madencilik endüstrilerinde kullanılan çoğunlukla dinamit gibi patlayıcı maddelerin üretiminde aktif bir bileşen olarak kullanılmaktadır. 1880'lerden beri, nitrogliserin ordu tarafından aktif bir bileşen ve kordit ve balistit gibi bazı katı itici yakıtlarda nitroselüloz için jelatinleştirici olarak kullanılmıştır.
Nitrogliserin fişek dolduranlar tarafından kullanılan çift bazlı dumansız barutların önemli bir bileşenidir. Nitroselülozlu yüzlerce barut bileşimi tüfek, tabanca ve av tüfeği fişeği dolduranlar tarafından kullanılır.
130 yılı aşkın süredir tıpta, anjina pektoris ve kronik kalp yetmezliği gibi kalp koşullarını tedavi etmek için, nitrogliserin güçlü bir vazodilatör (vasküler sistemin genişlemesi) olarak kullanılmıştır. Bu yararlı etkilerin daha önce nitrogliserinin, güçlü bir vazodilatör olan nitrik oksite dönüştürülmesinden kaynaklandığı bilinmesine rağmen, bu dönüşümü gerçekleştiren enzimin mitokondriyal aldehit dehidrojenaz (ALDH2) olduğu 2002 yılına kadar keşfedilememiştir.[3] Nitrogliserin dilaltı tabletler, spreyler, kremler ve yakılar hâlinde bulunabilir.[4]
Tarihçe
Nitrogliserin, karabaruttan daha güçlü üretilmiş ilk kullanışlı patlayıcıydı. İlk olarak 1847'de Torino Üniversitesi’nde Théophile-Jules Pelouze altında çalışan İtalyan kimyager Ascanio Sobrero tarafından sentezlendi.[5] Sobrero başlangıçta buluşuna pirogliserin adını verdi ve nitrogliserinin patlayıcı madde olarak kullanılmasına şiddetle karşı çıktı.[6]
Nitrogliserin, 1864 yılında Heleneborg, İsveç’te bulunan Nobel’in silah fabrikasındaki bir patlamada küçük kardeşi Emil Oskar Nobel ve birkaç fabrika işçisi öldükten sonra tehlikeli bileşikle çalışmanın daha güvenli yollarını deneyen Alfred Nobel tarafından ticari olarak yararlı bir patlayıcı olarak kabul edildi.[7]
Bir yıl sonra, Almanya’da Dynamit Nobel AG şirketini kuran Nobel Hamburg yakınlarındaki Geesthacht’da bulunan Krümmel tepelerinde izole bir fabrika inşa etti. Bu işletme "Patlatma Yağı" adı verilen nitrogliserin ve barutun sıvı karışımını ihraç etti. Ancak bu karışım, birçok felakete yol açtığı gibi son derece kararsız ve kullanımı zordu. Krümmel fabrikasının binaları iki kez yıkıldı.[8]
Nisan 1866'da, Sierra Nevada Dağları’ndan geçen 506 m. uzunluğundaki Zirve Tünelinin yapımını hızlandırmak için nitrogliserini bir patlayıcı olarak denemeyi planlayan Orta Pasifik Demiryolları için üç kasa nitrogliserin Kaliforniya’ya gönderildi . Sandıklardan biri patladı, San Francisco’daki Wells Fargo şirket ofisini yıktı ve 15 kişiyi öldürdü. Bu, Kaliforniya'da sıvı nitrogliserin taşınmasında tam bir yasağa yol açtı. Kuzey Amerika’daki İlk Kıtalararası Demiryolu tamamlanması için gereken sert kaya delme ve patlatma işleminde kullanılacak nitrogliserinin yerinde üretimi gerekli idi.[9]
Haziran 1869’da, o zamanlar yerel olarak Powder-Oil olarak bilinen ve her birinde birer ton olmak üzere, iki vagon nitrogliserin Kuzey Galler North Walles bölgesindeki Cwm-Y-Glo köy yolunda patladı. Patlama altı can kaybına, çok sayıda yaralanmaya ve köyde büyük hasara yol açtı. İki attan çok az iz bulundu. Birleşik Krallık Hükümeti, şehir bölgesinde meydana gelen hasar ve ne olabileceği konusunda çok endişe duydu (bu iki ton Liverpool yoluyla Almanya'dan gelen daha büyük bir yükün parçasıydı) ve kısa süre içerisinde 1869 Nitro-Gliserin Yasasını geçirdi.[10] Sıvı nitrogliserin başka yerlerde de yaygın olarak yasaklandı ve bu yasal kısıtlamalar 1867'de Alfred Nobel ve şirketinin dinamiti geliştirmesine sebep oldu. Bu, Krümmel tepelerinde bulunan diatomit (Almanca "Kizelgur") ile nitrogliserinin karıştırılmasıyla yapıldı. "Dualin" (1867), "lithofraktör" (1869) ve "jelatin dinamit" (1875) gibi benzer karışımlar, nitrogliserinin diğer inert emici veya soğurucu maddelerle karıştırılmasıyla oluşturuldu ve birçok bileşimler Nobel'in dinamit için sıkıca tutulan patentlerinden kurtulmak için yapılan girişimler sonucu olarak diğer şirketler tarafından denendi.
Karışımın vizkozitesini artıran nitroselüloz içerekli dinamit karışımları, genellikle "jelatinler" olarak bilinir.
Amil nitritin göğüs ağrısını hafifletmeye yardımcı olduğunu keşfinden sonra, doktor William Murrell anjina pektorisi hafifletmek ve kan basıncını azaltmak için nitrogliserin kullanımını denedi. 1878 yılında Murrel hastalarını seyreltilmiş küçük dozlarda nitrogliserin ile tedavi etmeye başladı ve sonuçlarını 1879'da The Lancet dergisinde yayınladıktan sonra bu tedavi kısa sürede yaygın olarak kullanıldı.[11][12] 1896'da ölümünden birkaç ay önce, Alfred Nobel kalp rahatsızlığı için nitrogliserin reçete edildiğinde bir arkadaşına şöyle yazmıştır: "Dahilen kullanmam için nitrogliserin reçete edildiğim kaderin cilvesi değil mi! Kimyager ve halkı korkutmamak için buna Trinitrin diyorlar."[13] Sağlık kurumları aynı sebepten dolayı "gliseril trinitrat" adını da kullandı.
Savaş zamanı üretim oranları
I. Dünya Savaşı ve II. Dünya Savaşı sırasında askeri itici yakıtlar olarak ve istihkâm işlerinde kullanılmak üzere büyük miktarlarda nitrogliserin üretildi. I. Dünya Savaşı sırasında, İngiltere'deki en büyük itici yakıt fabrikası olan HM Factory, Gretna, haftada yaklaşık 800 ton kordit RDB üretti. Bu miktar haftada en az 336 ton nitrogliserin (üretimde kayıp olmadığı varsayılarak) gerektiriyordu. Kraliyet Donanmasının, Holton Heath Dorset, İngiltere'de Royal Navy Cordite Factory adlı kendi fabrikası vardı. I. Dünya Savaşı sırasında Kanada'da büyük bir kordit fabrikası kuruldu. Nobel, Ontario’daki Canadian Explosives Limited kordit fabrikası ayda 680 ton kordit üretmek için tasarlanmıştır ve ayda yaklaşık 286 ton nitrogliserin gerektirir.
Kararsızlık ve duyarsızlaştırma
Saf hâliyle nitrogliserin kontakt patlayıcı maddedir. Fiziksel şok nitrogliserinin patlamasına neden olur ve zamanla daha kararsız formlara ayrışır. Bu nitrogliserinin taşınması veya kullanılmasını oldukça tehlikeli hâle getirir. Seyreltilmemiş formunda, daha yeni geliştirilen RDX ve PETN ile karşılaştırıldığında dünyanın en güçlü patlayıcılarından biridir.
Tarihinin başlarında sıvı nitrogliserinin yaklaşık 5-10 °C'ye soğutulmasıyla "duyarsızlaştırıldığı" bulunmuştur. Bu sıcaklıkta, nitrogliserin büzülüp, donar ve sonuçta katılaşır. Çözülmesi, özellikle safsızlıklar varsa veya ısınma çok hızlıysa, son derece hassaslaştırıcı olabilir.[14] Kimyasal olarak "duyarsızlaştırılan" nitrogliserin, kabaca %10–30 etanol, aseton,[15] veya dinitrotoluen gibi maddelerin ilavesiyle, modern yüksek patlayıcı maddeler kadar "güvenli" olarak değerlendirilebilecek bir noktaya kadar mümkündür. (Yüzde oranları kullanılan duyarsızlaştırıcı maddeye göre değişir.) Duyarsızlaştırma "saf" ürünü yeniden oluşturmak için ekstra çaba gerektirir. Aksi hâlde, duyarsızlaştırılmış nitrogliserinin patlamasının çok daha zor olduğu varsayılmalıdır. Bu da duyarsızlaştırılan nitrogliserini muhtemelen pratik uygulama için bir patlayıcı olarak işe yaramaz hâle getirir.
Nitrogliserin kullanımında ciddi sorun, onun 13 °C'lik yüksek donma noktasından kaynaklanır. Katı nitrogliserin sıvıya göre şoka çok daha az duyarlıdır, patlayıcılarda ortak bir özellik. Geçmişte, nitrogliserin genellikle donmuş hâlde sevk edilirdi. Ancak, kullanılmadan hemen önce çözülme işlemi sırasında çok sayıda kazaya neden olmuştur. Bu dezavantaj, nitrogliserinin diğer polinitratlarla olan karışımları kullanılarak aşılır. Örneğin, nitrogliserin ve etilen glikol dinitrat karışımı -29 °C'de donar.[16]
Patlama
Nitrogliserin ve seyrelticileri kesinlikle tutuşabilir (yanabilir). Nitrogliserinin patlayıcı gücü patlamadan kaynaklanır: ilk bozunmadan kaynaklanan enerji etrafındaki yakıtı patlatan güçlü bir basınç dalgası oluşturur. Bu basınç dalgası patlayıcı ortamda ses hızının 30 katına yakın hızda yayılan ve ayrışan yakıtın beyaz sıcak bir gaza dönüştüğü ani basınç kaynaklı kendi kendine devam eden bir şok dalgasıdır. Nitrogliserin patlaması normal oda sıcaklığı ve basıncında ilk hacminin 1,200 kat fazlasını kaplayan gazlar üretir. Serbest kalan ısı sıcaklığı yaklaşık 5000 °C'ye yükseltir.[16] Bu, basınç veya şok ne olursa olsun sadece mevcut yakıta bağlı olan tutuşma işleminden tamamen farklıdır. Bozunma diğer patlayıcılara kıyasla salınan enerjinin gaz mollerine oranının çok daha yüksek olması ile sonuçlanır ve bu da onu en sıcak olarak patlayan yüksek patlayıcı maddelerden biri yapar.
Üretimi
Nitrogliserin, gliserinin katalizör katılmış asitle nitratlaştırılması sonucu üretilebilir.
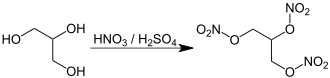
Endüstriyel üretim işlemi genellikle yaklaşık 1:1 oranındaki derişik sülfürik asit ve derişik nitrik asit karışımının gliserin ile reaksiyonu ile olur. Nitrogliserin beyaz dumanlı nitrik asit (azot oksitler içeren kırmızı dumanlı nitrik asitin aksine, azot oksitlerin uzaklaştırıldığı oldukça pahalı saf bir nitrik asit) ve derişik sülfürik asitin karıştırılmasıyla üretilebilir. Çoğunlukla, bu karışıma oleum olarak da bilinen dumanlı sülfürik asit (aşırı kükürt trioksit içeren sülfürik asit) ve azeotropik nitrik asit (yaklaşık %70 nitrik asit geri kalanı sudan oluşur) karıştırılarak daha ucuz yöntem ile ulaşılır.
Sülfürik asit, gliserinin nükleofilik oksijen atomlarına saldıran protonlu nitrik asit türlerini üretir. Nitro grubu böylece C−O−NO2 bir ester olarak eklenir ve su üretilir. Bu reaksiyon nitronyum iyonlarının elektrofil olduğu elektrofilik aromatik sübstitüsyon reaksiyonundan farklıdır.
Gliserin ilavesi, asit karışımı nitratlamalarında her zaman olduğu gibi bir ekzotermik reaksiyonla (yani, ısı üretilir) sonuçlanır. Karışım çok ısınırsa, denetimsiz bir reaksiyonla sonuçlanır. Organik maddelerin sıcak nitrik asit tarafından bozunumlu oksidasyonu ve patlama riski yüksek olan zehirli azot dioksit gazı salınımı ile beraber hızlandırılmış nitrolama durumu ortaya çıkar. Bu nedenle, gliserin karışımı karışık asidi içeren reaksiyon kabına yavaşça eklenir (gliserine asit değil). Nitratör soğuk su veya başka bir soğutucu karışımı ile soğutulur ve gliserin ilavesi boyunca yaklaşık 22 °C'de tutulur, bunun altında esterleştirme çok yavaş gerçekleşir. Çoğu kez demir veya kurşundan yapılan ve genellikle basınçlı hava ile karıştırılan nitratör kabının tabanında, bir patlamayı önlemek için bütün reaksiyon karışımının (şarj olarak adlandırılır) içine dökülebileceği (bu işleme boğulma denir) ve büyük bir su havuzunun üzerinde asılı olan bir acil durum tuzağı kapısı vardır. Şarjın sıcaklığı yaklaşık 30 °C'yi (ülkeye göre değişen gerçek değer) aşarsa veya nitratörün havalandırma bacasında kahverengi dumanlar görülürse hemen reaksiyon karışımı boğulur.
Patlayıcı madde ve itici yakıt olarak kullanımı
Nitrogliserinin ana kullanımı dinamit gibi patlayıcı maddeler ve itici yakıtlardır.
Nitrogliserin, ısı, şok veya aleve maruz kaldığında patlayabilen yağlı bir sıvıdır.
Alfred Nobel özellikle "Kizelgur" veya diatomit gibi inert soğurucularla nitrogliserin karıştırılarak patlayıcı madde olarak, nitrogliserin kullanımını geliştirdi. Bu patlayıcı maddeyi dinamit olarak adlandırdı ve 1867 yılında patentini aldı.[20] Dinamit, teker teker yağlı su geçirmez kağıt içerisine sarılmış çubuk şeklinde kullanıma hazır olarak tedarik edildi. Dinamit ve benzeri patlayıcılar karayolu ve demiryolu tünellerinin delinmesi, madencilik, tarım arazilerindeki köklerin temizlenmesi, taş ocakçılığı ve yıkım işlerinde olduğu gibi inşaat mühendisliği işlerinde yaygın olarak kullanılmıştır. Aynı şekilde, istihkâmcılarda inşaat ve yıkım işleri için dinamit kullanmışlardır.
Nitrogliserin ateşli silahlarda kullanılan askeri itici yakıtlarda bir bileşen olarak ayrıca kullanılmıştır.
Nitrogliserin şist oluşumlarından, petrol ve doğal gazı geri kazanmak için kullanılan hidrolik kırma işlemi ile birlikte kullanılmıştır. Teknik, doğal veya hidrolik kaynaklı kırık sistemlerinde nitrogliserinin yer değiştirmesini ve patlatılmasını ya da hidrolik kaynaklı kırıklarda nitrogliserinin yer değiştirmesi ve patlatılmasının ardından peletlenmiş TNT kullanılarak kuyu delinmesini içerir.[21]
Nitrogliserin patlama sırasında neredeyse hiç görünür duman üretmediği için diğer bazı yüksek patlayıcılara göre bir avantaja sahiptir. Bu nedenle, dumansız barutun çeşitli formülasyonunda bir bileşen olarak yararlıdır.[22]

Nitrogliserinin duyarlılığı askeri bir patlayıcı olarak kullanışlılığını sınırladı. TNT, RDX ve HMX gibi daha az duyarlı patlayıcılar mühimmatlarda onun yerini büyük ölçüde aldı. İstihkamda önemini sürdürmekte ve muharebe istihkamcılar hala dinamiti kullanmaktadırlar.
Alfred Nobel daha sonra nitrogliserin ve pamuk barutunu birleştirerek balistiti geliştirdi. 1887 yılında patentini aldı. Balistit birkaç Avrupa devleti tarafından askeri bir itici yakıt olarak kabul edildi. Bunu ilk kabul eden İtalya oldu. Buna karşılık, İngiliz devleti ve İngiliz Milletler Topluluğu devletleri 1889 yılında Birleşik Krallık'tan Sir Frederick Abel ve Sir James Dewar tarafından geliştirilen korditi kabul ettiler. Orijinal Cordite Mk I consisted of %58 nitrogliserin, %37 pamuk barutu ve %5 vazelinden oluşuyordu. Balistit ve korditin her ikisi de "filament-kort" formunda üretilmiştir.
Dumansız barutlar başlangıçta tek patlayıcı bileşen olarak nitroselüloz kullanılarak geliştirilmiştir. Bu nedenle, bunlar tek bazlı itici yakıtlar olarak biliniyorlardı. Nitroselüloz ve nitrogliserini birlikte içeren ve çift bazlı itici yakıtlar olarak da bilinen dumansız barut çeşitleri de geliştirilmiştir. Dumansız barutlar başlangıçta sadece askeri kullanım için tedarik edildi. Ancak, kısa süre sonra sivil kullanım için geliştirildi ve spor için hızla kabul edildi. Bazıları av barutları olarak bilinir. Nitroselüloz, nitrogliserin ve nitroguanidin içeren üç bazlı itici yakıtlar, ağırlıklı olarak tank topları ve donanma toplarında kullanılanlar gibi son derece yüksek kalibreli top mühimmatları için ayrılmıştır. Jelatin dinamit olarak da bilinen patlayıcı jelatin, 1875 yılında nitrogliserin, kağıt hamuru ve sodyum veya potasyum nitrat kullanılarak Nobel tarafından icat edildi. Bu ilk olarak düşük maliyetli, esnek bir patlayıcıydı.
Tıbbi kullanımı
Nitrogliserin, isosorbid dinitrat (Isordil) ve isosorbid mononitrat (Imdur, Ismo, Monoket) gibi diğer birçok nitratlar içeren ve nitratlar adı verilen bir ilaç grubuna aittir.[23] Bu maddelerin hepsi mitokondriyal aldehit dehidrogenaz (ALDH2) tarafından vücutta etkili bir doğal vazodilatör olan nitrik oksite dönüştürülerek etki gösterirler.[3]
Tıpta, nitrogliserin etkili bir antihipertansif ajan olarak ve kalbe kan ve oksijenin yetersiz akmasından kaynaklanan iskemik kalp hastalığının ağrılı bir belirtisi olan anjina pektoris için kullanılır. Nitrogliserin oksijen akışı ve kalbe giden kan arasındaki dengesizliği düzeltir.[23] Düşük dozlarda, nitrogliserin damarları, atardamarlardan daha fazla genişletir. Böylece, ön yükü (dolumdan sonra kalpteki kan hacmi) azaltır; bunun birincil etki mekanizması olduğu düşünülmektedir. Ön yükün azaltılmasıyla, kalbin pompalaması için daha az kan vardır. Bu da kalbin çok çalışmak zorunda kalmaması nedeni ile oksijen ihtiyacını azaltır. Ek olarak, daha düşük bir ön yüke sahip olmak, ventriküler transmural basıncı (kalbin duvarlarına uygulanan basınç) azaltır, bu da kalpten daha fazla kan akmasını sağlamak için kalp atardamarlarının sıkışmasını azaltır. Daha yüksek dozlarda, atardamarları genişletir, böylece son yükü azaltır (kalbin pompalaması gereken basıncı azaltır).[23] İyileştirilmiş miyokardiyal oksijen talebine karşı, oksijen iletim oranı anjina pektoris atakları sırasında aşağıdaki tedavi edici etkilere yol açar: göğüs ağrısının azalması, kan basıncının düşmesi, kalp atış hızında artış ve ortostatik hipotansiyon. Belirli fiziksel aktiviteler yaparken anjina yaşayan hastalar, aktiviteden 5-10 dakika önce nitrogliserin alarak semptomları önleyebilirler. Doz aşımı methemoglobinemi oluşturabilir.[24][25]
Nitrogliserin tabletler, merhem, intravenöz kullanım için çözelti, transdermal yakılar veya dil altı olarak uygulanan spreyler halinde bulunur. Bazı nitrogliserin formları vücutta diğerlerinden daha uzun sürer. Nitratlara sürekli maruz kalmanın vücudun bu ilaca normal olarak yanıt vermemesine neden olduğu gösterilmiştir.Uzmanlar, vücudun nitratlara yanıt vermesini sağlamak için vücudun yenileşmesi amacıyla birkaç saat izin verilerek, yakıların gece çıkarılmasını öneriyor. Daha kısa etkili nitrogliserin preparatları, tolerans geliştirme riski daha az olanlarla birlikte günde birkaç kez kullanılabilir.[26] Nitrogliserin ilk kez William Murrell tarafından 1878 yılında, anjina krizlerini tedavi etmek için kullanıldı ve keşif aynı yıl yayınlandı.[12][27]
Endüstriyel maruziyet
Yüksek dozlarda nitrogliserine maruz kalmak, nadiren "NG başı" veya "patlama başı" olarak bilinen şiddetli baş ağrılarına neden olabilir. Bu baş ağrıları bazı insanları iş yapamaz hale getirecek kadar şiddetli olabilir; bununla birlikte, insanlar uzun süreli maruziyetten sonra nitrogliserine tolerans ve bağımlılık geliştirirler. Nadiren de olsa, yoksunluğu ölümcül olabilir.[28] Yoksunluk belirtileri göğüs ağrısı ve diğer kalp problemlerini içerir. Bu belirtiler nitrogliserin veya diğer uygun organik nitratlara tekrar maruz bırakılmak suretiyle hafifletilebilir.[29]
Nitrogliserin (NTG) üretim tesislerindeki işçiler için, yoksunluğun etkileri bazen işyerinde düzenli olarak nitrogliserin maruziyeti yaşayanlarda "Pazar kalp krizi" ni içermekte ve damar genişleme etkisi toleransının gelişmesine yol açmaktadır. Hafta sonu boyunca, işçiler toleransı kaybederler ve Pazartesi günü tekrar maruz kaldıklarında, yüksek kalp hızı, baş dönmesi ve baş ağrılı etkili bir vazodilatasyon oluşur. Bu duruma "Pazartesi hastalığı" adı verilir.[30][31]
İnsanlar işyerinde nefes alarak, cilt emilimiyle, yutarak veya göz teması ile nitrogliserine maruz kalabilirler.Amerika İş Sağlığı ve Güvenliği İdaresi, işyerinde nitrogliserin maruziyetine ilişkin 8 saatlik iş günü boyunca cilt maruziyeti için, yasal sınırı (izin verilen maruziyet limiti) 0.2 ppm (2 mg/m3) olarak belirlemiştir. Amerika Ulusal Mesleki Sağlık ve Güvenlik Enstitüsü 8 saatlik bir iş günü boyunca cilt maruziyeti için, tavsiye edilen maruziyet limiti 0.1 mg/m3 olarak belirlemiştir. 75 mg/m3 seviyelerindeki nitrogliserin, hayata ya da sağlığa ivedi tehdittir.[32]
Ayrıca bakınız
- Eritritol tetranitrat
- Etilen glikol dinitrat
- Mannitol hekzanitrat
- Metil nitrat
- Tetranitratoksikarbon
- Ksilitol pentanitrat
- RE faktörü
Etimoloji
Fransızca nitroglycérine "bir tür patlayıcı madde" sözcüğünden alıntıdır. Fransızca sözcük İngilizce aynı anlama gelen nitroglycerin sözcüğünden alıntıdır. (İlk kullanımı: 1857 İng.) Daha fazla bilgi için nitro+, gliserin maddelerine bakınız. Tarihte en eski kaynak: [ Tıngır & Sinapian, Istılahat Lugati (1892) ][33]
Yararlanılan kaynaklar
- ^ a b "Archived copy". 16 Mayıs 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 October 2016.
- ^ NIOSH Pocket Guide to Chemical Hazards. "#0456". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b Chen, Z.; Foster, M. W.; Zhang, J.; Mao, L.; Rockman, H. A.; Kawamoto, T.; Kitagawa, K.; Nakayama, K. I.; Hess, D. T.; Stamler, J. S. (2005). "An essential role for mitochondrial aldehyde dehydrogenase in nitroglycerin bioactivation". Proceedings of the National Academy of Sciences. 102 (34). ss. 12159-12164. Bibcode:2005PNAS..10212159C. doi:10.1073/pnas.0503723102. PMC 1189320 $2. PMID 16103363.
- ^ "Archived copy". 10 Mayıs 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 April 2018.
- ^ Sobrero, Ascagne (1847). "Sur plusieur composés détonants produits avec l'acide nitrique et le sucre, la dextrine, la lactine, la mannite et la glycérine" [Nitrik asit, şeker, dekstrin, laktoz, mannitol ve gliserin ile üretilen çeşitli patlayıcı bileşikler hakkında]. Comptes Rendus. Cilt 24. ss. 247-248. 19 Mart 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mayıs 2020.
- ^ Sobrero, Ascanio (1849). "Sopra alcuni nuovi composti fulminanti ottenuti col mezzo dell'azione dell'acido nitrico sulle sostante organiche vegetali" [Nitrik asitin bazı bitkisel organik maddeler üzerine etkisiyle elde edilen bazı yeni patlayıcı ürünler hakkında]. Memorie della Reale Accademia delle Scienze di Torino (2nd Series). Cilt 10. ss. 195-201. 10 Mayıs 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mayıs 2020. On p. 197, Sobrero nitrogliserini "pirogliserin" olarak adlandırıyor:
- "Quelle gocciole costituiscono il corpo nuovo di cui descriverò ora le proprietà, e che chiamerò Piroglicerina." ("Pirogliserin" adını vereceğim ve özelliklerini şimdi açıklayacağım bu damlalar yeni bir maddeyi oluşturuyor.)
- ^ "Emil Nobel". NobelPrize.org. 15 January 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 October 2008.
- ^ "Krümmel". NobelPrize.org. 10 Temmuz 2006 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mayıs 2020..
- ^ "Transcontinental Railroad – People & Events: Nitroglycerin". American Experience. PBS. 12 Şubat 2003 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Mayıs 2020.
- ^ North Wales Daily Post newspaper of October 14th 2018.
- ^ Murrell, William (1879). "Nitroglycerin as a remedy for angina pectoris". The Lancet. Cilt 1. ss. 80-81, 113-115, 151-152, 225-227. 3 Ocak 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Mayıs 2020.
- ^ a b Sneader, Walter (2005). Drug Discovery: A History. John Wiley and Sons. ISBN 978-0-471-89980-8.
- ^ "History of TNG". beyonddiscovery.org. 1 Kasım 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Nisan 2018.
- ^ "Tales of Destruction – Thawing can be Hell". 22 Şubat 2001 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 Mayıs 2020.
- ^ "Tales of Destruction – Is Nitroglycerin in This?". 22 Şubat 2001 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 Mayıs 2020.
- ^ a b "Nitroglycerin". Encyclopaedia Britannica. 12 Eylül 2002 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Mart 2005.
- ^ "Zusammensetzung der Zuckerasche" [Composition of sugar ash]. Annalen der Chemie und Pharmacie. 64 (3). 1848. ss. 398-399. doi:10.1002/jlac.18480640364.
- ^ "Ueber Nitroglycerin". Annalen der Chemie und Pharmacie. 92 (3). 1854. ss. 305-306. doi:10.1002/jlac.18540920309.
- ^ Di Carlo, F. J. (1975). "Nitroglycerin Revisited: Chemistry, Biochemistry, Interactions". Drug Metabolism Reviews. 4 (1). ss. 1-38. doi:10.3109/03602537508993747. PMID 812687.
- ^ Bellis, Mary. "Alfred Nobel and the History of Dynamite". About.com Money. 28 Ağustos 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Mayıs 2020.
- ^ Miller, J. S.; Johansen, R. T. (1976). "Fracturing Oil Shale with Explosives for In Situ Recovery" (PDF). Shale Oil, Tar Sand and Related Fuel Sources. s. 151. 2 Ekim 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 27 Mart 2015.
- ^ "Nitroglycerin". 5 Ocak 2003 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Mayıs 2020.
- ^ a b c Ogbru, Omudhome. "nitroglycerin, Nitro-Bid: Drug Facts, Side Effects and Dosing". MedicineNet. 27 Mart 2003 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Mayıs 2020.
- ^ Kaplan, K. J.; Taber, M.; Teagarden, J. R.; Parker, M.; Davison, R. (1985). "Association of methemoglobinemia and intravenous nitroglycerin administration". American Journal of Cardiology. 55 (1). ss. 181-183. doi:10.1016/0002-9149(85)90324-8. PMID 3917597.
- ^ "IntraMed – Bienvenido". www.intramed.net. 25 Ağustos 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Nisan 2018.
- ^ "Nitroglycerin for angina, February 1997, Vol. 7". 10 Mayıs 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 Kasım 2009.
- ^ Smith, E.; Hart, F. D. (1971). "William Murrell, physician and practical therapist". British Medical Journal. 3 (5775). ss. 632-633. doi:10.1136/bmj.3.5775.632. PMC 1798737 $2. PMID 4998847.
- ^ Amdur, Mary O.; Doull, John (1991). Casarett and Doull's Toxicology (4.4yayıncı=Elsevier bas.). ISBN 978-0071052399.
- ^ Sullivan, John B., Jr.; Krieger, Gary R. (2001). Clinical Environmental Health and Toxic Exposures: Latex. Lippincott Williams & Wilkins. s. 264. ISBN 978-0-683-08027-8. 29 Mayıs 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Nisan 2013.
- ^ Marsh, N.; Marsh, A. (2000). "A short history of nitroglycerine and nitric oxide in pharmacology and physiology". Clinical and Experimental Pharmacology and Physiology. 27 (4). ss. 313-319. doi:10.1046/j.1440-1681.2000.03240.x. PMID 10779131.
- ^ Assembly of Life Sciences (U.S.) Advisory Center on Toxicology. Toxicological Reports. National Academies. s. 115. NAP:11288. 24 Haziran 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Nisan 2013.
- ^ "Nitroglycerine". NIOSH Pocket Guide to Chemical Hazards. CDC. 8 Ekim 1999 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Kasım 2015.
- ^ "Nitrogliserin". etimolojiturkce.com. 24 Kasım 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Kasım 2023.
Dış bağlantılar
- "Nitroglycerine! Terrible Explosion and Loss of Lives in San Francisco". Orta Pasifik Demiryolu Fotoğraf Tarihi Müzesi. 9 Nisan 2001 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2020. – 1866 Gazete makalesi
- WebBook page for C3H5N3O91 Ağustos 2018 tarihinde Wayback Machine sitesinde arşivlendi.
- CDC - NIOSH Pocket Guide to Chemical Hazards8 Ekim 1999 tarihinde Wayback Machine sitesinde arşivlendi.
- The Tallini Tales of Destruction19 Temmuz 2012 tarihinde Wayback Machine sitesinde arşivlendi. Petrol kuyularını yeniden başlatmak için nitrogliserin dolu torpidoların tarihsel kullanımının ayrıntılı ve korkunç hikâyeleri.
- Dynamite and TNT30 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi. The Periodic Table of Videos (Nottingham Üniversitesi)