Nitrobenzen
 | |
 | |
 | |
| Adlandırmalar | |
|---|---|
Nitrobenzen | |
Diğer adlar Nitrobenzol Mirban yağı | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.002.469 |
| KEGG | |
PubChem CID | |
| RTECS numarası |
|
| UNII | |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Molekül formülü | C6H5NO2 |
| Molekül kütlesi | 123.11 g/mol |
| Görünüm | sarımsı, yağlı sıvı[1] |
| Koku | keskin kokulu, katı ayakkabı cilası gibi[1] |
| Yoğunluk | 1.199 g/cm3 |
| Erime noktası | 5.7 °C |
| Kaynama noktası | 210.9 °C |
| Çözünürlük (su içinde) | 0.19 g/100 ml (20 °C) |
| Buhar basıncı | 0.3 mmHg (25°C)[1] |
| -61.80•10−6 cm3/mol | |
| Akmazlık | 1.8112 mPa•s[2] |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |   |
| İşaret sözcüğü | Tehlike |
| R-ibareleri | R10, R23/24/25, R40, R48/23/24, R51/53, R62 |
| G-ibareleri | S1/2, S28, S36/37, S45, S61 |
| Tehlike ifadeleri | H301+H311+H331, H351, H360F, H372, H412 |
| Önlem ifadeleri | P201, P273, P280, P302+P352, P304+P340, P308+P310 |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | 88 °C |
Kendiliğinden tutuşma sıcaklığı | 480 °C |
| Patlama sınırları | %1.8-?[1] |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 780 mg/kg (sıçan, oral) 600 mg/kg (sıçan, oral) 590 mg/kg (fare, oral) [3] |
LDLo (yayınlanan en düşük) | 750 mg/kg (köpek, oral)[3] |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 1 ppm (5 mg/m3) [skin][1] |
| REL (tavsiye edilen) | TWA 1 ppm (5 mg/m3) [skin][1] |
| IDLH (anında tehlike) | 200 ppm[1] |
| Benzeyen bileşikler | |
Benzeyen bileşikler | Anilin Benzendiazonyum klorür Nitrozobenzen |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
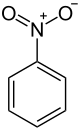
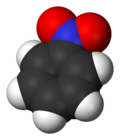
Nitrobenzen kimyasal formülü C6H5NO2 olan bir organik bileşiktir. Acıbadem benzeri bir kokuya sahip, suda çözünmeyen soluk sarı renkli bir yağdır. Donduğunda yeşilimsi sarı renkli kristallere dönüşür. Anilinin öncül maddesi olarak benzenden büyük ölçüde üretilir. Laboratuvarda, özellikle elektrofil reaktifler için, bazen bir çözücü olarak kullanılır.
Üretimi
Nitrobenzen, derişik sülfürik asit, su ve nitrik asit karışımı sayesinde benzenin nitrolanmasıyla hazırlanır. Bu karışıma bazen "karışık asit" adı verilir. Nitrobenzen üretimi, reaksiyonun ekzotermikliği (ΔH = −117 kJ/mol)[4] nedeniyle kimya endüstrisinde gerçekleştirilen en tehlikeli işlemlerden biridir.
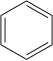 +
+ 
1985 yılında dünyadaki nitrobenzen kapasitesi yaklaşık 1.7×106 ton idi.[4]
Nitrolama işlemi nitronyum iyonunun (NO2+) oluşumu ve ardından bu iyonun benzen ile elektrofilik aromatik sübstitüsyon reaksiyonunu içerir. Nitronyum iyonu nitrik asit ve asidik bir dehidrasyon maddesinin(tipik olarak sülfürik asidin) reaksiyonu ile üretilir:
- HNO3 + H+
 NO2+ + H2O
NO2+ + H2O
Kullanımı
Nitrobenzenin yaklaşık % 95'I anilin üretiminde harcanır:[4]
- C6H5NO2 + 3 H2 → C6H5NH2 + 2 H2O
Anilin üretan polimerleri, lastik kimyasalları, pestisitler, boyar maddeler (özellikle azo boyar maddeler), patlayıcı maddeler ve ilaçlar için öncül bir maddedir.

Anilinin çoğu poliüretanların öncül maddesi olan metilendianilin üretiminde harcanır.
Özel uygulamalar
Nitrobenzen aynı zamanda ayakkabı ve zemin cilaları, deri kaplamalar, boya çözücüleri ve diğer malzemelerdeki hoş olmayan kokuları maskelemek için kullanılır. Mirban yağı olarak yeniden damıtılmış nitrobenzen sabunlar için ucuz bir parfüm olarak kullanılmıştır. Günümüzde, bu amaç için daha az toksik kimyasallar kullanılmaktadır.[5] Nitrobenzen için önemli bir ticaret pazarı ağrı kesici parasetamol (asetaminofen olarak da bilinir) (Mannsville 1991) üretiminde kullanımıdır.[6] Nitrobenzen, alışılmadık derecede büyük bir Kerr sabitine sahip olduğu için, Kerr hücrelerinde de kullanılır. Bulgular, tarımda bitki büyümesi / çiçeklenme uyarıcısı olarak kullanılmasını önermektedir.[7]
Organik reaksiyonlar
Aniline dönüşümünün yanı sıra, nitrobenzen seçime bağlı olarak azoksibenzene,[8] azobenzene,[9] nitrozobenzene,[10] hidrazobenzene,[11] ve fenilhidroksilamine[12] indirgenebilir. Skraup kinolin sentezi[13] gibi reaksiyonlarda zayıf bir yükseltgen olarak kullanılmıştır.
Güvenlik
Nitrobenzen oldukça toksiktir (Eşik sınır değeri 5 mg/m3) ve cilt yoluyla kolayca emilir.
Uzun süreli maruziyet merkezî sinir sisteminde ciddi hasara neden olabilir, görüşü bozabilir, karaciğer veya böbrek hasarına, anemi ve akciğer tahrişine neden olabilir. Buharların solunması baş ağrısı, bulantı, yorgunluk, baş dönmesi, siyanoz, kollarda ve bacaklarda güçsüzlüğe neden olabilir ve nadir durumlarda ölümcül olabilir. Yağ deriden kolayca emilir ve kalp atış hızını artırabilir, kasılmalara veya nadiren ölüme neden olabilir. Yutma, benzer şekilde baş ağrılarına, baş dönmesine, mide bulantısına, kusmaya ve sindirim sistemi tahrişine, uzuvlarda duyu / kullanım kaybına neden olabilir ve ayrıca iç kanamaya neden olabilir.[10]
Nitrobenzen, Birleşik Devletler Çevre Koruma Dairesi tarafından olası bir insan kanserojeni olarak kabul edilir,[14] ve IARC tarafından, "insanlar için kanserojen olabilir" demek olan Grup 2B kanserojen olarak sınıflandırılır.[15] Sıçanlarda karaciğer, böbrek ve tiroid tümörlerine ve kanserlerine neden olduğu gösterilmiştir.[16]
Kaynakça
- ^ a b c d e f g NIOSH Pocket Guide to Chemical Hazards. "#0450". National Institute for Occupational Safety and Health (NIOSH).
- ^ Ahluwalia, R.; Wanchoo, R. K.; Sharma, S. K.; Vashisht, J. L. (1996). "Density, viscosity, and surface tension of binary liquid systems: Ethanoic acid, propanoic acid, and butanoic acid with nitrobenzene". Journal of Solution Chemistry. 25 (9): 905-917. doi:10.1007/BF00972581. ISSN 0095-9782.
- ^ a b "Nitrobenzene". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ a b c Booth G (2007). "Nitro Compounds, Aromatic". Ullmann's Encyclopedia of Industrial Chemistry (6. bas.). Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_411. ISBN 978-3-527-30385-4.
- ^ Hogarth CW (Ocak 1912). "a case of poisoning by oil of mirbane (nitro-benzol)". British Medical Journal. 1 (2665): 183. doi:10.1136/bmj.1.2665.183. PMC 2344391 $2. PMID 20765985.
- ^ Bhattacharya A, Purohit VC, Suarez V, Tichkule R, Parmer G, Rinaldi F (Mart 2006). "One-step reductive amidation of nitro arenes: application in the synthesis of Acetaminophen". Tetrahedron Letters. 47 (11): 1861-1864. doi:10.1016/j.tetlet.2005.09.196.
- ^ "Flowering stimulant composition using nitrobenzene". 9 Ağustos 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2020.
- ^ "Azoxybenzene". echa.europa.eu (İngilizce). Substance Information - ECHA. 27 Aralık 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Nisan 2023.
- ^ "AZOBENZENE". Organic Syntheses.; Collective Volume, 3, s. 103
- ^ a b "NITROSOBENZENE". Organic Syntheses.; Collective Volume, 3, s. 668
- ^ Karwa, Shrikant L.; Rajadhyaksha, Rajeev A. (Ocak 1988). "Selective catalytic hydrogenation of nitrobenzene to hydrazobenzene". Industrial & Engineering Chemistry Research (İngilizce). 27 (1): 21-24. doi:10.1021/ie00073a005. ISSN 0888-5885.
- ^ "β-PHENYLHYDROXYLAMINE". Organic Syntheses.; Collective Volume, 1, s. 445
- ^ Clarke, HT; Davis, AW. "Quinoline". Organic Syntheses. 1: 478. 21 Haziran 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2020.
- ^ Division, US EPA, ORD, Integrated Risk Information System. "Nitrobenzene CASRN 98-95-3 - IRIS - US EPA, ORD". cfpub.epa.gov. 23 Ocak 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2017.
- ^ "Agents Classified by the IARC Monographs, International Agency for Research on Cancer" (PDF). 14 Mayıs 2011 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 10 Ağustos 2017.
- ^ National Institutes of Health • U.S. Department of Health and Human Services, Nomination: Nitrobenzene Review committee 21 Şubat 2017 tarihinde Wayback Machine sitesinde arşivlendi., 02/02/2010
Dış bağlantılar
- Uluslararası Kimyasal Güvenlik Kartı 00657 Ağustos 2018 tarihinde Wayback Machine sitesinde arşivlendi.
- Kimyasal Tehlikeler için NIOSH Cep Rehberi10 Ağustos 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- IARC Monograf: "Nitrobenzen"4 Mart 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- US EPA bilgi formu27 Haziran 2012 tarihinde Wayback Machine sitesinde arşivlendi.
- https://patents.google.com/patent/US91136289 Ağustos 2020 tarihinde Wayback Machine sitesinde arşivlendi.