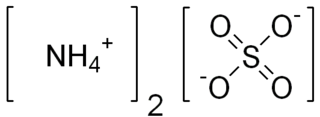Asit, pH derecesi 7'den düşük olup, değişen oranlarda yakıcı ve/veya aşındırıcı özelliğe sahip olan ve oldukça geniş kullanım alanına sahip kimyasal maddelere verilen isimdir. Suda çözündüklerinde hidrojen iyonu derişimini artırarak çözeltiyi asidik yapar. Mavi turnusol kâğıdının rengini kırmızıya çeviren asitlere eski Türkçede hamız veya ekşit denir.
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
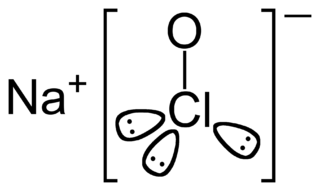
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.

Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Kükürt trioksit, suyla tepkimeye girdiğinde sülfürik asit oluşturan zehirli bir gazdır. Formülü SO3 şeklindedir. Kükürtlü asidi oluşturan sülfit iyonu (SO3 2-) ile karıştırılmamalıdır.

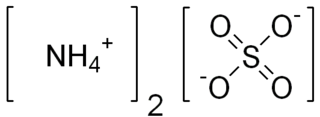
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.

Sodyum bisülfat, diğer bir adı sodyum hidrojen sülfat (NaHSO4) olan bu kimyasal madde asit tuz karakterlidir. Kuru halde iken güvenli bir şekilde nakledilebilir ve depolanabilir. Susuz formu higroskopiktir. Sodyum bisülfat suda hidroliz olarak asidik çözelti verir. 1 Molarlık çözeltisinin pH değeri 1 den küçüktür. Sodyum bisülfat yavaşça ısıtılırsa suyunu kaybederek sodyum pirosülfata dönüşür.
- 2NaHSO4 → Na2S2O7 + H2O

Potasyum sülfat, formülü K2SO4 olan, yanmaz, suda çözünebilen beyaz kristal yapıda bir potasyum tuzudur. Genellikle potasyum ve kükürt kaynağı olarak gübrelerde kullanılır.

Gümüş sülfat (Ag2SO4) gümüş kaplamada ve gümüş nitrat yerine boyanmayan madde olarak kullanılan gümüş iyonik bileşiği. Bu sülfat normal kullanım ve depolama durumunda kararlıdır fakat havaya ve ışığa maruz kaldığında kararır. Suda çok az çözünür.

Metil Metakrilat (MMA), CH
2C(CH
3)COOCH
3 formüllü organik bileşik. Metakrilik asitin Metil esteridir. Renksiz, yanıcı bir sıvıdır. Polimer üretimi için her yıl tonlarca MMA monomeri üretilir. Erime noktası -48 °C, kaynama noktası 101 °C'dir.
Permanganik asit, HMnO4 formülüne sahip bir inorganik bileşiktir. Bu güçlü oksoasit, dihidrat olarak izole edilmiştir. Permanganat tuzlarının konjugat asididir. Çok az sayıda yayın konusu olup, karakterizasyonu ve kullanımları çok sınırlıdır.
Amonyum hidroksit, oda sıcaklığında gaz hâlde bulunan amonyağın sulu çözeltisine verilen addır. Formülü olarak NH4+.OH- gösterilir.

Bakır karbonat, oda sıcaklığında katı hâlde bulunan bir inorganik bileşiktir. Havadan nem çeker. Su ile tepkimeye girerek bakır karbonat hidroksite dönüşür. Bazik özellik gösterir. Boya ve pigment olarak kullanılır.

Sezyum klorür, CsCl formülüne sahip inorganik bileşiktir. Bu renksiz tuz, çeşitli uygulamalarda önemli bir sezyum iyonu kaynağıdır. Kristal yapısı, her bir sezyum iyonunun 8 klor iyonu ile koordine edildiği önemli bir yapısal tip oluşturur. Sezyum klorür suda çözünür.
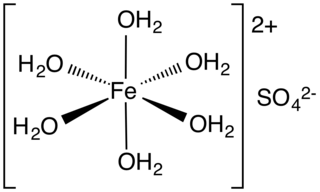
Demir (II) sülfat veya demir sülfat FeSO4•xH2O formülüne sahip bir dizi tuz anlamına gelir. Bu bileşikler en yaygın olarak heptahidrat (x = 7) olarak bulunursa da x için birkaç değer bilinmektedir. Hidratlı form tıp alanında demir eksikliğini tedavi etmek ve ayrıca endüstriyel uygulamalar için kullanılır. Antik çağlardan beri, Zaç-ı Kıbrıs ve yeşil vitriyol (vitriyol, sülfat için eski bir isimdir) olarak bilinen, mavi-yeşil heptahidrat (7 molekül su içeren hidrat) bu maddenin en yaygın şeklidir. Tüm demir (II) sülfatlar suda çözünerek oktahedral moleküler geometriye sahip ve paramanyetik olan aynı akua kompleksi [Fe(H2O)6]2+ verir.
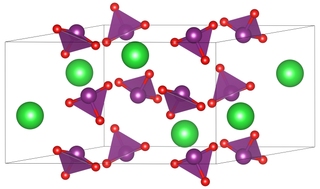
Baryum iyodat, kimyasal formülü Ba(IO3)2 olan inorganik bir kimyasal bileşiktir. Beyaz, granül bir maddedir.
Poliprotik asit terimi, molekül başına birden fazla proton sağlayabilen asitleri tanımlamak için kullanılır.

Kobalt(II) sülfat; CoSO4(H2O)x formülüne sahip inorganik bileşiklerden herhangi birine verilen isimdir. Genellikle sırasıyla kobalt sülfat, heksa- veya heptahidratları (CoSO4.6H2O or CoSO4.7H2O) tanımlar. Heptahidrat, suda ve metanolde çözünen kırmızı bir katıdır. Kobalt(II) tek sayıda elektrona sahip olduğu için tuzları paramanyetiktir.