Nöromiyelitis optika
Nöromiyelitis optika (NMO), optik sinir (optik nörit) ve omuriliğin (miyelit) enflamasyonu ile karakterize, otoimmün, inflamatuar ve demiyelinizan bir hastalıktır. Devic hastalığı olarak da bilinir. Optik nörit ve miyelit aynı anda veya art arda ortaya çıkabilir. NMO ilk kez Fernan Gault ve Eugene Devic tarafından keşfedilmiştir. 1894 yılında bu ikili NMO'yu akut ve ağır optik nörit ve miyelit olarak tanımlamışlardır. Monofazik olarak düşünülen bu hastalığın, 1996 yılında yineleyici bir seyir gösterebileceği kabul edilmiştir.

Multipl Skleroz (MS) ile klinik ve radyolojik açıdan benzerlikler gösteren NMO, uzun yıllar MS'in bir varyantı olarak kabul edilmiştir. 2004 yılında NMO Ig G antikorlarının, aquaporin-4 su kanalı moleküllerine karşı oluştuğu bulunmuş ve böylece MS'den farklılığı kanıtlanmıştır.
Semptomlar
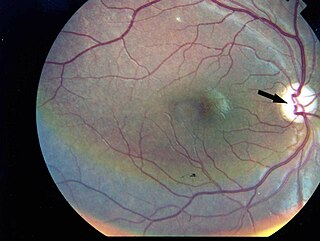
Optik nörit, tek taraflı veya çift taraflı olabilir. Görme kaybı ile birlikte gözün arkasında ağrı görülür. NMO hastalarında retinal lif tabakasının, MS hastalarına göre ince olduğu gözlemlenir. Yinelenen ataklarla birlikte retina liflerindeki incelme devam eder.
Miyelitte genellikle servikal ve dorsal omurilik bölümleri etkilenir. Üç ve daha fazla vertebral bölümü etkileyen transvers miyelit gözlemlenir.
Tetrapleji veya parapleji, simetrik duyu tutulumu, sfinkter disfonksiyonu, spazmlar ve ağrı görülen semptomlardandır. Miyelit ataklarında ise solunum yetmezliği, bulantı, kusma, hıçkırık gibi semptomlar görülebilir.
Klinik seyir

NMO, akut gelişen ağır optik nörit ve miyelit ataklarla karakterizedir. Hastalık başlangıcı öncesi grip, solunum yolu enfeksiyonu ve gastroenterit öyküsü mevcut hastaların sayısı fazladır.
NMO'da ataklar ağır geçer ve sekel bırakma riski fazladır. Atak öncesi baş ağrısı, uyuklama, mide bulantısı, ateş ve miyalji gibi belirtiler görülebilir.
Son yıllarda yapılan çalışmalarda NMO hastalarında posterior reversibl ensefalopati, hipotalamik disfonksiyon ve kognitif disfonksiyon görülmüştür.
Tanı
2015 yılında uluslararası bir panel tarafından yayınlanan tanı kriterlerinde AQP4 Ig G antikoru pozitif olan hastalar için en az bir temel klinik olması ve diğer hastalıkların dışlanması kabul edilmiştir.
Temel klinik kriterler
- Optik nörit
- Akut miyelit
- Area postrema sendromu (Açıklanamayan aşırı hıçkırık, bulantı atakları)
- Akut beyin sapı sendromu
- Semptomatik narkolepsi ya da akut diensefalik klinik sendromu
- Beyin lezyonlarıyla semptomatik serebral sendrom
Destekleyici kriterler
- Beyin MRG'sinde MS kriterlerini dışlama
- MRG'de omurilikte nispeten büyük bir lezyonu gösteren, 3 ya da daha fazla vertebral bölüme yayılan T2 ağırlıklı sinyal anormalliği
- Optik sinir MRG'si veya yörüngenin MRG'si normal bulgular, kayıtsız beyaz cevher lezyonları
- Alan Postrema Sendromu: Postrema alanında bir lezyon gösteren MRG
- Akut Beyin Sapı Sendromu: Periepandimal beyin sapında bir lezyon gösteren MRG
- Diğer olası tanıları dışlamak
Epidemiyoloji
Yapılan çalışmalarda gösterilen prevalansı ortalama milyonda 20 civarındadır. Hastalığın başlangıcı herhangi bir yaşta gözükse de genellikle 40 yaş civarında ağırlıktadır. Kadınlarda daha fazla görülmekle birlikte, kadın/erkek oranı ortalama 6/1'dır. NMO'da etnik gruplarda farklılık gözlenmemiştir. NMO'yu genetik faktörler ile ilişkilendiren çalışmalar olsa da genellikle bağımsızdır.
Tedavi
NMO'da ataklar ağır sekel bırakma eğiliminde olduğu için hızlı ve agresif bir tedavi uygulanması gerekir. Atak sırasında öncelikle 1 gr/gün intravenöz metilprednisolon tedavisi 5-10 gün arasında uygulanmalıdır. Sonrasında oral 1 mg/kg prednison ile bir ay devam edilmeli ve doz kademeli olarak azaltılarak 6 ile 12 ay arasında tamamen kesilmelidir. Bu tedaviye yanıt alınamayan hastalarda 5-7 seans plazmaferez uygulanabilir.
Steroid tedavisi uygulanan hastalarda tedavi aniden kesilmemelidir. Aksi takdirde atak tekrarlama riski yüksektir. Geleneksel MS ilaçları NMO'yu kötüleştirmektedir.
Atak sıklığını azaltmada azathiopirin kullanılır. Azathiopirini tolere edemeyen hastalarda mikofenolat mofetil tercih edilir. Günlük 2000 mg dozunun kullanımı atakları azalttığı gösterilmiştir. Diğer ilaçlara yanıt alamayan hastalarda rituximab yararlıdır. Tedavi sırasında hemorajik sistit gelişimini önlemek amacıyla profilaktik ürometiksan verilir.Folat takviyesi yapılmalıdır. Atak sonrası 5 yıl ataksızlık dönemi oluşturuluncaya kadar immünsüpretif tedavi devam etmelidir.
Rehabilitasyon
Yapılan sınırlı sayıdaki çalışmalarda NMO'lu hastalarda yoğun, multidisipliner bir rehabilitasyon programı sonucu nörolojik ve fonksiyonel kazanımlar sağlanabileceği gösterilmiştir.
NMO hastalarına üst ekstremite germe, kuvvetlendirme ve günlük aktiviteleri gerçekleştirmeye yönelik iş-uğraşı terapisi uygulanabilir. Hastalar el ince motor becerilerini arttırmaya yönelik günlük işlere yönlendirilmelidir. Hastalara alt ekstremite kuvvetlendirme, kondisyonu koruma ve arttırmaya yönelik aerobik egzersizler tavsiye edilir.
Ayrıca bakınız
Kaynakça
- Gault F(1894) De la Neuromyelite Optique aigue. These a la faculte de Medecine et de Pharmacie de Lyon 981.
- Rogers, JM, Panegyres, PK. Cognitive impairment in multiple sclerosis: evidence-based analysis and recommendations. J Clin Neurosci 2007; 14: 919– 927.10
- Lennon VA, Kryzer TJ, Pittock SJ, Verkman AS, Hinson SR. IgG marker of opticspinal multiple sclerosis binds to the aquaporin-4 water channel. J Exp Med. 2005; 202(4):473-477.
- Bobholz, JA, Rao, SM. Cognitive dysfunction in multiple sclerosis: a review of recent developments. Curr Opin Neurol 2003; 16: 283–288.
- Lennon VA, Wingerchuk DM, Kryzer TJ, et al. A serum autoantibody marker of neuromyelitis optica: distinction from multiple sclerosis. Lancet. 2004;364 (9451):2106-2112.
- Feinstein A. The neuropsychiatry of multiple sclerorosis. Can J Psychiatry 2004;49:157-63.
- Saji E, Toyoshima Y, Yanagawa K, Nishizawa M, Kawachi I (2010) Neuropsychiatric Presentation of Neuromyelitis Optica Spectrum Disorders. Neurology 74: A169
- Blanc F, Noblet V, Jung B, Rousseau F, Renard F, et al. (2012) White Matter Atrophy and Cognitive Dysfunctions in Neuromyelitis Optica. PLoS ONE 7(4)
- Blanc F, Zephir H, Lebrun C, Labauge P, Castelnovo G, et al. (2008) Cognitive functions in neuromyelitis optica. Arch Neurol 65: 84–88.
- Devic, E. (1894) Myelite subaigue compliquee de neurite optique. Bull Med. 8, 1033-1034.
- O'Riordan, J.I., Gallagher, H.L., Thompson, A.J., et al. (1996) Clinical, CSF, and MRI findings in Devic's neuromyelitis optica. J Neurol Neurosurg Psychiatry. 60(4), 382-387.
- Eraksoy, M., Akman-Demir, G. (2010) Merkezi sinir sisteminin miyelin hastalıkları.
- Siritho, S., Nakashima, I., Takahashi, T., et al. (2011) AQP4 antibody-positive Thai cases: clinical features and diagnostic problems. Neurology. 77, 827–834.
- Asgari, N., Lillevang, S.T., Skejoe, H.P., et al. (2011) A population-based study of neuromyelitis optica in Caucasians. Neurology. 76, 1589-1595.
- A. Emre Öge, Baykan B (ed.) Nöroloji 2. Baskı. Nobel Tıp kitabevi, İstanbul, s.603-629.
- Collongues, N., Marignier, R., Zephir, H., et al. (2011) Neuromyelitis optica in France: a multicenter study of 125 patients. Neurology. 74, 736–742.
- Kim, W., Kim, S.H., Nakashima, I., et al. (2012) Influence of pregnancy on neuromyelitis 51 optica spectrum disorder. Neurology. 78, 1264-1267.
- Matiello, M., Kim, H.J., Kim, W., et al. (2010) Familial neuromyelitis optica. Neurology. 75, 10–315.
- Matsushita, T., Matsuoka, T., Isobe, N., et al. (2009) Association of the HLA-DPB1*0501 allele with anti-aquoporin-4 antibody positivity in Japanese patients with idiopathic central nervous system demyelinating disorders. Tissue Antigens. 73, 171-176.
- Verkman, A.S. (2009) Knock-out models reveal new aquaporin functions. Handb Exp Pharmacol. 190, 359-381.
- Nagaishi, A., Takagi, M., Umemura, A., et al. (2011) Clinical features of neuromyelitis optica in a large Japanese cohort: comparison between phenotypes. J Neurol Neurosurg Psychiatry. 82, 1360–1364.
- Wingerchuck, D.M., Hogancamp, W.F., O'Brien, P.C., et al. (1999) The clinical course of neuromyelitis optica (Devic's syndrome). Neurology. 53, 1107-1114.
- Wingerhuck DM, Lennon VA, Pittock SJ et al. Revised diagnostic criteria for neuromyelitis optica. Neurology 2006; 66:1485-9.
- Wingerhuck DM, Lennon VA, Luchinetti CF et al. The spectrum of neuromyelitis optica.
- Lancet Neurol 2007; 6:805-15
- Iorio, R., Lucchinetti, C.F., Lennon, V.A., et al. Syndrome of inappropriate antidiuresis may herald or accompany neuromyelitis optica. Neurology. 77, 1644–1646.
- Nakamura, M., Nakazawa, T., Doi, H., et al. (2010) Early high-dose intravenous methylprednisolone is effective in preserving retinal nerve fiber layer thickness in patients with neuromyelitis optica. Graefes Arch Clin Exp Ophthalmol. 248, 1777–1785.
- Ghezzi, A., Bergamaschi, R., Martinelli, V., et al. (2004) Clinical characteristics, course and prognosis of relapsing Devic's Neuromyelitis optica. J Neurol. 251, 47-52
- Jarius, S., Ruprecht, K., Wildemann, B., et al. (2012) Contrasting disease patterns in seropositive and seronegative neuromyelitis optica: A multicentre study of 175 patients.
- Magana, S.M., Keegan, B.M., Weinshenker, B.G., et al. (2011) Beneficial plasma exchange response in central nervous system inflammatory demyelination. Arch Neurol. 68, 870–878.
- Warabi, Y., Matsumoto, Y., Hayashi, H. (2007) Interferon beta-1b exacerbates multiple sclerosis with severe optic nerve and spinal cord demyelination. J Neurol Sci. 252, 57–61.
- Axtell, R.C., Raman, C., Steinman, L. (2011) Interferon-beta exacerbates Th17-mediated inflammatory disease. Trends Immunol. 32, 272–277.
- Okamoto, T., Ogawa, M., Lin, Y., et al. (2008) Treatment of neuromyelitis optica: current debate. Ther Adv Neurol Disord. 1, 5–12.
- Kleiter, I., Hellwig, K., Berthele, A., et al. (2012) Failure of natalizumab to prevent relapses in neuromyelitis optica. Arch Neurol. 69, 239–245.
- Min, J.H., Kim, B.J., Lee, K.H. (2012) Development of extensive brain lesions following fingolimod (FTY720) treatment in a patient with neuromyelitis optica spectrum disorder. Mult Scler. 18, 113–115. 53
- Barnett, M., Prineas, J., Buckland, M., et al. (2011) Massive astrocyte destruction in neuromyelitis optica despite natalizumab therapy. Mult Scler. 18, 108-112.
- Costanzi, C., Matiello, M., Lucchinetti, C.F., et al. (2011) Azathiopirine: Tolerability, efficacy, and predictors of benefit in neuromyelitis optica. Neurology. 77, 659-666.
- Jacob, A., Matiello, M., Weinshenker, B.G., et al. (2009) Treatment of neuromyelitis optica with mycophenolate mofetil: retrospective analysis of 24 patients. Arch Neuro. 66, 1128–1133.
- Jacob, A., Weinshenker, B.G., Violich, I., et al. (2008) Treatment of neuromyelitis optica with rituximab: retrospective analysis of 25 patients. Arch Neurol. 65,1443–1448.
- Cree, B.A., Lamb, S., Morgan, K., et al. (2005) An open label study of the effects of rituximab in neuromyelitis optica. Neurology. 64, 1270–1272.
- Okada, K., Tsuji, S., Tanaka, K. (2007) Intermittent intravenous immunoglobulin succesfully prevents relapses of neuromyelitis optica. Intern med. 46(19), 1671-1672.
- Kim, S.H., Kim, W., Park, M.S., et al. (2011) Efficacy and safety of mitoxantrone in patients with highly relapsing neuromyelitis optica. Arch Neurol. 68, 473–479.
- Bakker, J., Metz, L. (2004) Devic's neuromyelitis optica treated with intravenous gammaglobulin (IVIG). Can J Neurol Sci. 31(2), 265-267.
- Weinstock-Guttman, B., Ramanathan, M., Lincoff, N., et al. (2006) Study of mitoxantrone for the treatment of recurrent neuromyelitis optica (Devic disease). Arch Neurol. 63, 957–963.
- Wingerchuck, D.M. (2012) Neuromyelitis optica: Potential Roles for Intravenous Immunoglobulin. J Clin Immunol. Doi:10.1007/s10875-012-9796-7.
- Weinshenker, B.G., Wingerchuk, D.M., Vukusic, S., et al. (2006) Neuromyelitis optica IgG predicts relapse after longitudinally extensive transverse myelitis. Ann Neurol. 59(3), 566-569.
- Won Bin Kim 1, So Young Lee, Bo Ryun Kim, Youn Ji Kim (2019) Rehabilitation of neuromyelitis optica: Two CARE-compliant case reports.