
Elektron dizilimi, atom fiziği ve kuantum kimyasında, bir atom ya da molekülün elektronlarının atomik ya da moleküler orbitallerdeki dağılımıdır. Örneğin Neon atomunun elektron dizilimi 1s2 2s2 2p6 olarak gösterilir.

Bir fizik terimi olarak maddenin hâli, maddenin aldığı farklı fazlardır. Günlük hayatta maddenin dört farklı hâl aldığı görülür. Bunlar; katı, sıvı, gaz ve plazmadır. Maddenin başka hâlleri de bilinir. Örneğin; Bose-Einstein yoğunlaşması ve nötron-dejeneje maddesi. Fakat bu hâller olağanüstü durumlarda gerçekleşir, çok soğuk ya da çok yoğun maddelerde. Maddenin diğer hâllerininde, örneğin quark-gluon plazmalar, mümkün olduğuna inanılır fakat şu an sadece teorik olarak bilinir. Tarihsel olarak, maddenin özelliklerindeki niteleyici farklılıklara dayanarak ayrım yapılır. Katı hâldeki madde bileşen parçaları ile bir arada tutulur ve böylece sabit hacim ve şeklini korur. Sıvı hâldeki madde hacmini korur fakat bulunduğu kabın şeklini alır. Bu parçalar bir arada tutulur ama hareketleri serbesttir. Gaz hâlindeki madde ise hem hacim olarak hem de şekil olarak bulunduğu kaba ayak uydurur.Bu parçalar ne beraber ne de sabit bir yerde tutulur. Maddenin plazma hâli ise, nötr atomlarda dahil, hacim ve şekil olarak tutarsızdır. Serbestçe ilerleyen önemli sayıda iyon ve elektron içerirler. Plazma, evrende maddenin en yaygın şekilde görülen hâlidir.

Organik kimya, organik bileşiklerin ve organik maddelerin yani karbon atomlarını içeren çeşitli formlardaki maddelerin yapısını, özelliklerini ve reaksiyonların bilimsel çalışmasını içeren, kimyanın bir alt dalıdır. Yapının incelenmesi yapısal formüllerini belirler. Özelliklerin incelenmesi, fiziksel ve kimyasal özellikleri ve davranışlarını anlamak için kimyasal reaktivitenin değerlendirilmesidir. Organik reaksiyonların incelenmesi doğal ürünlerin, ilaçların ve polimerlerin kimyasal sentezini ve bireysel organik moleküllerin laboratuvarda ve teorik çalışma yoluyla incelenmesidir.

Kovalent bağ, atomlar arasında elektron çiftleri oluşturmak için elektronların paylaşımını içeren kimyasal bağdır. Bu elektron çiftlerine paylaşılan çiftler veya bağ çiftleri denir. Atomlar arasında elektronları paylaştıklarında çekici ve itici kuvvetlerin kararlı dengesine kovalent bağ denir. Birçok molekül için elektronların paylaşılması her atomun kararlı elektronik gruplaşmasına denk gelen tam değerlik kabuğunun eşdeğerine ulaşmasına olanak tanır.

Enerji seviyesi, atom çekirdeğinin etrafında katman katman biçiminde bulunan kısımların her biridir. Bu yörüngelerde elektronlar bulunur. Yörüngenin numarası; 1, 2, 3, 4, ... gibi sayı değerlerini alabilir. Yörünge numarasına baş kuantum sayısı da denir ve "n" ile gösterilir. Yörünge numarası ile yörüngenin çekirdeğe uzaklığı doğru orantılıdır.
Süblimleşme, katı maddelerin ısıtılınca, ara bir hâl olan sıvı hâle geçmeden doğrudan gaz hâle geçmesi. Süblimleşme endotermik faz değişimidir. Faz diyagramındaki üçlü noktanın altında gerçekleşir. Süblimleşme'nin tersine ise kırağılaşma denir.
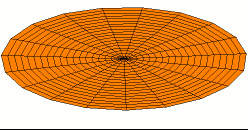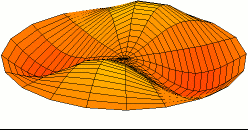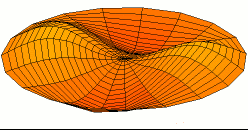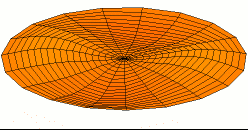
Titreşim bir denge noktası etrafındaki mekanik salınımdır. Bu salınımlar bir sarkaçın hareketi gibi periyodik olabileceği gibi çakıllı bir yolda tekerleğin hareketi gibi rastgele de olabilir.

Fosforesans, floresansla ilişkili bir çeşit ışıldama şeklidir. Floresanstan farklı olarak fosforesant maddeler soğurdukları enerjiyi hızlıca geri vermezler.

Kimyada istiflenme, genelde aromatik olan moleküllerin atomlar arası etkileşerek deste şeklinde üst üst üste gelmesidir. İstiflenmiş bir sistemin en yaygın bilinen örneği DNA molekülünde birbirini takibeden bazlarda görülür. İstiflenme proteinlerde, non-polar iki halkanın örtüşmesi halinde de meydana gelir. Hangi moleküllerarası kuvvetlerin istiflenmeye neden olduğu hâlen tartışma konusudur.

Organik kimyada bazı atom halkalarının yapısı beklenenin üstünde kararlıdır. Doymamış bağlar, yalın elektron çiftleri veya boş orbitallerden oluşan konjüge bir halkanın konjüge olmasından beklenecek kararlılıktan daha yüksek bir kararlılık gösterme özelliğine aromatiklik denir. Aromatiklik, halkasal delokalizasyon ve rezonansın bir belirtisi olarak da düşünülebilir.

Rydberg atomu çok yüksek temel nicem sayılı bir veya iki elektrona sahip bir uyarılmış atomdur Bu atomlar elektrik ve manyetik alana abartılı tepkiler vermeyi de içinde barındıran, uzun bozunma devri ve yaklaşık elektron dalgafonksiyonları, bazı şartlar altında çekirdekler etrafındaki elektronların klasik yörüngeleri gibi kendilerine has birçok özelliğe sahiptir. Çekirdek elektronları dış elektronları çekirdeğin elektrik alanından kalkanlar, öyle ki belirli bir mesafeden hidrojen atomundaki bir elektronun tecrübe ettiği gibi elektrik potansiyeli belirleyicidir.
Atomik, moleküler ve optik fizik, bir ya da birkaç atomun ölçeğinde, madde-madde ve ışık-madde etkileşimi çalışmadır ve enerji, birkaç elektron voltları etrafında ölçeklenir. Üç alanla yakından ilişkilidir. AMO teorisi, klasik, yarı klasik ve kuantum işlemlerini kapsar. Tipik olarak, teori ve emisyon uygulamaları, elektromanyetik yayılım ve emilme, spektroskopi analizi, lazer ve mazerlerin kuşağı ve genel olarak maddenin optik özellikleri, uyarılmış atom ve moleküllerden, bu kategorilere ayrılır.

Yoğunlaşma veya yoğuşma, maddenin fiziksel halinin gaz fazından sıvı faza değişimi ve buharlaşmanın tersidir. En sık su döngüsü anlamında kullanılır. Atmosfer içinde bir sıvı veya katı bir yüzey veya Yoğunlaşma bulutu ile temas ettiğinde, su buharının sıvı suya değişmesi olarak da tanımlanabilir. Doğrudan gaz fazdan katı faza geçiş gerçekleştiğinde, değişime kırağılaşma denir.

Franck–Condon ilkesi, spektroskopide ve kuantum kimyasında bir kuraldır ve titreşimsel geçişlerin yoğunluğu olarak açıklanır. Titreşimsel geçişler uygun enerjideki fotonların emme ve emisyonundan dolayı elektronik ve titreşimsel enerji seviyelerinde eş zamanlı değişiklik olur. Prensip belirtiyor ki, elektronik geçiş sırasında eğer bu iki titreşimsel dalga fonksiyonları büyük ölçüde aşar ise bir titreşimsel enerji seviyesinden diğerine değişiklik olur.
Hesaplamalı kimya, kimya problemlerini çözmeye yardımcı olmak için bilgisayar simülasyonunu kullanan bir kimya dalıdır. Moleküllerin, katıların yapı ve özelliklerini hesaplamak için verimli bilgisayar programlarına dahil edilmiş teorik kimya yöntemlerini kullanır. Bu yöntemlerin kullanılmasının nedeni, hidrojen moleküler iyonu ile ilgili nispeten yeni sonuçlar dışında, kuantum çok-gövdeli(many-body) problemlerin analitik olarak çözülemez oluşudur. Hesaplama sonuçları normal olarak kimyasal deneylerle elde edilen bilgileri tamamlarken, bazı durumlarda gözlemlenmeyen kimyasal olayları da tahmin edebilmektedir. Yeni ilaç ve materyallerin tasarımında yaygın olarak kullanılmaktadır.

Azulen organik bir bileşiktir ve Naftalinin bir izomeridir. Naftalinin renksiz olmasına karşın, azulen koyu mavi bir renge sahiptir. İki terpenoid, vetivazulen (4,6-dimetil-2-izopropilazulen) ve guaiazulen (1,4-dimetil-7-izopropilazulen), bu özelliklere sahip azulen iskeletli maddeler, doğal olarak mantar pigmentlerinde, Peygamber ağacı yağında ve bazı deniz omugasızlarında bulunabilir.

Spartan, Wavefunction'ın moleküler modelleme ve bilgisayarlı kimya uygulamasıdır. Moleküler mekanik, yarı-ampirik yöntemler, ab initio modeller, yoğunluklu fonksiyonel modeller, post Hartree-Fock modeller, G3 (MP2) ve T1 içeren termokimyasal tarifler için kodlar içerir.
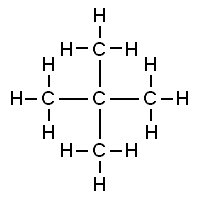
2,2-dimetilpropan olarak da adlandırılan neopentan, beş karbon atomlu çift dallı zincirli bir alkandır. Neopentan, oda sıcaklığında ve basıncında yanıcı bir gazdır, soğuk bir günde, bir buz banyosunda veya daha yüksek bir basınca sıkıştırıldığında oldukça uçucu bir sıvıya dönüşebilir.
Marcus teorisi, ilk olarak Rudolph A. Marcus tarafından 1956'da başlayarak, elektron transfer reaksiyonlarının oranlarını açıklamak için geliştirilen bir teoridir. Bir elektronun bir kimyasal türden bir diğerine geçişindeki oranlarla ilgilenir.

Erich Armand Arthur Joseph Hückel, Alman fizikçi ve fiziksel kimyagerdir. İki büyük katkısıyla tanınmaktadır.
- Debye-Hückel elektrolitik çözelti teorisi
- π elektron sistemlerinde yaklaşık moleküler orbital (MO) hesaplamaları için Hückel yöntemi.















