Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.

Gübre, bitkinin beslenmesinde gerekli olan kimyasal elementleri sağlamak için toprağa ilave edilen herhangi bir madde.

Klor, VIIA grubunda bulunan hafif, keskin kokulu, yeşilimsi sarı renkli, tahriş edici ve zehirleyici bir gaz. Havadan 2,5 kat ağır olan klor ilk zamanlar bir bileşik olarak kabul ediliyordu. Klor ilk olarak 1774 yılında Carl Wilhelm Scheele tarafından keşfedildi. 1810 yılında ise bugünkü ismi Humphry Davy tarafından verildi.

Molibden, periyodik cetvelde atom numarası 42 ve simgesi Mo olan elementtir..
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.

Kobalt kimyasal bir element'tir. Sembol'ü Co ve atom numarası 27'dir. Nikel gibi kobalt da, doğal meteorik demir alaşımlarında bulunan küçük birikintiler dışında, yer kabuğunda yalnızca kimyasal olarak birleşik formda bulunur. İndirgeyici eritme yoluyla üretilen serbest element sert, parlak, gümüş rengi bir metal'dir.

Kral suyu, asitlerin az etki ettiği ya da etki etmediği altın ve platin gibi metallerle tepkimeye girebilen kuvvetli bir asit çözeltisidir. Hidroklorik asit ve nitrik asitin 3:1 oranında karıştırılmasıyla oluşur. Ebu Musa Câbir bin Hayyan tarafından bulunduğu tahmin edilmektedir.
Klorür, nötr hâldeki klor atomunun, bir elektron alarak iyon (anyon) hâline geçtiğinde aldığı isim. Cl− olarak gösterilir. Klorür iyonu içeren maddelere de verilen bir isimdir. Bir iyon olduğundan dolayı, kendi başına doğada yer almaz; ancak bir çözeltide karşı iyonu ile yer alabilir.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Kimyasal buğu taşınımı, uçucu olmayan katıları billurlaştırmak ya da saflaştırmak için kullanılan yöntem. Schäfer tarafından yaygınlaştırılan bu tekniğin temel prensibi, taşınım sırasında uçucu olmayan bileşiklerin uçucu türevlerine tersinir dönüşümüdür. Bu özelliği ile benzer bir metot ancak biriktirme için bileşiğin uçucu öncüllerinin kullanıldığı kimyasal buhar biriktirmeden ayrılır. Ancak, iyodürün etkin madde olarak kullanıldığı Van Arkel-de Boer işlemi ile benzerlik taşır. Titanyum ve vanadyumun saflaştırılması için kullanılan bu yöntemden esinlenilmiş olması muhtemeldir.

Papa VI. Paulus Papa VI. Paulus, 1963 - 1978 yılları arasında papaydı.

Liqui Moly GmbH, sentetik yağ, motor yağı, yağlayıcı madde, yağ katkısı konusunda uzmanlaşmış bir Alman firmasıdır. 1 Ocak 2018'den itibaren Liqui Moly, önceki çoğunluk sahibi ve CEO Ernst Prost'un kalan hisselerini alan Würth Grubu'nun bir parçasıdır.
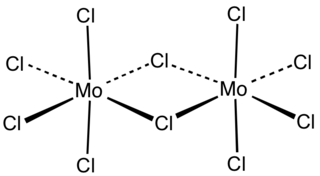
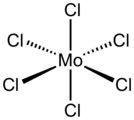
Molibden (V) klorür, [MoCl5]2 formülüne sahip olan bir bileşiktir. Bu koyu uçucu katı, diğer molibden bileşiklerini hazırlamak için araştırmada kullanılır. Neme duyarlıdır ve klorlu çözücülerde çözünür. Genelde molibden pentaklorür denir ve aslında Mo2Cl10 formüllü bir dimerdir.

Kloroplatinik asit (hekzakloroplatinik asit olarak da bilinir), [H3O]2[PtCl6](H2O)x (0≤x≤6) formülüne sahip bir inorganik bileşiktir. Kırmızı bir katı, genellikle sulu bir çözelti olarak önemli bir platin kaynağıdır. Genellikle kısaca H2PtCl6 olarak yazılsa da, hekzakloroplatinat anyonunun (PtCl62-) hidronyum (H3O+) tuzudur. Hekzakloroplatinik asit oldukça higroskopiktir.
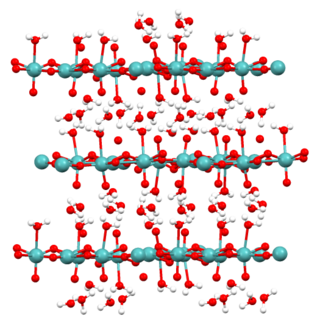
Molibdik asit, molibden trioksit ve ilgili türlerin hidratlanmış formlarını ifade eder. Monohidrat (MoO3·H2O) ve dihidrat (MoO3·2H2O) iyi karakterize edilir. Sarı diyamanyetik katılardır.

Sodyum klorür, yaygın olarak 'tuz' ismiyle bilinen kimyasal formülü NaCl; 1/1 oranında sodyum ve klorür iyonları olan iyonik bileşik. Molar kütleleri sırasıyla 22.99 ve 35.45 g/moldur. 100 g NaCl, 39.34 g Na ve 60.66 g Cl içerir. Sodyum klorür, deniz suyunun tuzluluğundan ve birçok çok hücreli organizmanın hücre dışı sıvısından en çok sorumlu olan tuzdur. Yenilebilir sofra tuzu biçiminde yaygın olarak bir çeşni ve gıda koruyucusu olarak kullanılır. Birçok endüstriyel proseste büyük miktarlarda sodyum klorür kullanılır ve daha ileri kimyasal sentezler için hammadde olarak kullanılan sodyum ve klor bileşiklerinin ana kaynağıdır. Sodyum klorürün ikinci bir ana uygulaması donma sıcaklığı altındaki havalarda yolların buzunun çözülmesidir.
Demir (III) klorür FeCl
3 formüllü inorganik bir bileşiktir. Kristal bir katı olmasının yanı sıra görüş açısına bağlı olarak farklı renklerle gözlemlenebilir; koyu yeşil, mor-kırmızı. Sulu formu da katı formu da fiziksel görünüm olarak koyu kahverengi rengindedir.
Renyum klorür deyimi genel bir ifade tarzı olup aşağıdaki anlamlardan herhangi birini ifade edebilir:
- Trirenyum nonaklorür (renyum(III) klorür/Renyum triklorür), Re3Cl9
- Renyum pentaklorür (renyum(V) klorür), ReCl5
- Renyum(IV) klorür (renyum tetraklorür), ReCl4
- Renyum(VI) klorür (renyum hekzaklorür), ReCl6

Magnezyum klorür, MgCl
2 formülüne sahip kimyasal bileşiğin adıdır. Susuz şekline ek olarak, MgCl
2 çeşitli hidratlar MgCl
2·nH
2O şeklinde olur. Bu tuzlar, suda oldukça çözünür olan tipik iyonik halojenürlerdir. Magnezyum klorür tuzlu su veya deniz suyundan ekstrakte edilebilir. Kuzey Amerikada, magnezyum klorür esas olarak Büyük Tuz Gölü tuzlu suyundan üretilir. Ürdün Vadisi'ndeki Lut Gölü'nden benzer bir işlemle çıkarılır. Mineral bişofit olarak magnezyum klorür de eski deniz yataklarından, örneğin kuzeybatı Avrupa'daki Zechstein deniz yatağından çıkarılır. Bu, ilk okyanustaki yüksek magnezyum klorür içeriği ile açıklanabilir. Bazı magnezyum klorür deniz suyunun buharlaşmasından yapılır. Susuz magnezyum klorür, büyük ölçekte üretilen magnezyum metalinin başlıca öncüsüdür. Hidratlı magnezyum klorür en kolay bulunabilen formdur.

Vanadyum tetraklorür ya da vanadyum(IV) klorür, VCl4 formüllü bir inorganik bileşiktir. Kırmızımsı kahverengi bir sıvı olup vanadyum bileşiklerinin hazırlanmasında reaktif olarak kullanılır. Vanadyumun klorlanmasıyla meydana gelir.