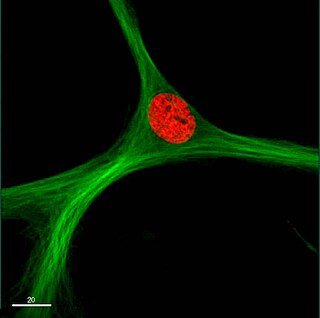
Miyogenez
Miyogenez, özellikle embriyonik gelişim sırasında iskelet kas dokusunun oluşumudur.

Kas lifleri genellikle öncü miyoblastların miyotüp adı verilen çok çekirdekli liflere füzyonu yoluyla oluşur. Bir embriyonun erken gelişiminde, miyoblastlar çoğalabilir veya bir miyotüpte farklılaşabilir. Bu seçimi in vivo olarak neyin kontrol ettiği genellikle belirsizdir. Hücre kültürüne yerleştirilirse, hücreleri çevreleyen ortamda yeterli fibroblast büyüme faktörü (FGF) veya başka bir büyüme faktörü varsa, miyoblast çoğalır. Büyüme faktörü tükendiğinde, miyoblastlar bölünmeyi durdurur ve miyotüplere terminal farklılaşmaya uğrar. Myoblast farklılaşması aşamalar halinde ilerler.
Farklılaşmanın Aşamaları
İlk aşama, hücre döngüsü çıkışını ve belirli genlerin ekspresyonunun başlamasını içerir.
Farklılaşmanın ikinci aşaması, miyoblastların birbirleriyle hizalanmasını içerir. Çalışmalar, sıçan ve civciv miyoblastlarının bile birbirlerini tanıyıp birbirleriyle hizalandığını göstermiştir, bu da ilgili mekanizmaların evrimsel olarak korunmasını önermektedir.
Üçüncü aşama, gerçek hücre füzyonunun kendisidir. Bu aşamada kalsiyum iyonlarının varlığı kritiktir. Farelerde, füzyona, meltrinler adı verilen bir dizi metaloproteinaz ve halen araştırılmakta olan çeşitli diğer proteinler yardımcı olur. Füzyon, aktinin plazma membranına alınmasını, ardından yakın yerleştirmeyi ve daha sonra hızla genişleyen bir gözenek oluşturmayı içerir.
Miyogenezi Destekleyen Miyosit Arttırıcı Faktörler (MEF)
Mef2
Moleküler biyoloji alanında, miyosit arttırıcı faktör-2 (Mef2 ) proteinleri, gen ekspresyonunun kontrolü yoluyla hücresel farklılaşmanın önemli düzenleyicileri olan ve dolayısıyla embriyonik gelişimde kritik bir rol oynayan bir transkripsiyon faktörleri ailesidir. Yetişkin organizmalarda, Mef2 proteinleri bazı dokularda stres tepkisine aracılık eder. Mef2 proteinleri hem MADS kutusu hem de Mef2 DNA bağlama alanları içerir .
Keşif
Mef2 başlangıçta kas farklılaşması sırasında mck güçlendirici bölge ile etkileşime giren nükleer faktörleri tanımlamak için kas kreatin kinaz (mck) geninin promoter analizi yoluyla bir transkripsiyon faktör kompleksi olarak tanımlandı.[1] RSRF (Serum Yanıt Faktörü ile İlgili) olarak adlandırılan üç insan mRNA kodlama dizisi klonlandı ve dimerize olduğu, MCK güçlendirici bölgesinde mevcut olana benzer bir konsensüs dizisini bağladığı ve transkripsiyonu tahrik ettiği gösterildi.[2] RSRF'lerin daha sonra artık Mef2A, Mef2B ve Mef2D olarak adlandırılan insan genlerini kodladığı gösterildi.
Tür dağılımı
Mef2 geni, mayadan insanlara kadar tüm ökaryot dallarında geniş çapta ifade edilir . Drosophila'nın tek bir Mef2 genine sahip olmasına rağmen, omurgalılar Mef2 geninin en az dört versiyonuna sahiptir (insan versiyonları MEF2A, MEF2B, MEF2C ve MEF2D olarak adlandırılır ), hepsi yetişkinlik boyunca embriyojenez sırasında farklı ancak örtüşen modellerde ifade edilir.[3]
Sıra ve yapı
Memeli Mef2 genlerinin tümü, yüksek oranda korunmuş N-terminal MADS-kutusu ve Mef2 alanları boyunca yaklaşık% 50 genel amino asit özdeşliği ve yaklaşık% 95 benzerlik paylaşır, ancak dizileri C-terminal transaktivasyon alanında farklılaşır (bkz. Sağdaki şekil ).[4]
MADS kutusu, minimum DNA bağlama alanı görevi görür, ancak yüksek afiniteli DNA bağlama ve dimerizasyon için Mef2 alanı adı verilen bitişik bir 29 amino asit uzantısı gereklidir. MADS kutusu ile etkileşim yoluyla, Mef2 transkripsiyon faktörleri homo- ve heterodimerize etme yeteneğine sahiptir[5] ve Mef2A, -C ve - D'nin C terminalindeki klasik bir nükleer lokalizasyon sekansı (NLS ) nükleer lokalizasyonu sağlar proteinin.[6] D-Mef2 ve insan MEF2B, bu korunmuş NLS'den yoksundur ancak yine de çekirdekte bulunur.[7]
Fonksiyon
Geliştirme
In Drosophila, MEF2 kas gelişimini düzenler.[8] Memeli Mef2, kültürdeki kas dışı hücreleri kasa dönüştürmek için bHLH transkripsiyon faktörleriyle işbirliği yapabilir.[9] bHLH faktörleri Mef2c ekspresyonunu etkinleştirebilir, bu da daha sonra kendi ifadesini sürdürme görevi görür.[10]
Nöral krest hücrelerinde Mef2c kaybı, gelişmekte olan embriyoda kraniyofasiyal kusurlara ve üst hava yolu pasajlarının bloke edilmesinden kaynaklanan neonatal ölüme neden olur.[11][12] Mef2c, kraniyofasiyal gelişim için gerekli olan iki transkripsiyon faktörü olan homeodomain transkripsiyon faktörleri DLX5 ve DLX6'nın ekspresyonunu yukarı düzenler.[11][12]
Stres tepkisi
Yetişkin dokularda, Mef2 proteinleri kardiyak hipertrofi[13] sırasındaki stres yanıtı ve kalp ve iskelet kasında doku yeniden şekillenmesini düzenler.[14]
Kardiyovasküler sistem
Mef2, kalp gelişimi ve kardiyak gen ekspresyonunda kritik bir düzenleyicidir.[15] Omurgalılarda, Mef2 transkripsiyon faktör ailesinde dört gen vardır: Mef2a, Mef2b, Mef2c ve Mef2d. Her biri geliştirme sırasında belirli zamanlarda ifade edilir. Kalpte ifade edilecek ilk gen olan Mef2c, kalp çıkış yolunun ve sağ ventrikülün çoğunun bileşenlerinin oluşturulmasına yardımcı olan ön (ikincil) kalp alanının (AHF) gelişimi için gereklidir.[16][17] Ek olarak, Mef2 genleri, mevcut damarlardan yeni kan damarlarının oluşumu olan anjiyogenezin filizlenmesine yardımcı olmak için gen ekspresyonunu etkinleştirmede endikedir.[18]
Nakavt çalışmaları
Farelerde, Mef2c'nin nakavt çalışmaları, kalp gelişiminde oynadığı çok önemli rolü göstermiştir. Mef2c'siz fareler, uygun olmayan döngü, çıkış yolu anormallikleri ve sağ ventrikülün tamamen yokluğu dahil olmak üzere önemli kalp kusurları ile embriyonik gün 9.5-10.[15] Bu, ön kalp alanının uygunsuz farklılaşmasını gösterir. Mef2c özellikle AHF'de devre dışı bırakıldığında, fareler doğumda bir dizi çıkış yolu kusuru ve şiddetli siyanoz ile ölür. Bu nedenle, özellikle ön kalp alanını düzenleyerek, kalp gelişiminin birçok yönü için Mef2 gereklidir.[16]
Ek Bilgiler
MEF2, Myocyte Enhancer Factor 2, MEF2A, B, C ve D gibi dört spesifik sayıya sahip bir transkripsiyon faktörüdür. Her MEF2 geni belirli bir kromozom üzerinde bulunur. MEF2'nin kalbin (Chen) gelişimi ve döngüsüne dahil olduğu bilinmektedir. MEF2 miyosit farklılaşması ve gen aktivasyonu için gereklidir (Siyah). Her iki rol de kalp yapısına katkıda bulunur ve embriyonik gelişimde MEF2 ile bir bozulma varsa, iki fenotipik soruna (Karamboulas) yol açabilir. Tip-I fenotip, kalpte ciddi malformasyonlara neden olabilir ve tip-II fenotipi normal görünmesine rağmen, kalp yetmezliğine neden olabilen ince duvarlı bir miyokardiyuma sahiptir. Ortaya çıkabilecek diğer bir sorun, nakavt gen MEF2C'den kaynaklanmaktadır. MEF2C'nin, Tdgf1 (teratokarsinomdan türetilmiş büyüme faktörü 1) ile ilişkili olduğunda doğuştan kalp hastalığı ile doğrudan ilişkili olduğu bilinmektedir. MEF2C, Tdgf1'i uygunsuz bir şekilde düzenlerse, özellikle kalbin embriyonik gelişiminde gelişimsel kusurlar ortaya çıkar. (Chen). MEF2C'nin Tdgf1 proteini ile etkileşim yolu, farklı mekanizmaları düzenlemek için gerekli olan 〖Ca〗 ^ (2+) sinyal yoludur. Küçük olmayan kodlayıcı RNA'lar olan MicroRNA'lar da MEF2C'nin düzenlenmesinde özel bir rol oynar. Doğuştan kalp hastalığının ifadesi, mikroRNA miR-29C'nin (Chen) aşağı regülasyonu nedeniyle yukarı regüle edilir. MEF2 ailesiyle ilişkili diğer birkaç bilinen hastalık, karaciğer fibrozu, kanserler ve nörodejeneratif hastalıklardır (Chen).
Kaynakça
- ^ Gossett, L A; Kelvin, D J; Sternberg, E A; Olson, E N (Kasım 1989). "A new myocyte-specific enhancer-binding factor that recognizes a conserved element associated with multiple muscle-specific genes". Molecular and Cellular Biology. 9 (11): 5022-5033. doi:10.1128/mcb.9.11.5022. ISSN 0270-7306.
- ^ Pollock, R; Treisman, R (1 Aralık 1991). "Human SRF-related proteins: DNA-binding properties and potential regulatory targets". Genes & Development. 5 (12a): 2327-2341. doi:10.1101/gad.5.12a.2327. ISSN 0890-9369.
- ^ McKinsey, Timothy A; Zhang, Chun Li; Olson, Eric N (Ocak 2002). "MEF2: a calcium-dependent regulator of cell division, differentiation and death". Trends in Biochemical Sciences. 27 (1): 40-47. doi:10.1016/s0968-0004(01)02031-x. ISSN 0968-0004.
- ^ Black, Brian L.; Olson, Eric N. (Kasım 1998). "TRANSCRIPTIONAL CONTROL OF MUSCLE DEVELOPMENT BY MYOCYTE ENHANCER FACTOR-2 (MEF2) PROTEINS". Annual Review of Cell and Developmental Biology. 14 (1): 167-196. doi:10.1146/annurev.cellbio.14.1.167. ISSN 1081-0706.
- ^ Molkentin, J. D.; Olson, E. N. (3 Eylül 1996). "Combinatorial control of muscle development by basic helix-loop-helix and MADS-box transcription factors". Proceedings of the National Academy of Sciences. 93 (18): 9366-9373. doi:10.1073/pnas.93.18.9366. ISSN 0027-8424.
- ^ Borghi, Serena; Molinari, Susanna; Razzini, Giorgia; Parise, Flavia; Battini, Renata; Ferrari, Stefano (15 Aralık 2001). "The nuclear localization domain of the MEF2 family of transcription factors shows member-specific features and mediates the nuclear import of histone deacetylase 4". Journal of Cell Science. 114 (24): 4477-4483. doi:10.1242/jcs.114.24.4477. ISSN 1477-9137.
- ^ Chavdarov, Anatoliy V (28 Haziran 2020). "DEVELOPING TECHNOLOGY OF CREATING WEAR-RESISTANT CERAMIC COATING FOR ICE CYLINDER". JOURNAL OF MECHANICS OF CONTINUA AND MATHEMATICAL SCIENCES. spl10 (1). doi:10.26782/jmcms.spl.10/2020.06.00048. ISSN 0973-8975. 9 Haziran 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Mart 2022.
- ^ Lilly, B.; Galewsky, S.; Firulli, A. B.; Schulz, R. A.; Olson, E. N. (7 Haziran 1994). "D-MEF2: a MADS box transcription factor expressed in differentiating mesoderm and muscle cell lineages during Drosophila embryogenesis". Proceedings of the National Academy of Sciences. 91 (12): 5662-5666. doi:10.1073/pnas.91.12.5662. ISSN 0027-8424.
- ^ Molkentin, Jeffery D.; Black, Brian L.; Martin, James F.; Olson, Eric N. (Aralık 1995). "Cooperative activation of muscle gene expression by MEF2 and myogenic bHLH proteins". Cell. 83 (7): 1125-1136. doi:10.1016/0092-8674(95)90139-6. ISSN 0092-8674.
- ^ Wang, Da-Zhi; Valdez, M. Renee; McAnally, John; Richardson, James; Olson, Eric N. (15 Kasım 2001). "The Mef2c gene is a direct transcriptional target of myogenic bHLH and MEF2 proteins during skeletal muscle development". Development. 128 (22): 4623-4633. doi:10.1242/dev.128.22.4623. ISSN 1477-9129.
- ^ a b Verzi, Michael P.; Agarwal, Pooja; Brown, Courtney; McCulley, David J.; Schwarz, John J.; Black, Brian L. (Nisan 2007). "The Transcription Factor MEF2C Is Required for Craniofacial Development". Developmental Cell. 12 (4): 645-652. doi:10.1016/j.devcel.2007.03.007. ISSN 1534-5807.
- ^ a b Miller, Craig T.; Swartz, Mary E.; Khuu, Patricia A.; Walker, Macie B.; Eberhart, Johann K.; Kimmel, Charles B. (Ağustos 2007). "mef2ca is required in cranial neural crest to effect Endothelin1 signaling in zebrafish". Developmental Biology. 308 (1): 144-157. doi:10.1016/j.ydbio.2007.05.018. ISSN 0012-1606.
- ^ Zhang, Chun Li; McKinsey, Timothy A.; Chang, Shurong; Antos, Christopher L.; Hill, Joseph A.; Olson, Eric N. (Ağustos 2002). "Class II Histone Deacetylases Act as Signal-Responsive Repressors of Cardiac Hypertrophy". Cell. 110 (4): 479-488. doi:10.1016/s0092-8674(02)00861-9. ISSN 0092-8674. 26 Temmuz 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Mart 2022.
- ^ Potthoff, Matthew J.; Wu, Hai; Arnold, Michael A.; Shelton, John M.; Backs, Johannes; McAnally, John; Richardson, James A.; Bassel-Duby, Rhonda; Olson, Eric N. (4 Eylül 2007). "Histone deacetylase degradation andMEF2 activation promote the formation of slow-twitch myofibers". Journal of Clinical Investigation. 117 (9): 2459-2467. doi:10.1172/jci31960. ISSN 0021-9738.
- ^ a b Anderson, Courtney M.; Hu, Jianxin; Thomas, Reuben; Gainous, T. Blair; Celona, Barbara; Sinha, Tanvi; Dickel, Diane E.; Heidt, Analeah B.; Xu, Shan-Mei; Bruneau, Benoit G.; Pollard, Katherine S. (1 Nisan 2017). "Cooperative activation of cardiac transcription through myocardin bridging of paired MEF2 sites". Development. 144 (7): 1235-1241. doi:10.1242/dev.138487. ISSN 1477-9129.
- ^ a b Barnes, Ralston M.; Harris, Ian S.; Jaehnig, Eric J.; Sauls, Kimberly; Sinha, Tanvi; Rojas, Anabel; Schachterle, William; McCulley, David J.; Norris, Russell A.; Black, Brian L. (1 Ocak 2016). "MEF2C regulates outflow tract alignment and transcriptional control of Tdgf1". Development. doi:10.1242/dev.126383. ISSN 1477-9129.
- ^ Verzi, Michael P.; McCulley, David J.; De Val, Sarah; Dodou, Evdokia; Black, Brian L. (Kasım 2005). "The right ventricle, outflow tract, and ventricular septum comprise a restricted expression domain within the secondary/anterior heart field". Developmental Biology. 287 (1): 134-145. doi:10.1016/j.ydbio.2005.08.041. ISSN 0012-1606.
- ^ Sacilotto, Natalia; Chouliaras, Kira M.; Nikitenko, Leonid L.; Lu, Yao Wei; Fritzsche, Martin; Wallace, Marsha D.; Nornes, Svanhild; García-Moreno, Fernando; Payne, Sophie; Bridges, Esther; Liu, Ke (15 Ekim 2016). "MEF2 transcription factors are key regulators of sprouting angiogenesis". Genes & Development. 30 (20): 2297-2309. doi:10.1101/gad.290619.116. ISSN 0890-9369.
Dış bağlantılar
- Tüm Ökaryotlarda OrthoDB Ortoloji
- MEF2 + protein, + C + elegans ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH)
- Mef2 + protein, + Drosophila, ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH)
- Mef2 + protein, + ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH) zebra balığı
- SMP1 + protein, + Arabidopsis ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH)
- ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH) SMP1 + protein, + S + cerevisiae