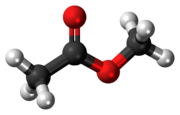
Metil asetat
 | |
 | |
| Adlandırmalar | |
|---|---|
Metil asetat | |
Sistematik IUPAC adı Metil etanoat | |
Diğer adlar Asetik asitin metil esteri | |
| Tanımlayıcılar | |
CAS numarası | |
3D model (JSmol) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.001.078 |
| KEGG | |
PubChem CID | |
| UNII | |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Kimyasal formül | C3H6O2 |
| Molekül kütlesi | 74,08 g mol−1 |
| Görünüm | Renksiz sıvı |
| Koku | Meyvemsi, hoş kokulu[2] |
| Yoğunluk | 0,932 gr/cm³ |
| Erime noktası | -98 °C (-144 °F; 175 K) |
| Kaynama noktası | 569 °C (1.056 °F; 842 K) |
| Çözünürlük (su içinde) | %~25 (20 °C) |
| Buhar basıncı | 173 mmHg (20°C)[2] |
| -42,60·10−6 cm3/mol | |
| Kırınım dizimi (nD) | 1,361 |
| Tehlikeler | |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | 14 °C (57 °F; 287 K) |
| Patlama sınırları | %3,1-%16[2] |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 3700 mg/kg (oral, tavşan)[3] |
LCLo (yayınlanan en düşük) | 11.039 ppm (fare, 4 saat) 21.753 ppm (kedi, 1 saat) 32.000 ppm (sıçan, 4 saat)[3] |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 200 ppm (610 mg/m³)[2] |
| REL (tavsiye edilen) | TWA 200 ppm (610 mg/m³) ST 250 ppm (760 mg/m³)[2] |
| IDLH (anında tehlike) | 3100 ppm[2] |
| Güvenlik bilgi formu (SDS) | External MSDS |
| Benzeyen bileşikler | |
Benzeyen | Metil format Etil asetat |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
MeOAc, asetik asit metil esteri ya da metil etanoat olarak da bilinen Metil asetat, formülü CH3COOCH3 olan karboksilli bir esterdir. Karakteristik olarak, bazı tutkallar ve oje çıkarıcıların hoş kokusunu anımsatan yanıcı bir sıvıdır. Metil asetat, zayıf polar ve lipofilik özellikte olduğundan bazen bir solvent olarak kullanılmaktadır. Ancak yakın akrabası olan etil asetat daha az toksik ve suda daha az çözündüğünden dolayı çok daha yaygın kullanılan bir çözücüdür. Metil asetat, oda sıcaklığındaki su içerisinde %25 kadar bir çözünürlüğe sahiptir. Yüksek sıcaklıktaki suda, çözünürlüğü çok daha yüksektir. Metil asetat kuvvetli sulu bazlar ya da sulu asitlerin mevcudiyetinde kararlı değildir.[4]
Üretimi ve reaksiyonları
Metil asetat, asetik asit üretiminin bir yan ürünü olarak metanolü karbonilleme yoluyla endüstriyel olarak üretilir.[5] Metil asetat aynı zamanda, sülfürik asit gibi kuvvetli asitlerin mevcudiyetinde metanol ile asetik asitin esterleşmesi yoluyla da oluşur. Eastman Kodak'ın reaktif damıtma kullanarak hızlandırdığı bu üretim prosesi oldukça ünlüdür.
Reaksiyonları
Sodyum hidroksit gibi kuvvetli bazlar ya da hidroklorik asit veya sülfürik asit gibi kuvvetli asitlerin mevcudiyetinde, özellikle yüksek sıcaklıkta hidrolize olarak ilk haldeki metanol ve asetik asite dönüşür. Metil asetatı bir asit yardımıyla geri bileşenlerine dönüştürme ester ile ilgili olarak birinci dereceden bir reaksiyondur. Metil asetat ve örneğin sodyum hidroksit gibi bir bazın reaksiyonu, her iki reaksiyon maddesi ile ilgili olarak ikinci derece bir reaksiyondur.
Kullanımı
Metil asetat düşük toksiteli uçucu solvent olduğu için başlıca olarak tutkallar, boyalar ve oje çıkarıcılarda kullanılır.
Asetik anhidrit, Monsanto asetik asit sentezinden esinlenerek uygulanan bir proseste metil asetatı karbonilleme yoluyla üretilir.[6]
Ayrıca bakınız
- Metil format
- Etil asetat
- Propil asetat
- Bütil asetat
Yararlanılan kaynaklar
- ^ Merck Index, 12th Edition, 6089.
- ^ a b c d e f NIOSH Pocket Guide to Chemical Hazards. "#0391". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b "Methyl acetate". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Sağlığı ve Güvenliği Enstitüsü (NIOSH).
- ^ Zeno, W. Wicks, JR, Frank N. Jones, S. Peter Pappas, and Douglas A. Wicks (2007). Organic Coatings. Hoboken, New Jersey: Wiley. ISBN 978-0-471-69806-7.
- ^ Hosea Cheung, Robin S. Tanke, G. Paul Torrence “Acetic Acid” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a01_045
- ^ Zoeller, J. R.; Agreda, V. H.; Cook, S. L.; Lafferty, N. L.; Polichnowski, S. W.; Pond, D. M. (1992). "Eastman Chemical Company Acetic Anhydride Process". Catalysis Today. Cilt 13. ss. 73-91. doi:10.1016/0920-5861(92)80188-S.