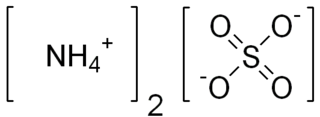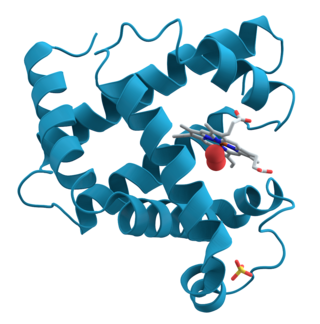
Proteinler, bir veya daha fazla uzun amino asit artık zincirini içeren büyük biyomoleküller ve makromolekül'lerdir. Proteinler organizmalar içinde, hücrelere yapı ve organizmalar sağlayarak ve molekülleri bir konumdan diğerine taşıyarak metabolik reaksiyonları katalizleme, DNA kopyalama, uyaranlara yanıt verme dahil olmak üzere çok çeşitli işlevler gerçekleştirir. Proteinler, genlerinin nükleotit dizisi tarafından dikte edilen ve genellikle faaliyetini belirleyen özel 3D yapıya protein katlanmasıyla sonuçlanan amino asit dizilimlerinde birbirlerinden farklıdır.

Kan, atardamar, toplardamar ve kılcal damarlardan oluşan damar ağının içinde dolaşan; akıcı plazma ve hücrelerden meydana gelmiş kırmızı renkli hayati sıvıdır.

Piridoksin, bir diğer adıyla B6 vitamini, özellikle protein metabolizmasında çok önemli bir koenzimdir ve birçok nörotransmitterin sentezinde rol alır. Besinler Piridoksamin ve Piridoksal şeklinde de bulunabilir. Aktif şekli Piridoksalfosfat'tır (PLF). Kolaylıkla bozulur, bu yüzden güneş ışığından, bazik ortamlardan uzak tutulmalıdır. İşlenme ve pişirme sırasında da kolaylıkla bozulur.

Amino asitler, proteinleri oluşturan temel yapı taşlarıdır.

Ribozom, tüm canlı hücrelerde bulunan karmaşık moleküler yapıya sahip ve protein oluşturma sürecinde hayati bir rol oynayan bir organeldir. Bu süreç, mRNA çevirisi olarak bilinen bir biyolojik mekanizma aracılığıyla gerçekleşir. Kısaca ribozomlar, haberci RNA (mRNA) molekülleri tarafından sağlanan talimatları takip ederek amino asitleri birbirine bağlar ve polipeptit adı verilen amino asit zincirlerini oluşturur.

Protein biyosentezi, hücrenin protein sentezlenmesi için gereken bir biyokimyasal süreçtir. Bu terim bazen sadece protein translasyonu anlamında kullanılsa da transkripsiyon ile başlayıp translasyonla biten çok aşamalı bir süreçtir. Prokaryotlarda ve ökaryotlarda ribozom yapısı ve yardımcı proteinler bakımından farklılık göstermesine karşın, temel mekanizma korunmuştur.

Pantotenik asit (vitamin B5), hem hayvansal hem de bitkisel kaynaklarda bulunabildiğinden dolayı Grekçede "her yerden" anlamına gelen "πάντοθεν" sözcüğünden kökenini almıştır. Vücutta depolanamayan ve suda eriyen bir vitamindir. Karbonhidrat, yağ ve protein metabolizması için gereklidir. Bu vitamin, insan bağırsak florası tarafından sentez edildiği için eksikliğine pek sık rastlanmaz. Ancak eksikliğinde deride yaralar, saç dökülmesi, sinir sistemi bozuklukları gibi belirtiler görülebilir. Savaş esirlerinde gözlenen Burning Foot sendromu, pantotenik asit eksikliğine bağlanmıştır.

Üre (Latince Urea Pura), organik bir bileşik. Formülü H2N-CO-NH2'dir. Karbonik asidin diamidi olan üre aynı zamanda karbamik asidin de amidi olduğundan karbamid adı ile de bilinir.

Max Ferdinand Perutz, Avusturyalı-Büyük Britanyalı moleküler biyolog. John Kendrew'la birlikte 1962'nin Nobel Kimya Ödülü'nün sahibi olmuştur.

Organik bileşikler, molekülleri karbon içeren kalabalık kimyasal bileşikler sınıfındandır. Aşağıda sunulan tarihsel nedenlerden dolayı, bu bileşiklerin küçük bir kısmı, örneğin karbonatlar, basit karbon oksitleri ve siyanürlerin yanı sıra, karbon allotropları inorganik kabul edilir. "Organik" ve "inorganik" karbon bileşikleri arasındaki ayrım "kimyanın geniş alanını düzenlemek için yararlı olsa da, çoğunlukla rastgeledir".

Glisin (kısaltılmışı Gly ya da G) formülü NH2CH2COOH olan apolar bir aminoasittir. Glisin kodonları GGU, GGC, GGA, GGG cf. genetik koddur. Yapısal olarak proteinlerde bulunan 20 aminoasit arasında en basit olanıdır. Yan zinciri sadece bir hidrojen atomundan ibarettir. Glisindeki α-karbon atomu da bir hidrojene bağlı olduğu için, glisin optik olarak aktif değildir, diğer bir deyişle optik izomeri bulunmamaktadır.

Peroksizom, hemen hemen tüm ökaryotik hücrelerde bulunan bir organeldir. Çok uzun zincirli yağ asitlerinin, dallı zincirli yağ asitlerinin, D amino asitlerinin, poliaminlerin katabolizmasında ve memelilerin beyin ve akciğerlerinin normal fonksiyonu için önem taşıyan bir eterfosfolipid olan plazmalojenlerin biyosentezi için gereklidir. Ayrıca enerji metabolizması için önemli olan pentoz fosfat yolundaki iki enzimin toplam aktivitesinin yaklaşık olarak %10'unu içerir. Peroksizomların, hayvanlardaki izoprenoid veya kolesterol senteziyle ilişkili olup olmadığı tartışılmaktadır. Filizlenen tohumlardaki glioksilat döngüsü ("glioksizom"), yapraklardaki fotosolunum, tripanazomatidlerdeki glikoliz ("glikozom") ve bazı mayalardaki metanol veya amin oksidasyonu ile asimilasyonu bilinen diğer peroksizomal işlevlerdir.
Yağ asitleri birçok organizma için önemli enerji kaynaklarıdır.Artmış glukoz sıklıkla yağ asidine çevrilerek depo edilmektedir. Trigliserdiler aynı miktardaki karbonhidrat ve proteinlerden yaklaşık 2 kat daha fazla enerji vermektedirler. Tüm hücre zarları iki tabakalı fosfolipitlerden oluşur. Yağ asitleri aynı zamanda protein modifikasyonunda da kullanılırlar. Bu nedenle yağ asidi metabolizması, yağ asitlerinin primer metabolitlerinin ve enerjinin oluştuğu katabolizmalarını ve biyolojik olarak oldukça önemli bileşiklerin sentez edildiği anabolizmalarını kapsar.
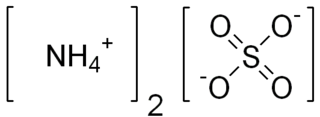
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.
Proteinler her organizmada bulunan önemli bir makromolekül sınıfıdır. Proteinler, 20 farklı tip L-α-amino asitten meydana gelen polimerlerdir. Amino asitler birbiriyle reaksiyona girdikten sonra meydana gelen polimerde bu amino asitlerden arta kalan birimlere amino asit kalıntısı denir. 40 kalıntıdan daha kısa olan zincirler için protein yerine genelde peptit terimi kullanılır. Biyolojik fonksiyonlarını yerine getirebilmek için proteinler uzay içinde belli bir biçim alacak şekilde katlanırlar. Bu katlanmayı yönlendiren güçler, protein atomları arasındaki hidrojen bağı, iyonik etkileşimler, van der Waals kuvvetleri ve hidrofobik istiflenme gibi, kovalent olmayan etkleşimlerdir. Proteinlerin işlevlerini moleküler düzeyde anlayabilmek için genelde onları üç boyutlu yapısının çözülmesi gerekir. Protein yapısını çözmek için X-ışını kristalografisi ve NMR spektroskopisi kullanılır, bunlar yapısal biyolojinin başlıca yöntemleri arasında yer alır.
Moleküler saat, moleküler saat hipotezi (MSH) temelinde, jeolojik geçmişte iki türün veya diğer taksonların birbirinden ne zaman ayrıldıklarını tespit etmek için fosil sabitleri ve moleküler değişim oranlarının moleküler evrimde kullanıldığı bir tekniktir. Moleküler saat, türleşme ya da radyasyon olarak adlandırılan olayların ortaya çıkma zamanlarını tahmin etmek için kullanılır. Bu tür hesaplamalar için kullanılan moleküler veriler, DNA'larda genellikle nükleotid dizileri veya proteinlerdeki amino asit dizileridir. Moleküler saate, bazen gen saati, genetik saat ya da evrimsel saat dendiği de olur.
Adolph Strecker tarafından bulunan Strecker amino asit sentezi bir aldehit dan bir dizi kimyasal reaksiyonla bir amino asit sentezlenmesidir. Aldehit potasyum siyanür eşliğinde amonyum klorür ile bir α-aminonitril oluşturacak şekilde reaksiyona sokulur. Daha sonra bu α-aminonitril hidrolize edilerek istenilen amino asit elde edilir. Orijinal Strecker reaksiyonunda asetaldehit, amonyak ve hidrojen siyanür ün verdiği reaksiyon ürünü, hidrolizlenerek alanin elde edilmiştir.
Moleküler evrim, nesiller boyu aktarılacak şekilde, DNA, RNA ve protein gibi hücresel moleküllerin diziliminin değiştirilmesi işlemidir ya da bununla ilgilenen bilim dalıdır. Moleküler evrimin alanı, bu değişimlerdeki kalıpları açıklamak için evrimsel biyoloji ve popülasyon genetiği ilkelerini kullanır. Moleküler evrim başlıca, nükleotid değişimlerinin oranları ve etkilerini, nötr evrimi, doğal seçilimi, yeni genlerin kökenlerini, karmaşık özelliklerin genetik yapısını, türleşmenin genetik temelini, gelişim evrimini ve evrimin genomik ve fenotipik değişikliklere neden olan etkilerini inceler.
Siklobüten bir sikloalkendir. Pratik uygulamalar için değil, temel bir değer olarak ilgi çekicidir. Renksiz, kolay yoğunlaşan bir gazdır. Modern bir sentezi, siklobütanolün 2 aşamalı dehidrasyonunu ile gerçekleşir. Bileşik ilk önce [C4H7NMe3]OH, amonyum tuzunun termolizi ile hazırlanmıştır.
Biyosentez, substratların canlı organizmalarda daha karmaşık ürünlere dönüştürüldüğü çok aşamalı, enzim katalizli bir süreçtir. Biyosentezde basit bileşikler modifiye edilir, diğer bileşiklere dönüştürülür veya makromoleküller oluşturmak üzere birleştirilir. Bu süreç genellikle metabolik yollardan oluşur. Bu biyosentetik yollardan bazıları tek bir hücresel organel içinde yer alırken diğerleri birden fazla hücresel organel içinde yer alan enzimleri içerir. Bu biyosentetik yolların örnekleri arasında çift katlı lipit katmanının bileşenlerinin ve nükleotidlerin üretimi yer alır. Biyosentez genellikle anabolizma ile eş anlamlıdır ve bazı durumlarda birbirinin yerine kullanılır.