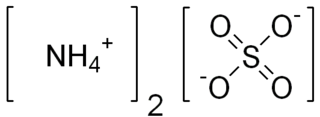Gübre, bitkinin beslenmesinde gerekli olan kimyasal elementleri sağlamak için toprağa ilave edilen herhangi bir madde.

Tuz, kimyada, bir asitle bir bazın tepkimeye girmesi neticesinde meydana gelen maddedir. Tuz, asitteki eksi yüklü iyonla (anyon) bazdaki artı yüklü iyondan (katyon) meydana gelir. Asitle baz arasındaki nötralleşme tepkimesi esnasında tuz ve su açığa çıkar. Erimiş tuz veya çözelti halindeki tuzların çoğu eksi ile artı yüklü iyonlarına ayrışır ve elektriği iletir. Tuz adı ayrıca sofra tuzu veya sodyum klorür (NaCl) için de kullanılır.

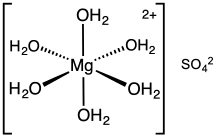
Magnezyum (Mg), gümüş beyazlığında bir metaldir ve genellikle alaşım maddesi olarak, yani başka metallerle karıştırılarak kullanılır. Kimyasal simgesi Mg, atom numarası 12; atom ağırlığı 24,312 olan bu element en hafif metallerden biridir ve bu özelliğiyle önem kazanmıştır. Toz halindeki magnezyum kolayca tutuşur ve parlak bir alevle yanar. Bu özelliği nedeniyle, elektrikli fotoğraf makinesi flaşları çıkmadan önce, magnezyum yakılarak flaşlı fotoğraflar çekilmiştir.

Alçı taşı, kalsiyum sülfat dihidrattan oluşan yumuşak bir sülfat mineralidir ve kimyasal formül CaSO4 · 2H2O'dur. Alçıtaşı ayrıca selenitin yarı saydam kristalleri olarak kristalleşir. Aynı zamanda bir evaporit minerali ve anhidritin hidrasyon ürünü olarak oluşur. İçinde su bulunan kalsiyum sülfat minerali, tek veya ikiz sütunlar hâlinde billûrlanır. Alçı billurlarına kil ve marn içinde veya tuzlu ve alçılı dağların boşluklarında rastlanır.

Anhidrit, susuz kalsiyum sülfat (CaSO4) yapısında, kayaç oluşturan önemli bir mineral. Kimyasal açıdan jips (alçıtaşı) ile arasındaki tek fark, kristalleşme suyunun olmamasıdır, nitekim nemli ortamlarda molekülüne su alarak jipse dönüşür. Anhidrit genellikle tuz birikintilerinde kayatuzu ve jipsle bir arada bulunur.

Küprik sülfat ya da sadece bakır sülfat olarak da bilinen Bakır (II) sülfat, kimyasal formülü CuSO4 olan bir kimyasal bileşiktir. Bu tuzun hidrasyon derecelerine bağlı olarak bir dizi farklı bileşikleri mevcuttur. Susuz formu soluk yeşil ya da grimsi beyaz bir toz olmasına karşın en çok bilinen pentahidrat (CuSO4•5H2O) formu, parlak mavi renktedir. Çok az miktardaki CuSO4•5H2O çevreye çok zehirlidir, gözleri ve cildi tahriş eder ve yutulduğunda zararlı da olabilir. Oktahedral moleküler geometriye ve paramanyetik özelliğe sahip olan bakır (II) sülfat ekzotermik olarak suda çözünürek [Cu(H2O)6]2+ kompleksini oluşturur. Bakır (II) sülfat "mavi vitriyol", "göztaşı" ve "göktaşı" olarak da bilinmektedir.
Fatma Elif Genceli Güner, Türk kimya mühendisi ve akademisyen. İstanbul Teknik Üniversitesi (İTÜ) kimya mühendisliği bölümü mezunudur. Hollanda'da Delft Teknik Üniversitesi'nde doktora yapmıştır. Günümüzde İstanbul Teknik Üniversitesi'nde doçent doktor olarak görev almaktadır. Meridianit ve ernstburkeite minerallerinin keşfiyle tanınmaktadır.
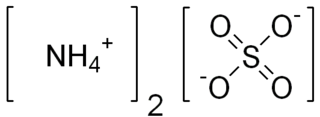
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.

Potasyum sülfat, formülü K2SO4 olan, yanmaz, suda çözünebilen beyaz kristal yapıda bir potasyum tuzudur. Genellikle potasyum ve kükürt kaynağı olarak gübrelerde kullanılır.

Evaporit, sulu bir çözeltinin buharlaşmasıyla kristalleşme ve yoğunlaşma sürecinde sonuçlanır. Evaporit suda çözünen mineral sedimentin (mineralin) ismidir. İki çeşit tuz taşı birikintisi vardır:
- Okyanus birikintisi olarak da bilinen marine ve göller gibi suyun ana bloklarında bulunmaktadır.
- Evaporit tuz taşları çökelti kayaları olarak bulunur.
Lewis asiti Lewis bazıyla Lewis eklenme ürününü oluşturmak için etkileşen kimyasal türdür. Lewis bazı, Lewis eklenme ürününü oluşturmak için, Lewis asidine elektron çifti veren türdür. Örneğin, OH− ve NH3 Lewis bazlarıdır çünkü bu iyonlar bağ yapmamamış elektron çiftlerini verebilirler. Eklenme ürününde, Lewis asidi ve bazı Lewis bazından gelen elektron çiftini paylaşır. Lewis asit ve bazının isim babası Gilbert N. Lewis'dir.

Magnezyum sitrat sitrik asidin 1:1 oranında karıştırılmasıyla oluşturulan tuz formunda bir magnezyum karışımdır. "Magnezyum sitrat" adı bazen başka tuzlar için de kullanılabilir, örneğin magnezyum sitrat oranı 3:2 olan trimagnesium sitrat.

Magnezyum nitrat Mg(NO3)2(H2O)x formülüne sahip inorganik bileşikleri ifade eder. Formüldeki, x = 6, 2 ve 0 olabilir. Hepsi beyaz renkli katılardır. Susuz madde higroskopiktir, havada bekletildiğinde hızlı bir şekilde hekzahidrat oluşturur. Bütün tuzları hem suda hem de etanolde çok çözünür.

Frijoles negros, Guatemala, Küba, Venezuela, Porto Riko, Meksika ve Latin Amerika'daki diğer ülkelerde hazırlanan siyah fasulye ile yapılan bir Latin Amerika yemeğidir. Phaseolus vulgaris türünden bir baklagil olan siyah fasulye, genellikle konserve veya kurutulmuş olarak satılır. Bir bardak kuru siyah fasulye, yaklaşık 2 buçuk bardak pişmiş fasulye verir. Siyah fasulye çorbası, yaygın olarak hazırlanan bir başka Küba yemeğidir.
Tuz muadilleri, yüksek kan basıncı ve yüksek sodyum klorür alımıyla kardiyovasküler hastalık riskini ortadan kaldırmak için pazarlanan düşük sodyumlu sofra tuzunun muadilleri, alternatifleridir.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.
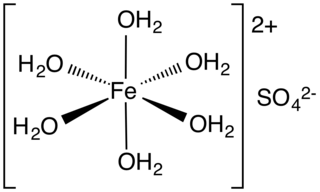
Demir (II) sülfat veya demir sülfat FeSO4•xH2O formülüne sahip bir dizi tuz anlamına gelir. Bu bileşikler en yaygın olarak heptahidrat (x = 7) olarak bulunursa da x için birkaç değer bilinmektedir. Hidratlı form tıp alanında demir eksikliğini tedavi etmek ve ayrıca endüstriyel uygulamalar için kullanılır. Antik çağlardan beri, Zaç-ı Kıbrıs ve yeşil vitriyol (vitriyol, sülfat için eski bir isimdir) olarak bilinen, mavi-yeşil heptahidrat (7 molekül su içeren hidrat) bu maddenin en yaygın şeklidir. Tüm demir (II) sülfatlar suda çözünerek oktahedral moleküler geometriye sahip ve paramanyetik olan aynı akua kompleksi [Fe(H2O)6]2+ verir.

Magnezyum klorür, MgCl
2 formülüne sahip kimyasal bileşiğin adıdır. Susuz şekline ek olarak, MgCl
2 çeşitli hidratlar MgCl
2·nH
2O şeklinde olur. Bu tuzlar, suda oldukça çözünür olan tipik iyonik halojenürlerdir. Magnezyum klorür tuzlu su veya deniz suyundan ekstrakte edilebilir. Kuzey Amerikada, magnezyum klorür esas olarak Büyük Tuz Gölü tuzlu suyundan üretilir. Ürdün Vadisi'ndeki Lut Gölü'nden benzer bir işlemle çıkarılır. Mineral bişofit olarak magnezyum klorür de eski deniz yataklarından, örneğin kuzeybatı Avrupa'daki Zechstein deniz yatağından çıkarılır. Bu, ilk okyanustaki yüksek magnezyum klorür içeriği ile açıklanabilir. Bazı magnezyum klorür deniz suyunun buharlaşmasından yapılır. Susuz magnezyum klorür, büyük ölçekte üretilen magnezyum metalinin başlıca öncüsüdür. Hidratlı magnezyum klorür en kolay bulunabilen formdur.

Kobalt(II) sülfat; CoSO4(H2O)x formülüne sahip inorganik bileşiklerden herhangi birine verilen isimdir. Genellikle sırasıyla kobalt sülfat, heksa- veya heptahidratları (CoSO4.6H2O or CoSO4.7H2O) tanımlar. Heptahidrat, suda ve metanolde çözünen kırmızı bir katıdır. Kobalt(II) tek sayıda elektrona sahip olduğu için tuzları paramanyetiktir.

Magnezyum biyolojik sistemlerde temel elementtir. Magnezyum genellikle Mg2+ iyonu olarak oluşur. Yaşam için gerekli mineral besin maddesidir ve her organizmada her hücre türünde vardır. Örneğin, hücrelerdeki ana enerji kaynağı olan adenozin trifosfat (ATP), biyolojik olarak aktif olabilmesi için magnezyum iyonuna bağlanmalıdır. ATP genellikle Mg-ATP'dir. Bu haliyle magnezyum, DNA ve RNA sentezi ile ilişkili olanlar da dahil olmak üzere hücrelerdeki tüm polifosfat bileşiklerinin kararlılığında rol oynar.