Lityum
 Yağ içinde yüzmekte olan lityum | ||||||||||||||||
| Görünüş | gümüşsü beyaz | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Standart atom ağırlığı Ar, std(Li) | [6,938, 6,997] geleneksel: 6,94 | |||||||||||||||
| Periyodik tablodaki yeri | ||||||||||||||||
| ||||||||||||||||
| Atom numarası (Z) | 3 | |||||||||||||||
| Grup | 1. grup: H ve alkali metaller | |||||||||||||||
| Periyot | 2. periyot | |||||||||||||||
| Blok | s bloku | |||||||||||||||
| Elektron dizilimi | [He] 2s1 | |||||||||||||||
| Kabuk başına elektron | 2, 1 | |||||||||||||||
| Fiziksel özellikler | ||||||||||||||||
| Faz (SSB'de) | Katı | |||||||||||||||
| Erime noktası | 453,65 K (180,50 °C, 356,90 °F) | |||||||||||||||
| Kaynama noktası | 1603 K (1330 °C; 2426 °F) | |||||||||||||||
| Yoğunluk (OS) | 0,534 g/cm3 | |||||||||||||||
| sıvıyken (en'de) | 0,512 g/cm3 | |||||||||||||||
| Kritik nokta | 3220 K, 67 MPa (ekstrapolasyon ile elde edilmiştir) | |||||||||||||||
| Erime entalpisi | 3,00 kJ/mol | |||||||||||||||
| Buharlaşma entalpisi | 136 kJ/mol | |||||||||||||||
| Molar ısı kapasitesi | 24,860 J/(mol·K) | |||||||||||||||
Buhar basıncı
| ||||||||||||||||
| Atom özellikleri | ||||||||||||||||
| Yükseltgenme durumları | +1 | |||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 0,98 | |||||||||||||||
| İyonlaşma enerjileri |
| |||||||||||||||
| Atom yarıçapı | Deneysel: 152 pm | |||||||||||||||
| Kovalent yarıçapı | 128±7 pm | |||||||||||||||
| Van der Waals yarıçapı | 182 pm | |||||||||||||||
| Diğer özellikleri | ||||||||||||||||
| Kristal yapı | Hacim merkezli kübik (hmk) | |||||||||||||||
| Ses hızı çubukta | 6000 m/s (20 °C'de) | |||||||||||||||
| Genleşme | 46 µm/(m·K) (25 °C'de) | |||||||||||||||
| Isı iletkenliği | 84,8 W/(m·K) | |||||||||||||||
| Elektrik direnci | 92,8 Ω·m | |||||||||||||||
| Manyetik düzen | paramanyetik | |||||||||||||||
| Manyetik alınganlık | +14,2×10-6 cm3/mol (298 K)[1] | |||||||||||||||
| Young modülü | 4,9 GPa | |||||||||||||||
| Kayma modülü | 4,2 GPa | |||||||||||||||
| Hacim modülü | 11 GPa | |||||||||||||||
| Mohs sertliği | 0,6 | |||||||||||||||
| Brinell sertliği | 5 MPa | |||||||||||||||
| CAS Numarası | 7439-93-2 | |||||||||||||||
| Tarihi | ||||||||||||||||
| Keşif | Johan August Arfwedson (1817) | |||||||||||||||
| İlk izolasyon | William Thomas Brande (1821) | |||||||||||||||
| Ana izotopları | ||||||||||||||||
| ||||||||||||||||
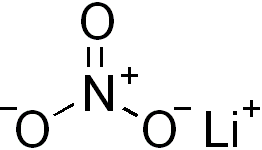
Lityum, sembolü Li atom numarası 3 olan kimyasal elementtir. Periyodik tabloda 1. grupta alkali metal olarak bulunur ve yoğunluğu en düşük olan metaldir. Lityum, yüksek reaktifliğinden dolayı doğada saf hâlde bulunmaz. Yumuşak ve gümüşümsü beyaz metaldir. Havada bulunan oksijenle reaksiyona giren lityum, lityum oksit (Li2O) oluşturur. Bu oksitlenme reaksiyonunu engellemek için yağ içinde saklanır. Hava ve su tarafından hızlı bir şekilde oksitlenip kararır ve lekelenir. Lityum metali doldurulabilir pillerde (örnek olarak cep telefonu ve kamera pili) ve ağırlığa yüksek direniş göstermesi sebebiyle alaşım olarak hava taşıtlarında kullanılır. Li+ iyonunun nörolojik etkilerinden dolayı, lityumlu bileşikler farmakolojik olarak özellikle bipolar duygudurum bozukluğunun tedavisinde duygudurum düzenleyici olarak kullanılır.

Genel özellikleri
Birinci grup elementi olmasına rağmen, lityum aynı zamanda 2. grubun toprak alkali özelliklerini de gösterir. Bütün alkali metaller gibi bir tane değerlik elektronu bulunur ve bu elektronu hemen kaybederek pozitif iyon haline geçer. Bu sebeplerden dolayı lityum su ile çok kısa sürede reaksiyona girer ve doğada doğal halinde bulunmaz. Ancak kendisiyle benzer kimyasal özellikler taşıyan sodyum elementi lityuma göre daha aktiftir ve daha çok insanların midelerinde yer alır
Lityum bıçakla kesilebilir ancak sodyumdan biraz daha sert olduğu için onu kesmek veya bölmek çok daha zordur. Reaksiyona girmemiş Lityum gümüşi bir renge sahiptir, ancak kısa sürede rengi kararır. Düşük yoğunluğu sayesinde hidrokarbonlar üzerinde batmadan durabilir.
Alev üzerine konulduğunda lityumda göz alıcı bir kırmızı renk gözlenir, ancak yanmaya başladığında parlak beyaz bir alev gözlemlenir. Lityum suda ve su buharında bulunan oksijen ile tutuşur ve yanma reaksiyonu gösterir. Oda sıcaklığında azot ile reaksiyona giren tek metaldir. Yüksek özgül ısısı, 3582 J/(kg·K) ve sıvı haldeki geniş sıcaklık değerleri lityumu kullanışlı hale getirmektedir.
Lityum hava ve su ile yanması ve potansiyel patlama tehlikesine rağmen diğer alkali metallere göre daha az tehlikelidir. Oda sıcaklığındaki Lityum-Su reaksiyonu aktif ve çabuk gerçekleşen bir reaksiyon olmasına rağmen çok tehlikeli bir reaksiyon değildir. Lityum alevlerini söndürmek zordur ve bunun için özel kimyasallardan oluşan söndürücüler kullanılır.
Lityum, ten ile temasını engellemek için özel koruma gerektirir. Lityumu toz olarak ya da alkalinli bileşimlerinin solunması, burun yollarında ve boğaz da tahriş ve zarara neden olur.
Tarihçe

Petalit (LiAlSi4O10) 1800 yılında Brezilyalı kimyager ve devlet adamı José Bonifácio de Andrada e Silva tarafından İsveç'teki Utö adasındaki bir madende keşfedildi.[2][3][4][5] Ancak 1817 yılına kadar Johan August Arfwedson, o zamanlar kimyager Jöns Jakob Berzelius'un laboratuvarında çalışırken, Petalit cevherini analizinde yeni bir elementin varlığını tespit etti.[6][7][8][9]
Karbonat ve hidroksit daha az suda çözünür ve daha az alkali olmasına rağmen bu element, sodyum ve potasyum'a benzer bileşikler oluşturdu.[10] Bitki küllerinde keşfedilen potasyum ve kısmen hayvan kanındaki bolluğuyla bilinen sodyumun aksine keşfini katı bir mineralde yansıtmak için Berzelius, alkali malzemeye Yunanca λιθoς ("taş" anlamına gelen lithos olarak çevrilmiştir) kelimesinden "lithion/lithina" adını verdi.[4][9][11]
Arfwedson daha sonra aynı elementin spodumen ve Lepidolit minerallerinde bulunduğunu gösterdi.[4][12] 1818'de Christian Gmelin, lityum tuzlarının aleve parlak kırmızı bir renk verdiğini ilk gözlemleyen kişiydi.[4][13] Bununla birlikte, hem Arfwedson hem de Gmelin, saf elementi tuzlarından ayırmaya çalıştılar ve başaramadılar.[4][9][14] Daha önce kimyager Sir Humphry Davy tarafından alkali metaller potasyum ve sodyumu izole etmede kullandığı elektroliz süreciyle, lityum oksit William Thomas Brande'nin elde ettiği 1821 yılına kadar izole edilmemişti.[14][15][16][17][18] Brande ayrıca klorür gibi bazı saf lityum tuzlarını tanımladı ve lithia'nın (lityum oksit) yaklaşık %55 metal içerdiğini tahmin ederek, lityumun atom ağırlığının yaklaşık 9,8 g/mol (modern değer ~6.94 g/mol) olduğunu tahmin etti.[19] 1855'te, Robert Bunsen ve Augustus Matthiessen tarafından lityum klorürün elektrolizi yoluyla daha büyük miktarlarda lityum üretildi.[4][20] Bu yöntemin bulunması 1923'te sıvı lityum klorür ve potasyum klorür karışımının elektrolizini yapan Alman Metallgesellschaft AG şirketi tarafından ticari lityum üretimine yol açtı.[4][21][22]
Avustralyalı psikiyatr John Cade, 1949'da mani tedavisinde lityum kullanımını yeniden tanıtması ve yaygınlaştırmasıyla tanınır.[23] Kısa bir süre sonra, 20. yüzyılın ortaları boyunca, lityumun mani ve depresyon Avrupa ve Amerika Birleşik Devletleri'nde yükselişe geçti.
Lityum üretimi ve kullanımı, tarihte birkaç ciddi değişikliğe uğradı. Lityumun ilk büyük uygulaması, uçak motorları için yüksek-sıcaklık lityum gresleri ve II. Dünya Savaşı'nda ve kısa bir süre sonraki benzer uygulamalardı. Lityum bazlı sabunların diğer alkali sabunlara göre daha yüksek erime noktasına sahip olması ve kalsiyum bazlı sabunlara göre daha az aşındırıcı olması bu kullanımı desteklemiştir. Lityum sabunlarına ve yağlama greslerine olan az talep, çoğu ABD'de olmak üzere birkaç küçük madencilik operasyonuyla desteklendi.
Nükleer füzyon silahları üretimiyle Soğuk Savaş sırasında lityuma olan talep önemli ölçüde arttı. Hem lityum-6 hem de lityum-7, nötronlar tarafından ışınlandığında trityum üretir ve bu nedenle, kendi başına trityum üretiminin yanı sıra lityum döterid şeklinde hidrojen bombalarında kullanılan bir katı füzyon yakıtı biçimi için yararlıdır. ABD, 1950'lerin sonları ile 1980'lerin ortaları arasında başlıca lityum üreticisi haline geldi. Sonunda, lityum stoğu kabaca 42.000 ton lityum hidroksit idi. Depolanan lityum, birçok standartlaştırılmış kimyasalda lityumun ölçülen atomik ağırlığını ve hatta izotop ayırma tesislerinden boşaltılan ve yer altı sularına karışan lityum tuzları tarafından "kontamine olmuş" bazı "doğal kaynaklar"daki lityumun atom ağırlığını etkilemek için yeterli olan lityum-6'da %75 oranında tükendi.[24][25]


Lityum, camın erime sıcaklığını düşürmek ve Hall-Héroult işlemi'nde alüminyum oksit'in erime davranışını iyileştirmek için kullanılır.[26][27] Bu iki kullanım, 1990'ların ortalarına kadar pazara hakim oldu. nükleer silahlanma yarışı sona erdikten sonra, lityuma olan talep azaldı ve enerji stoklarının açık piyasada satılması fiyatları daha da düşürdü.[25] 1990'ların ortalarında, birçok şirket lityumu tuzlu su yeraltı veya açık ocak madenciliğinden daha ucuz bir seçenek olduğunu kanıtladı. Madenlerin çoğu kapandı veya odaklarını diğer malzemelere kaydırdı, çünkü yalnızca bölgelere ayrılmış pegmatitlerden elde edilen cevher rekabetçi bir fiyatla çıkarılabiliyordu. Örneğin, Kuzey Karolina, Kings Mountain yakınlarındaki ABD madenleri 21. yüzyılın başlangıcından önce kapandı.
Lityum iyon pillerin geliştirilmesi, lityum talebini artırdı ve 2007'de baskın kullanım haline geldi.[28] 2000'li yıllarda pillerdeki lityum talebinin artmasıyla birlikte, yeni şirketler artan talebi karşılamak için tuzlu su izolasyonu çalışmalarını büyüttüler.[29][30]
Yenilenebilir enerjiyle çalışan ve pillere bağımlı bir dünyada lityumun jeopolitik rekabetin ana nesnelerinden biri olacağı tartışıldı, ancak bu bakış açısı, artırılmış üretim için ekonomik teşviklerin gücünü hafife aldığı için de eleştirildi.[31]
Spodumen cevheri, LiAl(SiO3)2, Lityum içeriği nedeniyle ticari olarak çok önemlidir. Öncelikle 1100 °C’ de a formu ısıtılarak daha yumuşak b formuna dönüştürülür. b formu sıcak sülfürik asit ile reaksiyona sokularak Li2SO4L2So4H5rt5 elde edilir. Elde edilen bu çökelek çözeltiden ayrılarak Na3CO3 ile yıkanır. Böylece suda çözünmeyen Li2CO3 elde edilir. Manik depresif tedavisinde ve pillerde kullanılır.
Li2SO3 + Na2CO3 → Na2SO4 + Li2CO3 (katı)
Elde edilen Li2CO3 çökeleği HCl ile reaksiyona sokularak LiCl elde edilir.
Li2CO3 + 2 HCl → 2 LiCl + CO2 + H2O
LiCl erime noktası 600 °C den fazla olduğu için elektroliz ile saflaştırılması zor olduğundan LiCl (55%) ve KCl (45%) karışımı kullanılarak erime noktası 430 °C'ye düşürülür. Bu karışımın elektrolizi ile Li saf olarak elde edilir.
- Katot: Li+ (s) + e- → Li (s)
- Anot: Cl- (s) → ½ Cl2 (g) + e-
İçme Suyunda Lityum ve İlgili Bulgular
1990 yılında, ABD'nin Texas eyaletinin 28 idari bölümünde (county) içme sularındaki lityum miktarı üzerine bir araştırma yayımlanmıştır. Bu araştırma, içme suyundaki lityum miktarıyla intihar, cinayet ve tecavüz vakalarının negatif korelasyon gösterdiğini destekler veriler sunmuştur. Çalışmaya dahil edilen zaman aralığında, suyundaki lityum miktarı en yüksek bölgelerde, en düşük olan bölgelere kıyasla %40 daha az intihar vakası görülmüştür.
2009 yılında Japonya'da, 1 milyon insanın yaşadığı 18 şehri ve 5 senelik bir zaman dilimini kapsayan bir araştırma bu sonuçları desteklemiş. Bunu takiple Avustralya ve Yunanistan'da da bu iddiaları destekler sonuçların elde edildiği araştırmalar yapılmıştır. Bu araştırmanın sahibi araştırmacılar, çok düşük miktarlarda lityuma maruz kalmanın sinir sistemini koruyucu, hatta sinir hücresi gelişimini destekleyici etkilerinin olabileceği fikrini öne sürmüşlerdir.
Bu araştırmada kullanılan verilerin tekrar analiziyle yayımlanan ikinci bir araştırmada, içme suyundaki lityum miktarındaki artışın, çalışmada gözlenen ölüm oranlarıyla negatif korelasyon gösterdiği bulgulanmıştır.
Bu süreçte, İngiltere'de yapılan bir araştırma, yukarıda anlatılanlara aykırı bir sonuç vermiştir. Fakat bu araştırmaya konu olan bölgede içme sularındaki lityum miktarının, öteki çalışmalara ve ilgili bölgelere kıyasla çok daha düşüktür.[32]
Üretim
| Ülke | Üretim | Rezervler | Kaynaklar |
|---|---|---|---|
| Arjantin | 6,200 | 1,900,000 | 19,300,000 |
| Avustralya | 40,000 | 4,700,000 | 6,400,000 |
| Avusturya | - | - | 50,000 |
| Bolivya | - | - | 21,000,000 |
| Brezilya | 1,900 | 95,000 | 470,000 |
| Kanada | 0 | 530,000 | 2,900,000 |
| Şili | 18,000 | 9,200,000 | 9,600,000 |
| Çin | 14,000 | 1,500,000 | 5,100,000 |
| Çekya | - | - | 1,300,000 |
| Kongo Demokratik Cumhuriyeti | - | - | 3,000,000 |
| Finlandiya | - | - | 50,000 |
| Almanya | - | - | 2,700,000 |
| Gana | - | - | 90,000 |
| Hindistan | - | 5,900,000[34][35] | - |
| Kazakistan | - | - | 50,000 |
| Mali | - | - | 700,000 |
| Meksika | - | - | 1,700,000 |
| Namibya | - | - | 50,000 |
| Peru | - | - | 880,000 |
| Portekiz | 900 | 60,000 | 270,000 |
| Sırbistan | - | - | 1,200,000 |
| İspanya | - | - | 300,000 |
| Amerika Birleşik Devletleri | 870[note 1] | 750,000 | 7,900,000 |
| Zimbabve | 1,200 | 220,000 | 500,000 |
| Dünya toplamı | 82,000 | 21,000,000 | 86,000,000+ |
Uygulamalar

Piller
2021'de çoğu lityum, elektrikli otomobil'ler ve mobil cihazlar için lityum iyon pil yapmak için kullanıldı.
Seramik ve cam
Lityum oksit, silika işlemek için malzemenin erime noktası ve viskozitesini azaltarak akı olarak yaygın kullanılır ve düşük termal genleşme katsayıları dahil olmak üzere iyileştirilmiş fiziksel özelliklere sahip sırlar elde edilmesini sağlar. Dünya çapında bu, lityum bileşikleri için en büyük kullanımlardan biridir.[36][38] Fırın kapları için lityum oksit içeren sırlar kullanılır. Lityum karbonat (Li2CO3) genellikle bu uygulamada kullanılır çünkü ısıtıldığında okside dönüşür.[39]
Elektrik ve elektronik
20. yüzyılın sonlarında lityum, yüksek elektrot potansiyeli nedeniyle pil elektrolitlerinin ve elektrotlarının önemli bir bileşeni haline geldi. Düşük atom kütlesi nedeniyle, yüksek yük ve güç-ağırlık oranına sahiptir.
Tipik bir lityum-iyon pil, kurşun-asit için 2.1 volt ve çinko-karbon için 1.5 volt ile karşılaştırıldığında hücre başına yaklaşık 3 volt üretebilir. Şarj edilebilir ve yüksek enerji yoğunluklu lityum iyon piller, anot olarak lityum veya bileşikleri ile tek kullanımlık (birincil) piller olan lityum piller'den farklıdır.[40][41] Lityum kullanan diğer şarj edilebilir piller arasında lityum-iyon polimer pil, lityum demir fosfat pil ve nanotel pil bulunur.
Yıllar boyunca potansiyel büyüme konusunda görüşler farklı olmuştur. 2008'de yapılan bir araştırma, "gerçekçi olarak ulaşılabilir lityum karbonat üretiminin geleceğin PHEV ve EV küresel pazar gereksinimlerinin yalnızca küçük bir bölümü için yeterli olacağı", "Taşınabilir elektronik sektöründen gelen talebin önümüzdeki on yılda planlanan üretim artışlarının çoğunu alacağı" ve "lityum karbonatın seri üretimi çevreye duyarlı olmadığı, korunması gereken ekosistemlerde onarılamaz ekolojik hasara neden olacağı ve LiIon tahrikinin 'Yeşil Araba' kavramıyla bağdaşmadığı'" sonucuna varmıştır.[42]
Gres yağları
Lityumun en çok üçüncü kullanımı greslerdir. Lityum hidroksit güçlü bir bazdır ve bir yağ ile ısıtıldığında lityum stearat'tan yapılmış bir sabun üretir. Lityum sabun, yağları yoğunlaştırma özelliğine sahiptir ve çok amaçlı, yüksek sıcaklık gres yağları üretmek için kullanılır.[43][44][45]
Metalurji
Lityum (örn. lityum karbonat olarak), akışkanlığı arttırdığı sürekli döküm kalıp akı cüruflarına katkı maddesi olarak kullanılır,[46][47] 2011'de küresel lityum kullanımının %5'i burada kullanıldı.[48]
Lityum bileşikleri damarlanmayı azaltmak için demir dökümünde döküm kumu'na katkı maddesi (akı) olarak da kullanılır.[49]
Lityum (lityum florür olarak) alüminyum izabe tesislerine (Hall–Héroult prosesi) katkı maddesi olarak kullanılır. Böylece alüminyumun erime sıcaklığını düşürür ve elektrik direncini arttırır.[50] 2011'de üretimin %3'ü bunun için kullanıldı.[48]
Kaynak veya lehimleme için akı olarak kullanıldığında, metalik lityum işlem sırasında metallerin kaynaşmasını destekler[51] ve safsızlıkları emerek oksitlerin oluşumunu ortadan kaldırır.[52]
Alüminyum, kadmiyum, bakır ve manganez içeren metal alaşımları yüksek performanslı, az yoğun uçak parçaları yapımında kullanılır (ayrıca bkz. Lityum-alüminyum alaşımları).[53]
Silikon nano kaynak
Lityum, elektrikli piller ve diğer cihazlar için elektronik bileşenlerde silikon nano kaynakların mükemmelleştirilmesine yardımcı olmada etkili bulunmuştur.[54]

Hava temizleme
Lityum klorür ve lityum bromür, higroskopiktir ve gaz akışlarında kurutucu olarak kullanılır.[43] Lityum hidroksit ve lityum peroksit, uzay aracı ve denizaltıların kapalı alanlarda karbondioksit giderme ve hava temizleme için en çok kullanılan tuzlardır. Lityum hidroksit, lityum karbonat oluşturarak havadan karbon dioksit emer ve düşük ağırlığı nedeniyle diğer alkalin hidroksitlere göre tercih edilir.
Lityum peroksit (Li2O2) nem varlığında sadece karbon dioksit ile reaksiyona girerek lityum karbonat oluşturmakla kalmaz, aynı zamanda oksijeni de serbest bırakır.[56][57] Reaksiyon aşağıdaki gibidir:
- 2 Li2O2 + 2 CO2 → 2 Li2CO3 + O2.
Yukarıda bahsedilen bileşiklerin bazıları ve lityum perklorat denizaltılara oksijen veren oksijen mumlarında kullanılır. Bunlar ayrıca küçük miktarlarda bor, magnezyum, alüminyum, silikon, titanyum, manganez ve demir içerebilir.[58]
Optik
Kristal olarak yapay olarak büyütülen lityum florür, berrak ve şeffaftır ve genellikle IR, UV ve VUV (vakum UV) uygulamaları için özel optiklerde kullanılır. En yaygın malzemelerin derin UV'sinde en az kırılma indekslerinden birine ve en uzak iletim aralığına sahiptir.[59]
Termolüminesan radyasyon dozimetrisi (TLD) için ince bölünmüş lityum florür tozu kullanılmıştır: Böyle bir numune radyasyona maruz kaldığında, ısıtıldığında yoğunluğu alınan radyasyon dozu ile orantılı mavimsi bir ışık salınımıyla çözülen kristal hatalarını biriktirir böylece bunun nicelleştirilmesine izin verir.[60]
Lityum florür bazen teleskopların odak merceklerinde kullanılır.[43][61]
Lityum niyobat'ın yüksek doğrusal olmama özelliği, doğrusal olmayan optik uygulamalarda faydalanılır.
Cep telefonları ve optik modülatör'ler gibi telekomünikasyon ürünlerinde, rezonant kristal'ler gibi bileşenlerde yaygın kullanılır. Cep telefonlarının %60'ından fazlasında lityum uygulamaları kullanılır.[62]
Organik ve polimer kimyası
Organolityum bileşikleri, polimer ve ince-kimyasalların üretiminde çok kullanılır. Bu reaktiflerin baskın tüketicisi olan polimer endüstrisinde alkil lityum bileşikleri fonksiyonelleştirilmemiş olefinlerin anyonik polimerizasyondaki katalizörler/başlatıcılar'dır.[63][64][65][66] İnce kimyasalların üretimi için organolityum bileşikler, karbon-karbon bağlarının oluşumu için güçlü bazlar ve reaktifler olarak iş görür. Organolityum bileşikleri, lityum metal ve alkil halojenürlerden hazırlanır.[67]
Organik bileşikleri hazırlamak için reaktif olarak birçok başka lityum bileşiği kullanılır. Bazı popüler bileşikler arasında lityum alüminyum hidrit (LiAlH4), lityum trietilborohidrit, n-bütillityum ve tert-bütillityum bulunur.
Askeri
Lityum alüminyum hidrit (Li[AlH4) gibi metalik lityum ve onun kompleksi hidritler, roket itici gazlara yüksek enerjili katkı maddeleri olarak kullanılır.[15] Lityum alüminyum hidrit kendi başına katı yakıt olarak da kullanılabilir.[68]
Mark 50 torpidosu depolanmış kimyasal enerji sevk sistemi (SCEPS), katı lityum bloğu üzerine püskürtülen küçük bir kükürt hekzaflorür tankı kullanır. Reaksiyon, torpidoyu kapalı bir Rankine çevrimi içinde itmek için buhar oluşturarak ısı üretir.[69]
Lityum-6 içeren Lityum hidrit, bombanın füzyon aşaması için yakıt görevi gördüğü termonükleer silahlarda kullanılır.[70]

İçecek sanayi
"7-Up", piyasaya "Bib-label Lithiated Lemon-Lime Soda" ismiyle sürülmüştür. İçecek, 1950 yılına kadar da lityum sitrat içermiştir. Şehir efsanelerine göre içeceğin ismindeki "7", lityumun atom ağırlığından kaynaklıdır.[32]
Tıp
Lityum tuzları bipolar bozukluk tedavisinde, duygu durum dengeleyici olarak kullanılır.[71] Lityumun bu etkisi 1949 yılında Avustralyalı psikiyatr John Cade tarafından belgelenmiştir. FDA, 1970 yılında lityumun etkili bir ilaç olarak tanındığını duyurmuştur.[32]
Lityumun hem depresyon hem mani üzerinde etkisi olsa da hipomanik veya manik dönem üzerindeki etkisi daha baskındır. Lityum, depresyon tedavisinde öteki antidepresanların etkisini güçlendirmek için de kullanılmaktadır.
Lityum, sindirilmesinin ardından, merkezi sinir sisteminde hızla yayılır ve çeşitli nörotransmitterler ve almaçlarla etkileşir. Norepinefrin salınımını azalttığı ve serotonin sentezini arttırdığı bilinmektedir. Mani üzerindeki etkisini ortaya çıkaran mekanizma bilinmemektedir.
Lityum tuzları, şizoaffektif bozukluk ve döngüsel majör depresyon gibi ilgili teşhisler için de yardımcı olabilir. Bu tuzların aktif kısmı lityum iyon Li+'tur.[71] Hamileliğin ilk üç aylık dönemindeki tedavi sırasında lityum alan kadınlardan doğan bebeklerde bunlar Ebstein kalp anomalisi gelişme riskini artırabilirler.[72]
Baş zonklamasında olası tedavi olarak lityum da araştırılmıştır.[73]
Notlar
- ^ In 2013
Kaynakça
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. ss. E110. ISBN 0-8493-0464-4.
- ^ D'Andraba (1800). "Des caractères et des propriétés de plusieurs nouveaux minérauxde Suède et de Norwège, avec quelques observations chimiques faites sur ces substances". Journal de Physique, de Chimie, d'Histoire Naturelle, et des Arts. 51: 239. 13 Temmuz 2015 tarihinde kaynağından arşivlendi.
- ^ "Petalite Mineral Information". Mindat.org. 16 Şubat 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2009.
- ^ a b c d e f g "Lithium:Historical information". 16 Ekim 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2009.
- ^ Weeks, Mary (2003). Discovery of the Elements. Whitefish, Montana, United States: Kessinger Publishing. s. 124. ISBN 978-0-7661-3872-8. Erişim tarihi: 10 Ağustos 2009.[]
- ^ Berzelius (1817). "Ein neues mineralisches Alkali und ein neues Metall" [A new mineral alkali and a new metal]. Journal für Chemie und Physik. 21: 44-48. 3 Aralık 2016 tarihinde kaynağından arşivlendi. From p. 45: "Herr August Arfwedson, ein junger sehr verdienstvoller Chemiker, der seit einem Jahre in meinem Laboratorie arbeitet, fand bei einer Analyse des Petalits von Uto's Eisengrube, einen alkalischen Bestandtheil, … Wir haben es Lithion genannt, um dadurch auf seine erste Entdeckung im Mineralreich anzuspielen, da die beiden anderen erst in der organischen Natur entdeckt wurden. Sein Radical wird dann Lithium genannt werden." (Mr. August Arfwedson, a young, very meritorious chemist, who has worked in my laboratory for a year, found during an analysis of petalite from Uto's iron mine, an alkaline component … We've named it lithion, in order to allude thereby to its first discovery in the mineral realm, since the two others were first discovered in organic nature. Its radical will then be named "lithium".)
- ^ "Johan August Arfwedson". Periodic Table Live!. 7 Ekim 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2009.
- ^ "Johan Arfwedson". 5 Haziran 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2009.
- ^ a b c van der Krogt, Peter. "Lithium". Elementymology & Elements Multidict. 16 Haziran 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ekim 2010.
- ^ Clark, Jim (2005). "Compounds of the Group 1 Elements". 11 Mart 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ağustos 2009.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;krebsisimli refler için metin sağlanmadı (Bkz: ) - ^ See:
- Arwedson, Aug. (1818) "Undersökning af några vid Utö Jernmalmsbrott förekommende Fossilier, och af ett deri funnet eget Eldfast Alkali" 25 Kasım 2017 tarihinde Wayback Machine sitesinde arşivlendi., Afhandlingar i Fysik, Kemi och Mineralogi, 6 : 145–172. (in Swedish)
- Arwedson, Aug. (1818) "Untersuchung einiger bei der Eisen-Grube von Utö vorkommenden Fossilien und von einem darin gefundenen neuen feuerfesten Alkali" 13 Mart 2021 tarihinde Wayback Machine sitesinde arşivlendi. (Investigation of some minerals occurring at the iron mines of Utö and of a new refractory alkali found therein), Journal für Chemie und Physik, 22 (1) : 93–117. (in German)
- ^ Gmelin, C. G. (1818). "Von dem Lithon" [On lithium]. Annalen der Physik. 59 (7): 238-241. Bibcode:1818AnP....59..229G. doi:10.1002/andp.18180590702. 9 Kasım 2015 tarihinde kaynağından arşivlendi.
p. 238 Es löste sich in diesem ein Salz auf, das an der Luft zerfloss, und nach Art der Strontiansalze den Alkohol mit einer purpurrothen Flamme brennen machte. (There dissolved in this [solvent; namely, absolute alcohol] a salt that deliquesced in air, and in the manner of strontium salts, caused the alcohol to burn with a purple-red flame.)
- ^ a b Enghag, Per (2004). Encyclopedia of the Elements: Technical Data – History –Processing – Applications. Wiley. ss. 287-300. ISBN 978-3-527-30666-4.
- ^ a b Emsley, John (2001). Nature's Building Blocks. Oxford: Oxford University Press. ISBN 978-0-19-850341-5.
- ^ Brande, William Thomas (1821) A Manual of Chemistry, 2nd ed. London, England: John Murray, vol. 2, pp. 57-58. 22 Kasım 2015 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ "The Quarterly journal of science and the arts". The Quarterly Journal of Science and the Arts. Royal Institution of Great Britain. 5: 338. 1818. 13 Mart 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ekim 2010.
- ^ "Timeline science and engineering". DiracDelta Science & Engineering Encyclopedia. 5 Aralık 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Eylül 2008.
- ^ Brande, William Thomas; MacNeven, William James (1821). A manual of chemistry. Long. s. 191. Erişim tarihi: 8 Ekim 2010.
- ^ Bunsen, R. (1855). "Darstellung des Lithiums" [Preparation of lithium]. Annalen der Chemie und Pharmacie. 94: 107-111. doi:10.1002/jlac.18550940112. 6 Kasım 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Ağustos 2015.
- ^ Green, Thomas (11 Haziran 2006). "Analysis of the Element Lithium". echeat. 21 Nisan 2012 tarihinde kaynağından arşivlendi.
- ^ Garrett, Donald E. (5 Nisan 2004). Handbook of Lithium and Natural Calcium Chloride. s. 99. ISBN 9780080472904. 3 Aralık 2016 tarihinde kaynağından arşivlendi.
- ^ Shorter, Edward (June 2009). "The history of lithium therapy". Bipolar Disorders. 11 (Suppl 2): 4-9. doi:10.1111/j.1399-5618.2009.00706.x. ISSN 1398-5647. PMC 3712976 $2. PMID 19538681.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;Coplen2002isimli refler için metin sağlanmadı (Bkz: ) - ^ a b Ober, Joyce A. (1994). "Commodity Report 1994: Lithium" (PDF). United States Geological Survey. 9 Haziran 2010 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 3 Kasım 2010.
- ^ Deberitz, Jürgen; Boche, Gernot (2003). "Lithium und seine Verbindungen - Industrielle, medizinische und wissenschaftliche Bedeutung". Chemie in unserer Zeit. 37 (4): 258-266. doi:10.1002/ciuz.200300264.
- ^ Bauer, Richard (1985). "Lithium - wie es nicht im Lehrbuch steht". Chemie in unserer Zeit. 19 (5): 167-173. doi:10.1002/ciuz.19850190505.
- ^ Ober, Joyce A. (1994). "Minerals Yearbook 2007 : Lithium" (PDF). United States Geological Survey. 17 Temmuz 2010 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 3 Kasım 2010.
- ^ Kogel, Jessica Elzea (2006). "Lithium". Industrial minerals & rocks: commodities, markets, and uses. Littleton, Colo.: Society for Mining, Metallurgy, and Exploration. s. 599. ISBN 978-0-87335-233-8. 7 Kasım 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Kasım 2020.
- ^ McKetta, John J. (18 Temmuz 2007). Encyclopedia of Chemical Processing and Design: Volume 28 – Lactic Acid to Magnesium Supply-Demand Relationships. M. Dekker. ISBN 978-0-8247-2478-8. 28 Mayıs 2013 tarihinde kaynağından arşivlendi.
- ^ Overland, Indra (1 Mart 2019). "The geopolitics of renewable energy: Debunking four emerging myths" (PDF). Energy Research & Social Science. 49: 36-40. doi:10.1016/j.erss.2018.10.018
 . ISSN 2214-6296. 13 Mart 2021 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 25 Ağustos 2019.
. ISSN 2214-6296. 13 Mart 2021 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 25 Ağustos 2019. - ^ a b c "Should We All Take a Bit of Lithium?". 5 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Kasım 2015.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;uslitisimli refler için metin sağlanmadı (Bkz: ) - ^ "India finds 5.9 million tonnes lithium deposits in Jammu and Kashmir". 10 Şubat 2023 tarihinde kaynağından arşivlendi.
- ^ "5.9 million tonnes Lithium deposits found in J&K: Why it's important". The Times of India. 10 Şubat 2023 tarihinde kaynağından arşivlendi.
- ^ a b "Lithium" (PDF). 2016. 30 Kasım 2016 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 29 Kasım 2016 – US Geological Survey (USGS) vasıtasıyla.
- ^ "Lithium" (PDF). USGS. USGS. 1 Kasım 2020 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 15 Kasım 2020.
- ^ "Fmclithium.com" (PDF). www.fmclithium.com. 7 Eylül 2014 tarihinde kaynağından (PDF) arşivlendi.
- ^ Clark, Jim (2005). "Some Compounds of the Group 1 Elements". chemguide.co.uk. 27 Haziran 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Ağustos 2013.
- ^ "Disposable Batteries - Choosing between Alkaline and Lithium Disposable Batteries". Batteryreview.org. 6 Ocak 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ekim 2013.
- ^ "Battery Anodes > Batteries & Fuel Cells > Research > The Energy Materials Center at Cornell". Emc2.cornell.edu. 22 Aralık 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ekim 2013.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;meridianisimli refler için metin sağlanmadı (Bkz: ) - ^ a b c Kaynak hatası: Geçersiz
<ref>etiketi;CRCisimli refler için metin sağlanmadı (Bkz: ) - ^ Totten, George E.; Westbrook, Steven R.; Shah, Rajesh J. (2003). Fuels and lubricants handbook: technology, properties, performance, and testing. 1. ASTM International. s. 559. ISBN 978-0-8031-2096-9. 23 Temmuz 2016 tarihinde kaynağından arşivlendi.
- ^ Rand, Salvatore J. (2003). Significance of tests for petroleum products. ASTM International. ss. 150-152. ISBN 978-0-8031-2097-6. 31 Temmuz 2016 tarihinde kaynağından arşivlendi.
- ^ The Theory and Practice of Mold Fluxes Used in Continuous Casting: A Compilation of Papers on Continuous Casting Fluxes Given at the 61st and 62nd Steelmaking Conference, Iron and Steel Society
- ^ Lu, Y. Q.; Zhang, G. D.; Jiang, M. F.; Liu, H. X.; Li, T. (2011). "Effects of Li2CO3 on Properties of Mould Flux for High Speed Continuous Casting". Materials Science Forum. 675–677: 877-880. doi:10.4028/www.scientific.net/MSF.675-677.877.
- ^ a b Kaynak hatası: Geçersiz
<ref>etiketi;minerals.usgs.govisimli refler için metin sağlanmadı (Bkz: ) - ^ "Testing 1-2-3: Eliminating Veining Defects", Modern Casting, July 2014, 2 Nisan 2015 tarihinde kaynağından arşivlendi, erişim tarihi: 15 Mart 2015
- ^ Haupin, W. (1987), Mamantov, Gleb; Marassi, Roberto (Ed.), "Chemical and Physical Properties of the Hall-Héroult Electrolyte", Molten Salt Chemistry: An Introduction and Selected Applications, Springer, s. 449
- ^ Garrett, Donald E. (5 Nisan 2004). Handbook of Lithium and Natural Calcium Chloride (İngilizce). Academic Press. s. 200. ISBN 9780080472904. 3 Aralık 2016 tarihinde kaynağından arşivlendi.
- ^ Prasad, N. Eswara; Gokhale, Amol; Wanhill, R. J. H. (20 Eylül 2013). Aluminum-Lithium Alloys: Processing, Properties, and Applications (İngilizce). Butterworth-Heinemann. ISBN 9780124016798. 1 Ocak 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Kasım 2020.
- ^ Davis, Joseph R. ASM International. Handbook Committee (1993). Aluminum and aluminum alloys. ASM International. ss. 121-. ISBN 978-0-87170-496-2. 28 Mayıs 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Mayıs 2011.
- ^ Karki, Khim; Epstein, Eric; Cho, Jeong-Hyun; Jia, Zheng; Li, Teng; Picraux, S. Tom; Wang, Chunsheng; Cumings, John (2012). "Lithium-Assisted Electrochemical Welding in Silicon Nanowire Battery Electrodes" (PDF). Nano Letters. 12 (3): 1392-7. Bibcode:2012NanoL..12.1392K. doi:10.1021/nl204063u. PMID 22339576. 10 Ağustos 2017 tarihinde kaynağından arşivlendi (PDF).
- ^ Koch, Ernst-Christian (2004). "Special Materials in Pyrotechnics: III. Application of Lithium and its Compounds in Energetic Systems". Propellants, Explosives, Pyrotechnics. 29 (2): 67-80. doi:10.1002/prep.200400032.
- ^ Mulloth, L.M.; Finn, J.E. (2005). "Air Quality Systems for Related Enclosed Spaces: Spacecraft Air". The Handbook of Environmental Chemistry. 4H. ss. 383-404. doi:10.1007/b107253. ISBN 978-3-540-25019-7.
- ^ "Application of lithium chemicals for air regeneration of manned spacecraft". Lithium Corporation of America & Aerospace Medical Research Laboratories. 1965. 7 Ekim 2012 tarihinde kaynağından arşivlendi.
- ^ Markowitz, M. M.; Boryta, D. A.; Stewart, Harvey (1964). "Lithium Perchlorate Oxygen Candle. Pyrochemical Source of Pure Oxygen". Industrial & Engineering Chemistry Product Research and Development. 3 (4): 321-30. doi:10.1021/i360012a016.
- ^ Hobbs, Philip C. D. (2009). Building Electro-Optical Systems: Making It All Work. John Wiley and Sons. s. 149. ISBN 978-0-470-40229-0. 23 Haziran 2016 tarihinde kaynağından arşivlendi.
- ^ Point Defects in Lithium Fluoride Films Induced by Gamma Irradiation. Proceedings of the 7th International Conference on Advanced Technology & Particle Physics: (ICATPP-7): Villa Olmo, Como, Italy. 2001. World Scientific. 2002. s. 819. ISBN 978-981-238-180-4. 6 Haziran 2016 tarihinde kaynağından arşivlendi.
- ^ Sinton, William M. (1962). "Infrared Spectroscopy of Planets and Stars". Applied Optics. 1 (2): 105. Bibcode:1962ApOpt...1..105S. doi:10.1364/AO.1.000105.
- ^ "You've got the power: the evolution of batteries and the future of fuel cells" (PDF). Toshiba. 17 Temmuz 2011 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 17 Mayıs 2009.
- ^ "Organometallics". IHS Chemicals. February 2012. 7 Temmuz 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Ocak 2012.
- ^ Yurkovetskii, A. V.; Kofman, V. L.; Makovetskii, K. L. (2005). "Polymerization of 1,2-dimethylenecyclobutane by organolithium initiators". Russian Chemical Bulletin. 37 (9): 1782-1784. doi:10.1007/BF00962487.
- ^ Quirk, Roderic P.; Cheng, Pao Luo (1986). "Functionalization of polymeric organolithium compounds. Amination of poly(styryl)lithium". Macromolecules. 19 (5): 1291-1294. Bibcode:1986MaMol..19.1291Q. doi:10.1021/ma00159a001.
- ^ Stone, F. G. A.; West, Robert (1980). Advances in organometallic chemistry. Academic Press. s. 55. ISBN 978-0-12-031118-7. 13 Mart 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Kasım 2020.
- ^ Bansal, Raj K. (1996). Synthetic approaches in organic chemistry. s. 192. ISBN 978-0-7637-0665-4. 18 Haziran 2016 tarihinde kaynağından arşivlendi.
- ^ "AN EXPERIMENTAL INVESTIGATION OF A LITHIUM ALUMINUM HYDRIDE-HYDROGEN PEROXIDE HYBRID ROCKET" (PDF). 28 Haziran 2003. 28 Haziran 2003 tarihinde kaynağından (PDF) arşivlendi.
- ^ Hughes, T.G.; Smith, R.B.; Kiely, D.H. (1983). "Stored Chemical Energy Propulsion System for Underwater Applications". Journal of Energy. 7 (2): 128-133. Bibcode:1983JEner...7..128H. doi:10.2514/3.62644.
- ^ Emsley, John (2011). Nature's Building Blocks.
- ^ a b Kean, Sam (2011). The Disappearing Spoon.
- ^ Yacobi S; Ornoy A (2008). "Is lithium a real teratogen? What can we conclude from the prospective versus retrospective studies? A review". Isr J Psychiatry Relat Sci. 45 (2): 95-106. PMID 18982835.
- ^ Lieb, J.; Zeff (1978). "Lithium treatment of chronic cluster headaches" (PDF). The British Journal of Psychiatry. 133 (6): 556-558. doi:10.1192/bjp.133.6.556. PMID 737393. 9 Şubat 2020 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 26 Aralık 2020.
Ayrıca bakınız
- Aktiflik