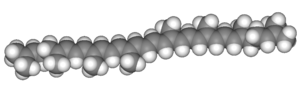
Deoksiriboz nükleik asit veya kısaca DNA, tüm organizmaların ve bazı virüslerin canlılık işlevleri ve biyolojik gelişmeleri için gerekli olan genetik talimatları taşıyan bir nükleik asittir. DNA'nın başlıca rolü bilgiyi uzun süre saklamasıdır. Protein ve RNA gibi hücrenin diğer bileşenlerinin inşası için gerekli olan bilgileri içermesinden dolayı DNA; bir kalıp, şablon veya reçeteye benzetilir. Bu genetik bilgileri içeren DNA parçaları gen olarak adlandırılır. Bazı DNA dizilerinin yapısal işlevleri vardır, diğerleri ise bu genetik bilginin ne şekilde kullanılacağının düzenlenmesine yararlar.
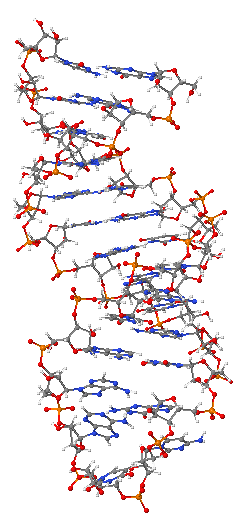
Ribonükleik asid (RNA), bir nükleik asittir, nükleotitlerden oluşan bir polimerdir. Her nükleotit bir azotlu baz, bir riboz şeker ve bir fosfattan oluşur. RNA pek çok önemli biyolojik rol oynar, DNA'da taşınan genetik bilginin proteine çevirisi (translasyon) ile ilişkili çeşitli süreçlerde de yer alır. RNA tiplerinden olan mesajcı RNA, DNA'daki bilgiyi protein sentez yeri olan ribozomlara taşır, ribozomal RNA ribozomun en önemli kısımlarını oluşturur, taşıyıcı RNA ise protein sentezinde kullanılmak üzere kullanılacak aminoasitlerin taşınmasında gereklidir. Ayrıca çeşitli RNA tipleri genlerin ne derece aktif olduğunu düzenlemeye yarar.

Karbon, doğada yaygın bulunan ametal kimyasal elementtir. Evrende bolluk bakımından altıncı sırada yer alan karbon, kızgın yıldızlarda hidrojenin termonükleer yanmasında temel rol oynar. Dünyada hem doğal halde, hem de başka elementlerle bileşik halinde bulunan karbon, ağırlık olarak Dünya'nın yerkabuğunun yaklaşık %0,2'sini oluşturur. En arı (katışıksız) biçimleri elmas ve grafittir; daha düşük arılık derecelerinde maden kömürünün, kok kömürünün ve odun kömürünün bileşeni olarak bulunur. Atmosferin yaklaşık % 0,05'ini oluşturan ve bütün doğal sularda erimiş olarak bulunan karbon dioksit, kireç taşı ve mermer gibi karbonat mineralleri, kömürün, petrolün ve doğalgazın başlıca yapıtaşları olan hidrokarbonlar, en bol bulunan bileşikleridir.

Oksijen atom numarası 8 olan ve O harfi ile simgelenen kimyasal elementtir. Oksijen ismi Yunanca ὀξύς (oxis - "asit", tam anlamıyla "keskin", asitlerin acı tadı kastedilir) ve -γενής (-genēs) ("üretici", tam anlamıyla "sebep olan şey") köklerinden gelmektedir, çünkü isimlendirildiği zamanlarda tüm asitlerin oksijen içerikli olduğu sanılırdı. Standart şartlar altında, elementin iki atomu bağlanarak çok soluk mavi renkte, kokusuz, tatsız, diatomik yapıdaki, O2 formülüne sahip dioksijen gazını oluşturur.

Antioksidan veya yükseltgeme önleyici, yağların oksidasyonunu yavaşlatan madde. Canlılarda, kimyasal süreçler, özellikle oksitlenme, erkin radikallerin oluşmasına neden olur. Yüksek derecede ayıraç olan serbest radikaller farklı moleküller ile kolayca tepkimeye girebilir ve böylece hücrelere, canlıya zarar verebilir. Antioksidanlar serbest radikallerle tepkimeye girerek hücrelere zarar vermelerini önler. Bu özellikleriyle hücrelerin anormalleşme ve sonuç olarak tümör oluşturma risklerini azalttıkları gibi, hücre yıkımını da azalttıkları için, daha sağlıklı ve yaşlılık etkilerinin en az olduğu bir yaşam yaşama şansını yükseltir.
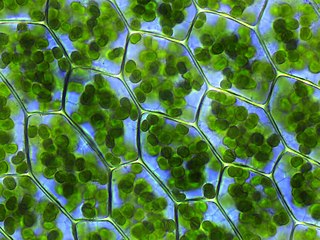
Plastitler, deniz yosunu, bitki ve kimi protist hücrelerinde bulunan, çeşitli görevleri olan çift zarlı temel organeldir. 1,5 milyar yıl önce endosimbiyoz ile ökaryot hücrelerine aktarılmış siyanobakteriler olarak değerlendirilir. Genç hücrelerde renksiz olan plastitler (lökoplast), hücre ile birlikte gelişerek, hücrenin görevine uygun biçim ve renk kazanır. Bulundurdukları pigment ve görevlerine göre birbirine dönüşebilen üç çeşit plastit vardır:

Molekül, birbirine bağlı gruplar halindeki atomların oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır. Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farklı sayılarda farklı atomların bağlanması sonucunda oluşabilirler. Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve 2 oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 1996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen. Molekülleri oluşturan kimyasal bağlara Moleküler bağlar denir. Bunlar kovalent, iyonik ve metalik bağlardır.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.

Karotenoid bitkilerde ve bazı diğer fotosentetik mikroorganizmalarda bulunan biyolojik pigmenttir. Altı yüzün üzerinde bilinen karotenoid vardır; ksantofiller ve karotenler olarak iki sınıfa ayrılır.

Prostat kanseri eril üreme sisteminde yer alan bir bez olan prostatta gelişen bir kanserdir. Prostat kanserlerinin çoğu yavaş gelişim gösterir; bununla beraber, görece hızlı gelişim gösterenleri de vardır. Prostat kanseri hücreleri prostattan vücudun diğer kısımlarına, özellikle kemiklere ve lenf düğümlerine yayılabilir. Başlangıçta hiçbir belirti vermeyebilir. İlerleyen aşamalarda ise işemede zorluk, idrarda kan ya da pelviste, sırtta veya işeme sırasında ağrıya sebep olabilir. İyi huylu prostat büyümesi olarak bilinen hastalık da benzer belirtiler verebilir. İleri aşamada ortaya çıkan diğer belirtiler arasında düşük alyuvar hücresi sayısından kaynaklanan yorgunluk hissi sayılabilir.

Karoten, C40H56 formüllü birbiriyle ilişkili birkaç bileşik için kullanılan bir terimdir. Karoten, fotosentez için önemli bir fotosentetik pigmenttir. Soğurduğu ışığı klorofile aktararak fotosenteze katkıda bulunur. Havuç ve çoğu başka sebze ve meyvelerin turuncu renginden sorumludur.

Kızılötesi, görünür ışıktan daha uzun ancak mikrodalgalardan daha kısa dalga boylarına sahip elektromanyetik radyasyondur (EMR). Kızılötesi spektral bant, kırmızı ışığınkinden biraz daha uzun dalgalarla başlar, bu nedenle IR insan gözü için görünmezdir. IR'nin genellikle yaklaşık 750 nm (400 THz) ila 1 mm (300 GHz) arasındaki dalga boylarını içerdiği anlaşılmaktadır.

Genetikte, mikroRNA (miRNA) yaklaşık 21-23 nükleotit uzunluğunda tek iplikli RNA molekülü türüdür, gen ifadesinin düzenlenmesinde rol oynar. miRNA'lar kodlamayan RNA'lardandır, yani DNA'dan transkripsiyonu yapılan ama proteine çevirisi yapılmayan genler tarafından kodlanırlar. Pri-miRNA olarak adlandırılan primer transkriptler işlenerek, önce pre-miRNA adlı kısa sap-ilmik yapılarına, sonra da fonksiyonel miRNA'ya dönüşürler. Olgun miRNA moleküller bir veya daha çok mesajcı RNA (mRNA) ile kısmî tamamlayıcıdır ve başlıca işlevleri gen ifadesini aşağı ayarlamaktır. 1993'te Lee ve çalışma arkadaşları tarafından Victor Ambros laboratuvarında keşfedilmişlerdir, ancak mikroRNA terimi ilk 2001'de kullanıma girimiştir.
Biyokimyada, liyaz, hidroliz ve yükseltgenme (oksidasyon) harici yollarla çeşitli kimyasal bağları kırabilen, çoğu zaman bunu yeni bir çift bağ veya halka yapısı oluşturarak gerçekleştiren bir enzimdir. Örneğin bu reaksiyonu katalizleyen enzim bir liyazdır.
- ATP → cAMP + PPi

Kimyada radikaller eşleşmemiş elektronu olan atom, molekül veya iyonlardır. Bu eşleşmemiş elektronlar genelde son derece reaktiftir. Radikaller, yanma, atmosfer kimyası, polimerleşme, plazma kimyası, biyokimya ve pek çok başka kimyasal süreçte önemli rol oynar. Örneğin, insan fizyolojisinde, süperoksit ve azot oksit, damar tonusu gibi pek çok biyolojik süreci düzenler. Radikal ve serbest radikal terimleri genelde eşanlamlı kullanılmakla beraber, bir radikal bir çözelti kafesi içinde hapsolmuş veya başka bir moleküle bağlanmış durumda olabilir. 1900'de Michigan Üniversitesi'nde Moses Gomberg tarafından betimlenen trifenilmetil radikali, ilk tespit edilmiş organik serbest radikal olmuştur.

Organik kimyada bazı atom halkalarının yapısı beklenenin üstünde kararlıdır. Doymamış bağlar, yalın elektron çiftleri veya boş orbitallerden oluşan konjüge bir halkanın konjüge olmasından beklenecek kararlılıktan daha yüksek bir kararlılık gösterme özelliğine aromatiklik denir. Aromatiklik, halkasal delokalizasyon ve rezonansın bir belirtisi olarak da düşünülebilir.
Çift kırılma, bir ışının anisotropik (eşyönsüz) maddelerden geçerken iki ışına ayrışmasıdır. Kalsit ya da boron nitrit bu türden maddelere örnek olarak verilebilir. Bu etki ilk olarak Danimarkalı bilim adamı Rasmus Barthonlin tarafından 1669da kalsit üzerinde gözlemlendi. Bu etkinin belli plastik, manyetik, çeşitli kristal yapıda olmayan maddeler ve sıvı kristallerde de olur.
Trans yağ, trans-izomer (E-izomer) doymamış yağ asitlerine verilen yaygın ad. Terim çift karbon-karbon bağının konfigürasyonuna işaret ettiğinden trans yağlar bazen tekli bazen de çoklu doymamış yağ olabilir, ama hiçbir zaman doymuş yağ olamaz.

Oksijen doygunluğu, kandaki oksijen derişimini belirten bir terimdir. İnsan vücudu, kandaki oksijen düzeyinin çok duyarlı olarak özellikli bir değerde bulunmasına ihtiyaç duyar ve vücut bunun için gerekli düzenlemeleri yapar. İnsan kanındaki oksijen düzeyinin yüzde 97 ile 100 arasında olması olağan kabul edilir. Yüzde 90'ın altındaki oksijen düzeyi düşük olarak kabul edilir ve bu, hipoksemiye neden olabilir. Yüzde 80'in altındaki oksijen düzeyleri, bu düzeylerde beyin ve kalp gibi organların çalışması bozulabileceğinden, gecikmeksizin müdahale gerektirir. Düşük oksijen düzeyinin sürekli olması, solunum krizi ya da kalp krizi ile sonuçlanabilir.

Fiziğin optik alanında, geçirgenlik ışığın bir materyal üzerinden dağılmadan geçebilmesine olanak sağlayan fiziksel bir özelliktir. Makroskopik (büyük) ölçeklerde, fotonların Snell kanununa göre hareket ettikleri söylenebilir. Yarı saydamlık, geçirgenliğin içinde bulunan bir üst kümedir ve ışığın geçmesine izin verir ancak Snell kanununu takip etmek zorunda değildir. Fotonlar, kırınım işaretleri içinde herhangi bir değişim meydana geldiğinde her iki arayüzde de dağınım gösterebilirler. Diğer bir deyişle, yarı saydam bir ortam ışığın ulaşım yapmasına olanak sağlarken saydam olan bir ortam sadece ışığın geçişini onaylamakla kalmaz aynı zamanda görüntü oluşumuna da izin verir. Yarı saydamlığın karşıtı olan kavram opaklıktır. Saydam yani geçirgen olan maddeler oldukça net görülen, tamamının tek bir renge sahip olduğu ya da her rengi içeren bir spekturumu meydana getiren herhangi bir kombinasyona sahip olabilir.