Kimya, maddenin yapısını, özelliklerini, birleşimlerini, etkileşimlerini, tepkimelerini araştıran ve uygulayan bilim dalıdır. Kimya bilmi daha kapsamlı bir ifadeyle maddelerin özellikleriyle, sınıflandırılmasıyla, atomlarla, atom teorisiyle, kimyasal bileşiklerle, kimyasal tepkimelerle, maddenin hâlleriyle, moleküller arası ve moleküler kuvvetlerle, kimyasal bağlarla, tepkime kinetiğiyle, kimyasal dengenin prensipleriyle vb konularla ilgilenir. Kimyanın en önemli dalları arasında analitik kimya, anorganik kimya, organik kimya, fizikokimya ve biyokimya sayılır.

Elektron dizilimi, atom fiziği ve kuantum kimyasında, bir atom ya da molekülün elektronlarının atomik ya da moleküler orbitallerdeki dağılımıdır. Örneğin Neon atomunun elektron dizilimi 1s2 2s2 2p6 olarak gösterilir.

Porfirin, dört metiliden (-CH=) köprüsüyle birbirine bağlı dört pirol halkasından ibaret olan porfin halka sistemi ihtiva eden molekül sistemidir. Bu molekül inorganik yapının organik yani canlı yaşamına nasıl evrildiğinin anlaşılmasını da sağlamıştır. Yani dünyadaki yaşam cansızdan canlıya bu madde ile geçmiştir. Doğada genellikle I ve III numaralı porfirin şekli bulunur. Porfirinlerdeki yan grupların dizilimi simetrik olduğu takdirde Tip I; asimetrik olduğu takdirde Tip III izomerleri oluşur. Tip III izomerleri en fazla bulunan ve önemli olan tiptir.

Kobalt kimyasal bir element'tir. Sembol'ü Co ve atom numarası 27'dir. Nikel gibi kobalt da, doğal meteorik demir alaşımlarında bulunan küçük birikintiler dışında, yer kabuğunda yalnızca kimyasal olarak birleşik formda bulunur. İndirgeyici eritme yoluyla üretilen serbest element sert, parlak, gümüş rengi bir metal'dir.

İyon ya da yerdeş, bir veya daha çok elektron kazanmış ya da yitirmiş bir atomdan oluşmuş elektrik yüklü parçacıktır. Atomlar kararsız yapılarından kurtulmak ve kararlı hale gelebilmek için elektron alırlar ya da kaybederler. Bunun için de başka bir atomla ya da kökle bağ kurarlar.

Kovalent bağ, atomlar arasında elektron çiftleri oluşturmak için elektronların paylaşımını içeren kimyasal bağdır. Bu elektron çiftlerine paylaşılan çiftler veya bağ çiftleri denir. Atomlar arasında elektronları paylaştıklarında çekici ve itici kuvvetlerin kararlı dengesine kovalent bağ denir. Birçok molekül için elektronların paylaşılması her atomun kararlı elektronik gruplaşmasına denk gelen tam değerlik kabuğunun eşdeğerine ulaşmasına olanak tanır.

Kimyasal bağ, atomların veya iyonların molekülleri, kristalleri ve diğer yapıları oluşturmak üzere birleşmesidir. Bağ, iyonik bağlar'da olduğu gibi zıt yüklü iyonlar arasındaki elektrostatik kuvvetten veya kovalent bağ'larda olduğu gibi elektronların paylaşılmasından veya bu etkilerin bazı kombinasyonlarından kaynaklanabilir. Açıklanan kimyasal bağların farklı mukavemetleri vardır: kovalent, iyonik ve metalik bağlar gibi "güçlü bağlar" veya "birincil bağlar" ve dipol-dipol etkileşimleri, London dağılım kuvveti ve hidrojen bağı gibi "zayıf bağlar" veya "ikincil bağlar" vardır.

Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür oksidasyona, diğer türler indirgemeye uğrar. Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.

Kimyada amid sözcüğü iki anlama sahiptir: - Birinci anlamıyla amid, bir azot atomuna (N) bağlı bir karbonil grubu bulunduran bir organik fonksiyonel grup veya bu gruba sahip bir bileşiktir. - İkinci anlamıyla amid, bir azot anyonudur.

Kimyada asil grubu bir oksoasitten bir veya daha fazla hidroksil grubunun çıkartılmasıyla kalan fonksiyonel gruptur. Sözcük, 'asit radikali' anlamından türetilmiştir, 'asil' Türkçeye Fransızca 'acyle' den girmiş, 'açil' ise İtalyanca 'acile'den. Bir asil grubunun eklenmesine asilasyon denir.
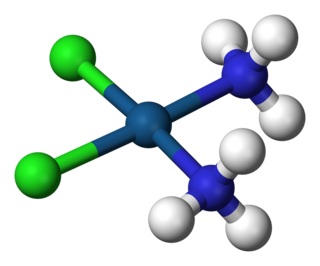
Kompleks, merkez atom olarak bir ya da birden fazla metal atomu veya iyonu ve metale bağlı ligandlardan oluşan yapıdır. Ligand, metale elektron vererek kompleks oluşturur. Metal içeren bileşiklerin birçoğu, özellikle geçiş metalleri içerenler koordinasyon bileşikleridir.

Ligand ya da ligant, bir biyomoleküle bağlanarak bir kompleks oluşturan bir bileşiktir. Genelde, iyonik bağlar, hidrojen bağları veya Van der Waals güçleri ile hedef bir proteindeki bağlanma yerine bağlanır. Ligand molekülün bağlanma yerine yanaşması genelde tersinir, yani birleşme ve ayrışma arasında bir denge vardır. Biyolojik sistemlerde bir ligandın hedef molekülü ile tersinmez kovalent bağlanması enderdir. İnorganik kimyadaki ligand tanımından farklı olarak, ligandın mutlaka bir metale bağlanması şart değildir. Sinyal reseptörlerine bir ligand bağlanınca reseptör proteinin üç boyutlu şekli değişebilir, bu da onun işlevsel özelliğini değiştirir. Bağlanma eğilimi veya gücüne "afinite" denir. Ligand tipleri arasında substratlar, inhibitörler, aktivatörler ve nörotransmitterler sayılabilir. Radyoligandlar, radyoizotopla işaretlenmiş bileşiklerdir, ligand bağlanma ölçümlerinde kullanılırlar.
Kimyada dişlilik, bir koordinasyon kompleksindeki merkezî metale bağ kurmuş ligand atomlarının sayısıdır.
Lewis asiti Lewis bazıyla Lewis eklenme ürününü oluşturmak için etkileşen kimyasal türdür. Lewis bazı, Lewis eklenme ürününü oluşturmak için, Lewis asidine elektron çifti veren türdür. Örneğin, OH− ve NH3 Lewis bazlarıdır çünkü bu iyonlar bağ yapmamamış elektron çiftlerini verebilirler. Eklenme ürününde, Lewis asidi ve bazı Lewis bazından gelen elektron çiftini paylaşır. Lewis asit ve bazının isim babası Gilbert N. Lewis'dir.

Kalay(II) klorür ya da stanit klorür, SnCl2 formülüne sahip, beyaz kristal halinde bir katıdır. Kararlı bir dihidrat oluşturur, ancak sulu çözeltileri, özellikle sıcaksa, hidrolize uğrama eğilimindedir. SnCl2 yaygın bir şekilde indirgeyici madde (bir asit çözeltisi içinde) olarak ve kalay kaplamada elektrolitik banyolarda kullanılır. Kalay (II) klorür, diğer kalay klorür (kalay(IV) klorür (SnCl4) ile karıştırılmamalıdır.
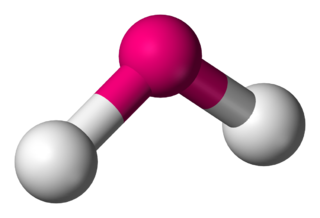
Kimyada, " açısal" ya da "bükülmüş" terimi bazı moleküllere moleküler geometrilerini tanımlamak için kullanılabilir. Oksijen gibi bazı atomlar, Elektron dizilimi nedeniyle hemen hemen her zaman iki (veya daha fazla) kovalent bağını doğrusal olmayan yönlerde ayarlarlar. Su (H2O), analoglarının yanı sıra açısal bir molekül örneğidir. İki hidrojen atomu arasındaki bağ açısı yaklaşık olarak 104,45°'dir. Doğrusal olmayan geometri genel olarak sadece ana grup elementleri içeren diğer üç atomlu molekülleri ve iyonlar için gözlemlenir, belirgin örnekler: Azot dioksit (NO2), kükürt diklorür (SCL2) ve metilen (CH2).
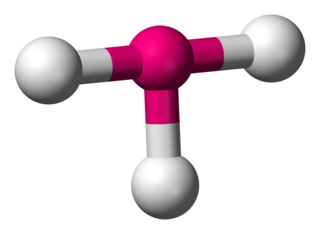
Kimyada, T-şeklindeki moleküler geometri, merkezi bir atomun üç liganda sahip olduğu bazı moleküllerin yapılarını açıklar. Normalde, üç koordineli bileşikler üçgen düzlemsel veya piramidal geometrileri kullanır. T-şekilli moleküllerin örnekleri arasında, halojen triflorürler vardır, örneğin ClF3.
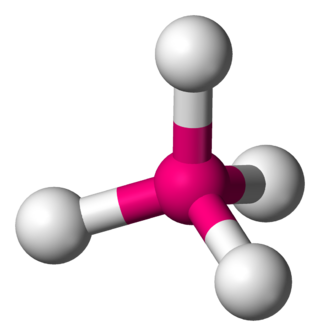
Dörtyüzlü veya tetrahedral molekül geometrisi, merkezi atomun, dört yüzlünün ortasında, dört köşede ise sübstitüentlerin yer aldığı molekül geometrisidir. Bağ açıları, dört sübstitüent aynı olduğunda (örn. metan CH4 ya da daha ağır analogları) cos−1 (-⅓) = 109,4712206 ...° ≈ 109.5° olur. Metan veya diğer simetrik yüzlü moleküller Td nokta grubuna aittir, ama dörtyüzlü moleküller genellikle düşük simetriye sahiptir. Tetrahedral moleküller kiral olabilir.

Kimyada, oktahedral moleküler geometri, bir oktahedronun köşelerini tanımlayan, merkezi bir atom etrafında simetrik olarak düzenlenmiş altı atomlu bileşiklerin veya atom gruplarının veya ligandların şeklini tanımlar. Oktahedronun sekiz yüzü vardır, dolayısıyla octa ön ekini alır. Oktahedron, Platonik katılardan biridir, ancak oktahedral moleküller tipik olarak merkezlerinde bir atom içerir ve ligand atomları arasında bağ yoktur. Mükemmel bir oktahedron Oh nokta grubuna aittir. Oktahedral bileşiklerin örnekleri arasında kükürt hekzaflorür SF6 ve molibden hekzakarbonil Mo (CO)6 gösterilebilir. "Oktahedral" terimi, kimyagerler tarafından, merkezi atoma olan bağların geometrisine odaklanarak ve ligandların kendi aralarındaki farklılıkları dikkate almadan biraz gevşek bir şekilde kullanılır. Örneğin, N-H bağlarının oryantasyonu nedeniyle matematiksel anlamda oktahedral olmayan [Co(NH3)6]3+, oktahedral olarak adlandırılır.
Koordinasyon geometrisi, merkezî atom etrafındaki atomlar tarafından tanımlanan geometrik modeldir. Terim, çeşitli yapıların gözlendiği inorganik kimya alanında yaygın olarak kullanılır. Koordinasyon geometrisi, metal merkezine bağlı ligandların türüne değil sayısına ve konumlarına bağlıdır. Bağlanan atomların sayısı koordinasyon numarasıdır. Geometrik desen, çokyüzlünün köşelerinin ligandlardaki koordine eden atomların merkezleri olduğu bir çokyüzlü olarak tanımlanabilir.















