
Helyum, sembolü He ve atom numarası 2 olan kimyasal element. Periyodik cetvelin birinci periyot 8A grubunda yer alan bir gazdır. Kokusuz, renksiz bir gazdır ve yanmaz.

Elektron, eksi bir temel elektrik yüküne sahip bir atomaltı parçacıktır. Lepton parçacık ailesinin ilk nesline aittir ve bileşenleri ya da bilinen bir alt yapıları olmadığından genellikle temel parçacıklar olarak düşünülürler. Kütleleri, protonların yaklaşık olarak 1/1836'sı kadardır. Kuantum mekaniği özellikleri arasında, indirgenmiş Planck sabiti (ħ) biriminde ifade edilen, yarım tam sayı değerinde içsel bir açısal momentum (spin) vardır. Fermiyon olmasından ötürü, Pauli dışarlama ilkesi gereğince iki elektron aynı kuantum durumunda bulunamaz. Temel parçacıkların tamamı gibi hem parçacık hem dalga özelliklerini gösterir ve bu sayede diğer parçacıklarla çarpışabilir ya da kırınabilirler.

Soy gaz veya asal gaz, standart şartlar altında her biri, diğer elementlere kıyasla daha düşük kimyasal reaktifliğe sahip, kokusuz, renksiz, tek atomlu gaz olan kimyasal element grubudur. Helyum (He), neon (Ne), argon (Ar), kripton (Kr), ksenon (Xe) ve radon (Rn) doğal olarak bulunan altı soy gazdır ve tamamı ametaldir. Her biri periyodik tablonun sırasıyla ilk altı periyodunda, 18. grubunda (8A) yer alır. Grupta yer alan oganesson (Og) için ise önceleri soy gaz olabileceği ihtimali üzerinde durulsa da günümüzde metalik görünümlü reaktif bir katı olduğu öngörülmektedir.

Bir fizik terimi olarak maddenin hâli, maddenin aldığı farklı fazlardır. Günlük hayatta maddenin dört farklı hâl aldığı görülür. Bunlar; katı, sıvı, gaz ve plazmadır. Maddenin başka hâlleri de bilinir. Örneğin; Bose-Einstein yoğunlaşması ve nötron-dejeneje maddesi. Fakat bu hâller olağanüstü durumlarda gerçekleşir, çok soğuk ya da çok yoğun maddelerde. Maddenin diğer hâllerininde, örneğin quark-gluon plazmalar, mümkün olduğuna inanılır fakat şu an sadece teorik olarak bilinir. Tarihsel olarak, maddenin özelliklerindeki niteleyici farklılıklara dayanarak ayrım yapılır. Katı hâldeki madde bileşen parçaları ile bir arada tutulur ve böylece sabit hacim ve şeklini korur. Sıvı hâldeki madde hacmini korur fakat bulunduğu kabın şeklini alır. Bu parçalar bir arada tutulur ama hareketleri serbesttir. Gaz hâlindeki madde ise hem hacim olarak hem de şekil olarak bulunduğu kaba ayak uydurur.Bu parçalar ne beraber ne de sabit bir yerde tutulur. Maddenin plazma hâli ise, nötr atomlarda dahil, hacim ve şekil olarak tutarsızdır. Serbestçe ilerleyen önemli sayıda iyon ve elektron içerirler. Plazma, evrende maddenin en yaygın şekilde görülen hâlidir.

Lityum, sembolü Li atom numarası 3 olan kimyasal elementtir. Periyodik tabloda 1. grupta alkali metal olarak bulunur ve yoğunluğu en düşük olan metaldir. Lityum, yüksek reaktifliğinden dolayı doğada saf hâlde bulunmaz. Yumuşak ve gümüşümsü beyaz metaldir. Havada bulunan oksijenle reaksiyona giren lityum, lityum oksit (Li2O) oluşturur. Bu oksitlenme reaksiyonunu engellemek için yağ içinde saklanır. Hava ve su tarafından hızlı bir şekilde oksitlenip kararır ve lekelenir. Lityum metali doldurulabilir pillerde (örnek olarak cep telefonu ve kamera pili) ve ağırlığa yüksek direniş göstermesi sebebiyle alaşım olarak hava taşıtlarında kullanılır. Li+ iyonunun nörolojik etkilerinden dolayı, lityumlu bileşikler farmakolojik olarak sakinleştiricilerde kullanılır.

Bir lityum-iyon veya Li-iyon pil, enerji depolamak için lityum iyonlarının tersine çevrilebilir indirgemesini kullanan şarj edilebilir pil türüdür. Geleneksel lityum iyon pilinin anodu genelde karbon'dan yapılan grafit'tir. Katot genellikle metal oksit'tir. Elektrolit genelde bir organik çözücü içindeki lityum tuz'udur.
Ksenon, Xe sembolü ile gösterilen 54 atom numaralı kimyasal elementtir. Renksiz, ağır, kokusuz bir soy gaz olan ksenon Dünya atmosferinde eser miktarda bulunur. Genellikle reaktif olmayan element, sentezlenen ilk soy gaz bileşiği olan ksenon heksafloroplatinatın oluşumu gibi birkaç kimyasal reaksiyona maruz kalabilir.

Karanlık madde, astrofizikte, elektromanyetik dalgalarla etkileşime girmeyen, varlığı yalnız diğer maddeler üzerindeki kütleçekimsel etkisi ile belirlenebilen varsayımsal maddelere denir. Karanlık maddelerin varlığını belirlemek için gök adaların döngüsel hızlarından, gök adaların diğer gök adalar içerisindeki yörüngesel hızlarından, geri planda yer alan maddelere uyguladığı kütleçekimsel mercekleme özelliğinden ve gök adaların içerisindeki sıcak gazların sıcaklık dağılımından yararlanılır. İncelemeler, gök adalarda, gök ada gruplarında ve Evren'de, görülebilen maddelerden çok daha fazla karanlık madde olduğunu göstermektedir. Karanlık maddelerin bileşenleri tamamen bilinmemekle birlikte, WIMP'ler, aksiyonlar, sıradan ve ağır nötrinolar, gezegenler ve sönmüş yıldızlarla birlikte verilen isim MACHO'lar ile ışıma yapmayan gaz bulutlarından oluşur.

Mutlak sıfır, bir maddenin moleküllerinin entalpi ve entropisinin teorik minimum değerine ulaştığı termodinamik sıcaklık ölçeğinin en alt sınırıdır. Teorik sıcaklık, ideal gaz yasasının ekstrapolasyonu ile hesaplanmıştır. Uluslararası uzlaşı neticesinde, mutlak sıfır Celsius ölçeğinde −273.15 derece, Fahrenheit ölçeğinde −459.67 derece, Kelvin ve Rankine ölçeklerinde de 0 derece olarak alınmıştır.

Plazma, gaz hâldeki maddelerin manyetik kutuplaştırmaya bağlı doğrusal noktalarda oluşan fiziksel ve kimyasal tepkimenin kontrollü etkileşim sürecine verilen genel ad. Daha kolay bir tanımla; atomun elektronlardan arınmış hâlidir.

proton-proton (pp) zincir reaksiyonu, yıldızların hidrojeni helyuma dönüştürdüğü bilinen iki nükleer füzyon reaksiyonu setinden biridir. Güneş kütlesine eşit veya daha az kütleli yıldızlarda egemendir. Bilinen diğer reaksiyon CNO döngüsüdür. CNO, daha çok güneş kütlesinin yaklaşık 1.3 katından daha büyük kütlelere sahip yıldızlarda hakim olabilen reaksiyonlardır.
Etan, C2H6 formülüne sahip bir bileşiktir. Alkanların ikinci en küçük molekülü olan etan, normal sıcaklık ve basınçta kokusuz ve renksiz bir gazdır. Etan, doğalgazda metandan sonra en fazla bulunan ikinci gazdır.

David Lee Morris "helyum-3 süperakışkanlık buluşları için" Robert C. Richardson ve Douglas Osheroff ile Fizik 1996 Nobel Ödülü'nü kazanan Amerikalı fizikçi.

Walter Kohn, John A. Pople ile birlikte 1998 Nobel Kimya Ödülü sahibi Yahudi kökenli Amerikalı fizikçi. Walter Kohn ve John Pople bu ödülü kuantum kimyası üzerine bir birlerinden bağımsız olarak yaptıkları çalışmalar üzerine almaya hak kazanmışlardır. Kohn özelde bu ödülü Atomlar arasındaki kimyasal bağları açıklamak üzere karmaşık matematiği kuantum mekaniğine uygulayarak geliştirdiği yoğunluk fonksiyonları teorisi sayesinde kazanmıştır.
Helyum hidrür iyonu ya da hidrohelyum(1+) katyonu, HeH+, bir protonun gaz hâlindeki bir helyum atomu ile reaksiyona girmesi sonunda oluşan pozitif yüklü bir iyondur. İlk olarak 1925'te keşfedildi ve moleküler hidrojen ile izoelektroniktir. 177,8 kJ/mol proton ilgisi ile bilinen en güçlü asittir. Bu iyon aynı zamanda Helyum hidrür moleküler iyonu olarak da anılır. Doğal olarak yıldızlararası maddede bulunduğu öne sürülmüştür. En basit heteronükleer iyondur ve hidrojen moleküler iyon, H+2 ile karşılaştırılabilir. Ancak H+2'den farklı olarak, spectroskopik karakterizasyonunu kolaylaştıran kalıcı moleküler kutuplaşması vardır.

Süperakışkanlık maddenin sıfır akmazlığa sahip bir akışkan gibi davrandığı hâlidir. Bu fenomen ilk olarak sıvı helyum ile keşfedildiyse de yalnızca sıvı helyum teorisinde değil aynı zamanda astrofizik, yüksek enerji fiziği ve kuantum kütleçekimi teorilerinde de uygulama alanına girmiştir. Bu fenomen Bose-Einstein yoğunlaşması ile bağıntılıdır ancak özdeş değildir: Bütün Bose-Einstein yoğuşukları süperakışkan olmadığı gibi bütün süperakışkanlar da Bose-Einstein yoğuşuğu değildir.
Standart solar model (SSM), güneşi küresel bir gaz topu olarak ele alan matematiksel bir yaklaşımdır. Teknik olarak simetrik küresel durağanımsı bir yıldız modeli olan bu model, yıldızsal yapıyı tarif eden basit fizik prensiplerinden elde edilmiş birçok diferansiyel denkleme sahiptir. Bu model, güneşin ışıklılığı, çapı, yaşı ve bileşenleri gibi iyi bilinen sınır koşullara bağlıdır. Güneş'in yaşı direkt olarak ölçülemez. Tahmini bir değer bulmanın yollarından biri en eski meteorların yaşını bulmak ve Güneş sisteminin gelişim modellerine bakmaktır. Günümüzdeki Güneş'in fotosferinin yapısı %74,9 oranında hidrojen ve %23.8 oranında helyumdan oluşmaktadır. Astronomide metaller denilen tüm ağır elementler ise %2den daha az bir kütleye tekabül etmektedir. Standart solar model yıldızsal gelişim teorisinin doğruluğunu test etmek için kullanılmaktadır. Aslında, iki serbest parametre olan helyum mevcudiyeti ve karışma uzunluğu değerlerini bulmanın tek yolu SSMyi gözlemlenen güneşe "uygun" hale getirecek şekilde ayarlamaktır.
Süperakışkan Helyum-4, helyum elementi helyum-4 ün oluşturduğu bir süper akışkandır. Bir süperakışkan maddenin 0 viskoziteli bir akışkan gibi davrandığı durumudur. Normal bir sıvı gibi görünen madde her tür yüzeyde sürtünmesiz şekilde engellerin etrafından dolaşır ve kabının gözeneklerinden yalnızca kendi eylemsizliğine bağlı olarak akar.
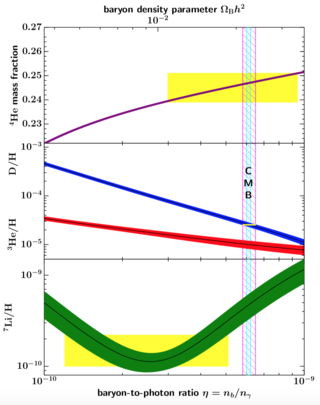
Astronomide, lityum sorunu veya lityum tutarsızlığı, galaksimizdeki metal açısından fakir halo yıldızlarının gözlemlerinden anlaşılan lityumun ilkel bolluğu ile Big Bang nükleosentezi + WMAP, CMB'nın(Kozmik Mikrodalga Arkaalan Işınımı kozmik baryon yoğunluğu tahminleri nedeniyle teorik olarak var olması gereken miktar arasındaki tutarsızlığı ifade eder. Yani, Big Bang'in en yaygın kabul gören modelleri, ilkel lityumun, özellikle 7Li'nin üç katı kadar var olması gerektiğini öne sürüyor. Bu, tahminlerle tutarlı olan hidrojen ve helyum izotoplarının gözlenen bolluğuyla çelişir. Tutarsızlık, bu ilkel bollukları standart BBN tahminlerinden kozmik baryon içeriğinin bir fonksiyonu olarak tasvir eden, astrofizikçi David Schramm'ın onuruna adlandırılan sözde "Schramm planı" ile vurgulanmıştır.
Metalik hidrojen, hidrojenin iletken gibi davrandığı bir fazdır. Bu faz 1935 yılında Eugene Wigner ve Hillard Bell Huntington tarafından teorik olarak öngörülmüştür.













