Langmuir adsorpsiyon modeli
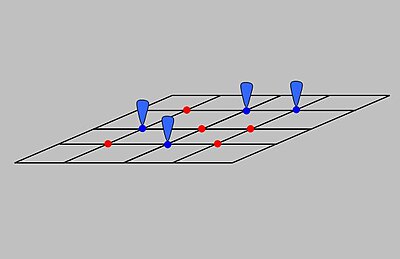
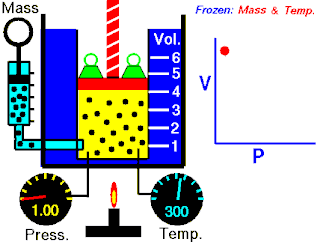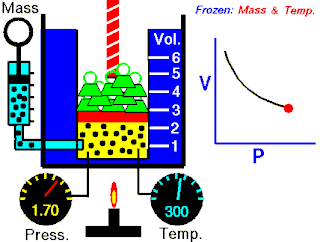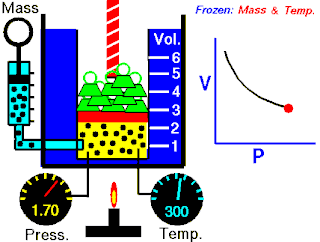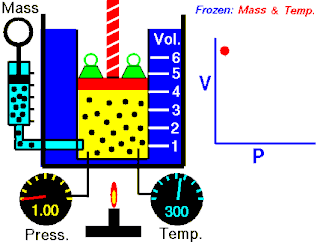
Langmuir adsorpsiyon modeli, bir adsorbatın izotermal koşullarda ideal bir gaz olarak davrandığını varsayarak adsorpsiyonu açıklar. Modele göre adsorpsiyon ve desorpsiyon tersinir işlemlerdir. Bu model, bu koşullar altında katı biradsorban üzerine absorbe edilen hacmine, V, bağlı olan kısmi adsorbatın kısmi basıncını, bile açıklar. Şekilde gösterildiği gibi, adsorbanın, adsorbatları bağlayabilen bir dizi farklı bölgeden oluşan ideal bir katı yüzey olduğu varsayılır. Adsorbat bağlanması, adsorbat gazlı molekül ve boş bir sorpsiyon sahası, S arasında bir kimyasal reaksiyon olarak işlenir. Bu reaksiyon, ilişkili bir denge sabiti ile ile adsorbe edilmiş bir tür ile sonuçlanır.
Bu temel hipotezlerden, Langmuir adsorpsiyon izoterminin matematiksel formülasyonu çeşitli bağımsız ve tamamlayıcı yollarla türetilebilir: sırasıyla kinetik, termodinamik ve istatistiksel mekanik yaklaşımlarla (farklı gösterimler için aşağıya bakınız).
Langmuir adsorpsiyon denklemi aşağıdaki gibidir:
adsorpsiyon bölgelerinin fraksiyonel doluluktaki alanlarıdır, örneğin katı üzerine adsorbe edilen gazın hacmi V'nin 'ye oranında, bir gaz molekülünün hacmi, katının tüm yüzeyini kaplayan ve adsorbat tarafından tamamen işgal edilen tek tabakadır. Homojen, düz bir katı yüzeyi kaplayan sürekli bir tek tabakalı adsorbat molekülleri, bu adsorpsiyon modelinin kavramsal temelidir.[1]
Arka plan ve deneyler
1916'da Irving Langmuir, türlerin basit yüzeylere adsorpsiyonuna ilişkin modelini sundu. Langmuir, yüzey kimyası ile ilgili çalışmaları nedeniyle 1932'de Nobel Ödülü'ne layık görüldü. Belirli bir yüzeyin fiziksel emilim veya kemisorpsiyon yoluyla bir türün "yapışabileceği" belirli sayıda eşdeğer bölgeye sahip olduğunu varsaydı. Teorisi, gaz moleküllerinin bir yüzeyden elastik olarak geri dönmediğini, ancak katı cisimlerdeki molekül gruplarına benzer şekilde onun tarafından tutulduğunu varsaymasıyla başladı.[2]
Langmuir, adsorbe edilmiş filmlerin kalınlık olarak bir molekülü aşmadığı varsayımını doğrulayan iki makale yayınladı. İlk deney, gazlardaki ısıtılmış filamentlerden elektron emisyonunun gözlemlenmesini içeriyordu.[3] İkincisi, daha doğrudan bir kanıt, sıvı filmlerini bir adsorban yüzey tabakası üzerinde incelemeyi ve ölçmeyi içeriyordu. Ayrıca yüzey ve adsorbe edilmiş maddenin birinci tabakası arasındaki çekici kuvvetin, birinci ve ikinci tabaka arasındaki kuvvetten çok daha büyük olduğunu da kaydetti. Bununla birlikte, doğru sıcaklık ve basınç kombinasyonu ile sonraki katmanların yoğunlaşabileceği durumları da kaydetti.[4]
Modelin temel hipotezleri
Bu modelin doğasında var olan aşağıdaki hipotezler[5] özellikle en basit durum için geçerlidir: tek bir adsorbatın katının yüzeyindeki bir dizi eşdeğer alan üzerine adsorpsiyonu.
- Adsorbe bölgelerini içeren yüzey, oluksuz tamamen düz bir düzlemdir (yüzeyin homojen olduğu varsayılmalıdır). Bununla birlikte, kimyasal olarak heterojen yüzeyler, adsorbat yüzey üzerinde sadece bir tip fonksiyonel gruba bağlıysa homojen olarak kabul edilebilir.
- Adsorbe edici gaz, hareketsiz bir duruma adsorbe olur.
- Tüm alanlar enerjisel olarak eşdeğerdir ve adsorpsiyon enerjisi tüm alanlar için eşittir.
- Her bölge en fazla bir A molekülünü tutabilir (yalnızca tek katmanlı kapsama alanı).
- Bitişik bölgelerdeki adsorbat molekülleri arasında etkileşim yoktur (veya ideal etkileşim yoktur). Etkileşimler ideal olduğunda, yan yana etkileşimlerin enerjisi, yüzey doluluğuna bakılmaksızın tüm alanlar için eşittir.
Ayrıca bakınız
- Hill denklemi (biyokimya)
- Michaelis-Menten kinetiği (aynı matematiksel forma sahip denklem)
- Monod denklemi (aynı matematiksel forma sahip denklem)
- Yüzeylerdeki reaksiyonlar
Kaynakça
- ^ Hanaor (2014). "Scalable Surface Area Characterization by Electrokinetic Analysis of Complex Anion Adsorption" (PDF). Langmuir. 30 (50): 15143-15152. doi:10.1021/la503581e. PMID 25495551. 17 Mayıs 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 18 Kasım 2020.
- ^ Langmuir (Haziran 1918). "The Adsorption of Gases on Plane Surface of Glass, Mica and Platinum". Journal of the American Chemical Society. 40 (9): 1361-1402. doi:10.1021/ja02242a004. 18 Ağustos 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Kasım 2020.
- ^ Langmuir (1916). "Part I". The Research Laboratory of the General Electric Company: 2221.
- ^ Langmuir (1918). "Part II". The Research Laboratory of the General Electric Company: 1848.
- ^ Principles of Adsorption and Reaction on Solid Surfaces. Wiley Interscience. 1996. s. 240. ISBN 978-0-471-30392-3.
- Katı ve sıvıların yapısı ve temel özellikleri. bölüm i. katılar. Irving Langmuir; J. Am. Chem. Soc. 38, 2221-95 1916