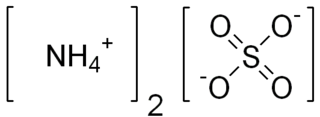Kimyada, sülfür terimi -2 yükseltgenme seviyesinde kükürt içeren kimyasal bileşiklerin birkaç tipi için kullanılır.

Kükürt, simgesi S, atom numarası 16 olan, limon sarısında ametal, yalın katı bir elementtir.
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.

Asit yağmuru, asidik kimyasalların yağmur, kar, sis, çiy veya kuru parçacıklar hâlinde yeryüzüne düşmesine verilen isimdir.

Sülfürik(VI) asit ya da halk arasında bilinen ismi ile zaç yağı, H2SO4, güçlü bir mineral asididir. Olası kâşifi 8. yüzyıl simyacısı Cabir bin Hayyan tarafından yenime uğratıcı, renksiz ve yoğunluğu yüksek sıvı olarak tanımlanmıştır. Suda her konsantrasyonda çözünebilir. Büyük ölçüde korozif oluşu, güçlü asidik yapısından ve dehidrasyon özelliğinden kaynaklanmaktadır.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Kükürt trioksit, suyla tepkimeye girdiğinde sülfürik asit oluşturan zehirli bir gazdır. Formülü SO3 şeklindedir. Kükürtlü asidi oluşturan sülfit iyonu (SO3 2-) ile karıştırılmamalıdır.

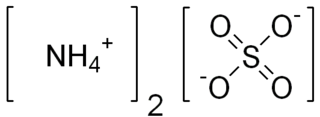
Amonyum sülfat, (NH4)2SO4 formülüne ve çok sayıda ticari kullanıma sahip bir inorganik tuzdur. Toprak gübresi olarak yaygın bir şekilde kullanılır. %21 azot ve %24 kükürt içerir.
Floroantimonik asit (HSbF6) hidrojen florür ve antimon pentaflorürün farklı oranlardaki karışımıdır. Bu karışımlardan 1:1 kombinasyonu, bilinen en güçlü süperasit formunu oluşturur. Öyle ki, bu form, hidrokarbonları iyonize ederek karbokatyonlar ve H2 oluşturabilmektedir.

Genellikle metabisülfit olarak bilinen bir disülfit, disülfit iyonu (metabisülfit iyonu) [S2O5]−2 içeren bir kimyasal bileşiktir.
Bir asidin kuvveti, onun içinde bulunduğu çözeltiye ne kadar proton (H+) verebildiğinin ölçüsüdür. Kuvvetli asitler %100 çözünürler ve bu çözünme iyonlaşarak gerçekleşir. Yani 1 mol HA kuvvetli asidi suda çözündüğünde 1 mol H+ ve onun eşlenik bazı A- 1 mol oluşur. Hidroklorik asit, hidroiyodik asit, hidrobromik asit, perklorik asit, nitrik asit ve sülfürik asit, kuvvetli asitlere örnektir.
Protonasyon, protonlanma veya protonlaşma; bir atom, molekül veya iyona proton (H+) eklenerek konjuge asidin oluşturulmasıdır. Bazı örnekleri:
- suyun sülfürik asit tarafından protonasyonu:
- H2SO4 + H2O
 H3O+ + HSO-4
H3O+ + HSO-4
- Karbokatyon oluşumunda izobütenin protonasyonu:
- (CH3)2C=CH2 + HBF4
 (CH3)3C+ + BF-4
(CH3)3C+ + BF-4
- Amonyak ve hidrojen klorür reaksiyonundan amonyum klorür oluşumunda amonyakın protonasyonu:
- NH3(g) + HCl(g) → NH4Cl(s)

Hidrojen bromür, HBr formülüne sahip iki atomlu moleküldür. Renksiz bir bileşik ve bir hidrojen halojenürdür. Hidrobromik asit, su içinde bir HBr çözeltisidir. Hem HBr'nin susuz hem de sulu çözeltileri, bromür bileşiklerinin hazırlanmasında ortak reaktiflerdir.

Arsenöz asit (veya arsenik oksit), H3AsO3 formülüne sahip bir inorganik bileşiktir. Sulu çözeltilerde meydana geldiği bilinmektedir, ancak bu gerçek As(OH)3'ün öneminden uzaklaşmasa da saf bir malzeme olarak izole edilmemiştir.
Permanganik asit, HMnO4 formülüne sahip bir inorganik bileşiktir. Bu güçlü oksoasit, dihidrat olarak izole edilmiştir. Permanganat tuzlarının konjugat asididir. Çok az sayıda yayın konusu olup, karakterizasyonu ve kullanımları çok sınırlıdır.

Disülfürik asit veya pirosülfürik asit, kükürtün bir oksoasitidir. Oleumun önemli bir bileşenidir ve çoğu kimyager bu şekilde karşılaşır. Aynı zamanda, dengeye bağlı olarak sıvı susuz sülfürik asidin küçük bir bileşenidir:
- H2SO4 ⇌ H2O + SO3
- SO3 + H2SO4 ⇌ H2S2O7

Bromöz asit, HBrO2 formülüne sahip bir inorganik bileşiktir. Konjugat bazının -bromitlerinin- tuzları izole edilmiş olmasına rağmen, kararsız bir bileşiktir. Asidik çözeltide, bromitler broma ayrışır.

Tellürik asit, Te(OH)6 formülüne sahip kimyasal bir bileşiktir. Sulu çözelti içinde devam eden oktahedral Te(OH)6 moleküllerinden oluşan beyaz bir katıdır. Rombohedral ve monoklinik olmak üzere iki formu vardır ve her ikisi de oktahedral Te(OH)6 molekülleri içerir. Tellürik asit, güçlü bazlara sahip tellürat tuzları ve zayıf bazlara sahip hidrojen tellürat tuzları veya sudaki tellüratların hidrolizi üzerine dibazik olan zayıf bir asittir.
Poliprotik asit terimi, molekül başına birden fazla proton sağlayabilen asitleri tanımlamak için kullanılır.