Koligatif özellikler
Kimyada, koligatif özellikler, çözünen parçacıkların sayısının, mevcut kimyasal türlerin doğasına değil, bir çözelti içindeki çözücü moleküllerinin sayısına oranına bağlı olan çözeltilerin özellikleridir.[1] Sayı oranı, örneğin molarite, molalite, normallik (kimya) vb. çözeltilerin konsantrasyonu için çeşitli birimlerle ilişkili olabilir. Çözelti özelliklerinin çözünen parçacıkların doğasından bağımsız olduğu varsayımı sadece ideal çözeltiler için doğrudur ve seyreltik gerçek çözeltiler için yaklaşık değerlerdir. Başka bir deyişle, koligatif özellikler, çözümün ideal olduğunu varsayarak makul bir şekilde yaklaşılabilen bir çözüm özellikleri kümesidir.
Sadece uçucu olmayan çözünenin uçucu bir sıvı çözücüde çözünmesinden kaynaklanan özellikler dikkate alınır.[2] Esas olarak çözünenin varlığı ile değiştirilen çözücü özellikleridir. Çözünen parçacıklar, sıvı fazdaki bazı çözücü moleküllerini değiştirir ve bu nedenle çözücü konsantrasyonunu azaltır, böylece koligatif özellikler çözünenin doğasından bağımsızlaşır. Colligative kelimesi, birbirine bağlı Latince colligatus anlamından türetilmiştir. Bu, tüm koligatif özelliklerin ortak bir özelliğe sahip olduğunu, yani sadece çözünen moleküllerin sayısına göre çözünen moleküllerin sayısına bağlı değiştiğini ve çözünenin doğasına bağlı olmadığını gösterir.[3]
Koligatif özellikleri şunlardır:
- Buhar basıncının göreceli olarak düşürülmesi
- Kaynama noktasının yükselmesi
- Donma noktasının alçalması
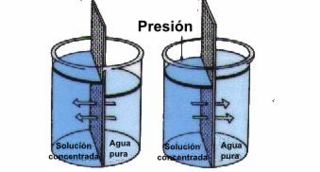
- Ozmotik basınç
Belirli bir çözünen çözücü kütle oranı için, tüm koligatif özellikler çözünen molar kütle ile ters orantılıdır.
Üre veya suda glikoz veya başka bir çözücü gibi iyonize olmayan bir çözünenin seyreltik bir çözeltisi için koligatif özelliklerin ölçülmesi, hem küçük moleküller hem de başka yollarla çalışılamayan polimerler için göreceli molar kütlelerin belirlenmesini sağlayabilir. Alternatif olarak, iyonize çözünenler için Ölçümler, ayrılma yüzdesinin tahmin edilmesine yol açabilir.
Koligatif özellikler çoğunlukla seyreltik çözeltiler için incelenir, davranışları ideal bir çözümün davranışı olarak yaklaştırılabilir. Aslında, yukarıda listelenen tüm özellikler seyreltik limitte sadece koligatiftir: daha yüksek konsantrasyonlarda, donma noktası depresyonu, kaynama noktası yükselmesi, buhar basıncı yükselmesi veya depresyonu ve ozmotik basınç, çözücünün ve çözünenin kimyasal yapısına bağlıdır.[4]
Köken
Koligatif (Latince: co,ligare) kelimesi 1891'de Wilhelm Ostwald tarafından tanıtıldı. Ostwald üç kategoride çözünen özelliklerini sınıflandırdı:[5][6]
- Sadece çözünen konsantrasyona ve sıcaklığa bağlı olan ve çözünen parçacıkların doğasından bağımsız olan kolligatif özellikleri,
- Bileşen parçacıkların özelliklerinin toplamları olan ve bu nedenle çözünenin bileşimine (veya moleküler formülüne) bağlı olan kütle gibi katkı özellikleri,
- Çözünenin moleküler yapısına daha fazla bağlı olan yapısal özellikleri.
Kaynakça
- ^ McQuarrie, Donald, et al. Colligative properties of Solutions" General Chemistry Mill Valley: Library of Congress, 2011. 978-1-89138-960-3.
- ^ KL Kapoor Applications of Thermodynamics Volume 3
- ^ Castellan, Gilbert W. (1983). Physical Chemistry (3.3url=https://books.google.ca/books?id=YI9aDwAAQBAJ&pg=PA281&lpg=PA281&dq=colligative+%22bound+together%22&source=bl&ots=NVWhBv5olx&sig=ACfU3U3ERV5KB6Xct2RwNhLosrPBAur3jA&hl=fr&sa=X&ved=2ahUKEwiXyO2xosPjAhUKhOAKHXRfDgs4ChDoATAAegQIBxAB#v=onepage&q=colligative%20%22bound%20together%22&f=false bas.). Addison-Wesley. s. 281. ISBN 978-0201103861.
- ^ "Arşivlenmiş kopya". 27 Şubat 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Şubat 2020.
- ^ W.B. Jensen, J. Chem. Educ. 75, 679 (1998) Logic, History, and the Chemistry Textbook I. Does Chemistry Have a Logical Structure?
- ^ H.W. Smith, Circulation 21, 808 (1960) THEORY OF SOLUTIONS : A Knowledge of the Laws of Solutions ...