C vitamini veya askorbik asit, suda çözünebilen ve birçok görevi olan vitamin. Çoğu Hayvanlar ve bitkiler, kendi C vitaminlerini glukozdan üretebilirler. İnsanlar, bazı meyve yarasaları, hint domuzu ve insan benzeri primatlar C vitamini üretemediklerinden bunu besinlerden almak zorundadırlar.

Lipit, tüm canlıların yapısında bulunan temel organik bileşiklerden biridir. Lipitler, doymuş ve doymamış yağlar olarak ayrılır. Doymamış yağlar, oda sıcaklığında sıvı hâlde bulunan lipitler; doymuş yağlar ise oda sıcaklığında katı hâlde bulunan lipitlerdir. Biyolojik önemi olan lipitler için yağ asitleri, nötr lipitler (trigliserit), fosfolipitler ve steroitler örnek gösterilebilir. Lipitler, insan ve hayvanların temel besinleri arasında yer alır.

Tuz, kimyada, bir asitle bir bazın tepkimeye girmesi neticesinde meydana gelen maddedir. Tuz, asitteki eksi yüklü iyonla (anyon) bazdaki artı yüklü iyondan (katyon) meydana gelir. Asitle baz arasındaki nötralleşme tepkimesi esnasında tuz ve su açığa çıkar. Erimiş tuz veya çözelti halindeki tuzların çoğu eksi ile artı yüklü iyonlarına ayrışır ve elektriği iletir. Tuz adı ayrıca sofra tuzu veya sodyum klorür (NaCl) için de kullanılır.

Laktik asit, kimyasal formülü C₃H₆O₃ olan organik bir asittir. İzomerik iki formu vardır: L(+) laktik asit ve D(-) laktik asit. Laktik asit, birçok doğal süreçte ve mikroorganizmalar tarafından fermantasyon sırasında üretilir. Bu asit, sütte de doğal olarak bulunur ve bu nedenle "laktik" adını almıştır.

Üre (Latince Urea Pura), organik bir bileşik. Formülü H2N-CO-NH2'dir. Karbonik asidin diamidi olan üre aynı zamanda karbamik asidin de amidi olduğundan karbamid adı ile de bilinir.
Kimya ve biyokimyada, yağ asidi, genelde uzun, alifatik kuyruklu bir karboksilik asittir. Uzun karboksilik yağ asitlerinden 4 karbonlu ve daha uzun zincirlileri yağ asidi olarak sayılır; doğal yağları (trigliseritleri) oluşturan yağ asitlerinden söz ederken ise bunların en az 8 karbonlu olduğu varsayılabilir. Çoğu doğal yağ asitlerinin çift sayılı karbon atomu vardır, çünkü bunların biyolojik sentezlerinde iki karbon atomlu asetat kullanılır.
Safra asitleri, memeli hayvanların safrasında bulunan steroit asitlerdir. Karaciğerde kolesterolun oksidasyonu sonucu oluşurlar, safra kesesinde depolanıp ince bağırsağa salgılanırlar. Surfaktan olarak etki ederler, lipitleri çözüp onların emilmesi ve sindirimine yardım ederler. Taurin ve glisin ile konjuge safra asitleri safra tuzları olarak isimlendirilen artıklar bırakırlar. Çeşitli safra tuzları arasındaki kimyasal farklılıklar çok ufaktır, 3,7,12 pozisyonlarında hidroksil gruplarının olup olmamasıyla birbirlerinden fark ederler.

Hidroklorik asit, hidrojen ve klor elementlerinden oluşan, oda sıcaklığı ve normal basınçta gaz hâlinde olan hidrojen klorürün sulu çözeltisine verilen ad. Halk arasında tuz ruhu olarak da bilinir. 9. yüzyılda simyacı Câbir bin Hayyân tarafından keşfedildi ve sonrasında simya alanında kullanıldı. Sanayi Devrimi sırasında, sanayideki önemi keşfedilen asit, önce Leblanc işlemi, sonrasında Solvay işlemi ile sanayi alanında üretilmeye başladı. Hidroklorik asit, tarihte yeni kolaylıkların keşfinde önemli roller üstlendi. Günümüzde PVC'den demir-çeliğe, organik madde üretiminden gıda sektörüne kadar hemen hemen tüm alanlarda hidroklorik asit kullanılmaktadır.

Asetik asit veya etanoik asit CH3COOH formüllü bir organik asittir, sirkeye ekşi tadını ve keskin kokusunu vermesiyle bilinir. Bu yüzden halk arasında sirke ruhu veya sirke asidi şeklinde de adlandırılır. Karboksilik asitlerin en küçüklerindendir (en küçük olan formik asittir). Doğada karbonhidratların yükseltgenmesiyle oluşur. Sanayide asetik asit hem biyolojik yolla hem de sentetik yolla imal edilir. Tuz ve esterine asetat denir. Suda tamamen çözünür.
Nitrik asit, HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.

Sülfat iyonu, inorganik kimyada bir sülfür atomu ile bunu tetrahedral yapıda çevreleyen dört eş oksijen atomundan oluşan, negatif yüklü bir anyondur. Ampirik formülü SO42- ve moleküler ağırlığı 96,06 daltondur. Hidrojenle birleştiğinde sülfürik asit oluşturur. Ayrıca,Dimetil sülfat gibi organik sülfatlar, kovalent bileşiklerdir ve sülfürik asidin esterleridir.
- Sülfürik asitte metalin eritilmesi
- Sülfürik asidin bir metal hidroksit veya oksit ile reaksiyonu
- Metal sülfür veya sülfitlerin oksidasyonu
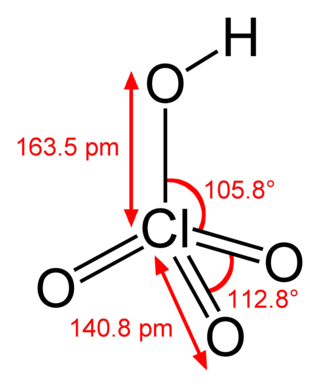
Perklorik asit, HClO4, suda çözünebilen renksiz bir sıvı olan bir klor oksoasididir. Sülfürik asit ya da nitrik asit ile kıyaslanabilecek kadar güçlü bir asittir. Perklorik asit bir süper asittir ancak en güçlü Brønsted-Lowry asidi değildir (en güçlüsü HSbF6 ya da floroantimonik asittir). Asidin pKa'sı −7'dir.

Gerty Theresa Cori, Çek Yahudisi biyokimyacı. Nobel Fizyoloji veya Tıp Ödülü sahibi ilk kadın bilimci.

Peroksidisülfürik asit kimyasal formülü H2S2O8 olan kükürtlü bir oksiasittir. Marshall asidi adı da verilmektedir. Yapısal adlandırmada HO3SOOSO3H olarak yazılabilir. Peroksidisülfürik asidin, niçin sülfatlardan daha yüksek bir yükseltgenme basamağı olduğunu göstermesi +6 yükseltgenme basamağındaki kükürt içermesinden başka, peroksit grubu da içermesinden dolayıdır. Asidin kendisi olmasa da, çoğunlukla persülfat olarak tanınan tuzları sanayi bakımından oldukça önemlidir. Tuzları peroksisülfat iyonu içerir. Bu tuzlar oldukça kuvvetli yükseltgen maddelerdir.

Esansiyel yağ asitleri, insan ve hayvanların yaşamlarını devam ettirebilmesi için dışarıdan alması gereken, vücutta sentezlenemeyen yağ asitleridir. "Esansiyel yağ asidi" terimi solunumda kullanılan yağ asidi için değil, biyolojik faaliyetleri gerçekleştirmek için gerekli olan yağ asitleri için kullanılır.

Asit saldırısı, şiddetli bir saldırı biçimidir. Bu tip saldırılarda hedef çoğunlukla şahsın yüzüdür ve kurban genellikle kadındır. Halk arasında kezzap atma olarak bilinse de aslında asit saldırılarında genelde kezzap değil sülfürik asit kullanılır. Nitrik asidin kullanıldığı vakalar da bulunmaktadır. Nadir olarak hidroklorik asit kullanılsa da sülfürik asit kadar güçlü değildir. Sülfürik asit, kezzaptan çok daha güçlüdür, sülfürik asidin su ile egzotermik bir tepkime vermesi deride üçüncü dereceden yanıklara sebep olmaktadır. Sülfürik asit ile gerçekleştirilen asit saldırılarına vitriolaj denir.

Kloröz asit, HClO2 formülüne sahip bir inorganik bileşiktir. Zayıf bir asittir. Klor, bu asitte +3 oksidasyon durumuna sahiptir. Saf madde dengesiz, hipokloröz aside (Cl oksidasyon hali + 1) ve klorik aside (Cl oksidasyon hali + 5) orantısızdır:
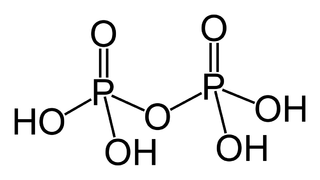
Difosforik asit olarak da bilinen pirofosforik asit, H4P2O7 formülüne sahip inorganik bir bileşik veya daha açıklayıcı olarak [(HO)2P(O)]2O'dur. Renksiz ve kokusuzdur, su, dietil eter ve etil alkolde çözünür. Susuz asit, 54.3 °C ve 71.5 °C'de eriyen iki polimorf içinde kristalleşir. Bileşik, polifosforik asit ve pirofosfat anyonunun konjugat asidinin bir bileşeni olması dışında özel olarak yararlı değildir. Pirofosforik asit anyonları, tuzları ve esterlerine pirofosfatlar denir.

Disülfürik asit veya pirosülfürik asit, kükürtün bir oksoasitidir. Oleumun önemli bir bileşenidir ve çoğu kimyager bu şekilde karşılaşır. Aynı zamanda, dengeye bağlı olarak sıvı susuz sülfürik asidin küçük bir bileşenidir:
- H2SO4 ⇌ H2O + SO3
- SO3 + H2SO4 ⇌ H2S2O7
Karboksilik asitlerden 3C'a sahip olan propiyonik asit içerdiği hidrojen bağları ile güçlü olup kaynama noktası diğer fonksiyonel gruplardan (sırasıyla) Alkol-Keton-Aldehit-Eter büyüktür. Propionik asit CH3CH2CO2H kimyasal formülüne sahip doğal olarak oluşan bir karboksilik asittir. Vücut kokusuna benzeyen keskin ve hoş olmayan bir kokuya sahip bir sıvıdır. CH3CH2CO2− anyonu ile propiyonik asidin tuzları ve esterleri, propiyonatlar veya propanoatlar olarak bilinir.