Sodyum, periyodik cetvelde Na simgesi ile gösterilen ve atom numarası 11 olan element. Sodyum yumuşak ve kaygan bir metal olup alkali metaller grubuna aittir. Doğal bileşiklerin içinde bol miktarda bulunur. Yüksek oranda reaktiftir, sarı bir alevle yanar, su ile şiddetli reaksiyon verir ve havada hızla oksitlenir. Dolayısıyla, vazelin, gazyağı gibi hava ve su ile temasını kesecek bir ortamda saklanması gerekir.
Hidrojen klorür ya da Kloran, HCl formülüne sahip renksiz, zehirli bir gazdır. Hidrojen ve klor elementlerin oluşan inorganik bileşiktir. Havadaki nem ile temasında beyaz hidroklorik asit dumanı oluşturur. Hidroklorik asit, hidrojen klorürün sulu çözeltisine verilen addır.

Çamaşır suyu, genellikle etken madde olarak sodyum hipoklorit (NaClO) içeren ağartma, temizlik ve hijyen amacıyla kullanılan kimyasal maddedir.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.

Kostik ve kostik soda ( ) olarak da bilinen sodyum hidroksit (kostik soda veya sud kostik de denir), NaOH formülüne sahip bir inorganik bileşiktir. Sodyum katyonları Na+ ve hidroksit anyonları OH- içeren beyaz renkli katı bir iyonik bileşiktir.
) olarak da bilinen sodyum hidroksit (kostik soda veya sud kostik de denir), NaOH formülüne sahip bir inorganik bileşiktir. Sodyum katyonları Na+ ve hidroksit anyonları OH- içeren beyaz renkli katı bir iyonik bileşiktir.
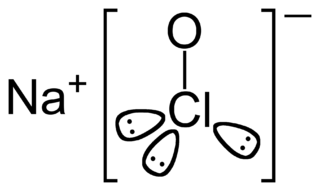
Sodyum hipoklorit, (NaClO) bir tür tuzdur. Günlük hayatta beyazlatıcı çamaşır sularında kullanılmaktadır. Oda koşullarındaki klor ile sabunlardaki sodyum hidroksit tepkimeye sokularak üretilmektedir.
Kalsiyum hipoklorit, Ca(ClO)2 formülüyle gösterilen bir hipoklorit tuzudur. Günlük hayatta su arıtım ve havuz temizleme sistemleri ve sıvı çamaşır suyunda kullanılmaktadır.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.

Baryum klorat formülü Ba(ClO3)2 olanbeyaz kristal yapıya sahip bir kimyasal bileşiktir. Tüm çözünür baryum bileşikleri gibi tahriş edici ve zehirlidir. Klorik asitin baryum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir. Bazen piroteknikte yeşil bir renk üretmek için kullanılır. Klorik asit üretiminde de kullanılır.

Sodyum klorat NaClO3 kimyasal formülüne sahip bir inorganik bileşiktir. Suda kolayca çözünür, beyaz kristal bir tozdur. Higroskopiktir. Sodyum klorat 300 °C’nin üzerinde ayrışarak oksijen ve sodyum klorür ortaya çıkar. Özellikle, çok parlak kâğıt imal etmek için ağartma hamurundaki uygulamalara yönelik olarak yılda birkaç yüz milyon ton üretilmektedir.

Sodyum iyodat, (NaIO3) iyodik asitin sodyum tuzudur. Sodyum iyodat oksitleyici madde olduğundan, yanıcı maddeler ya da indirgeyici maddelerle temas ettiğinde alev almalarına sebep olabilir.
Kimyasal reaktiflik, bir reaksiyonun meydana gelme eğilimiyle ilişkilidir. Kimyasal tepkimelerin gerçekleşmesini belirleyen faktörler termodinamik düzeyinde incelenir. Termodinamik olarak bir reaksiyon eğer tepkimenin ürünleri reaktanlara kıyasla daha düşük serbest enerji düzeyinde ise gerçekleşir. Diğer taraftan Reaktiflik ise genel olarak bir maddenin kimyasal değişikliklere ya da kimyasal tepkimelere girme eğilimine denir. Elementlerin atomik yapısı ve elektronlarının dizilişi elementlerin ve oluşturdukları moleküllerin reaktifliğinde önemli rol oynar. Soygazların örneğin kimyasal olarak çok az reaktiflik gösterdiği belirtilir. Dolayısıyla kimyasal bileşik oluşturmaları zordur. Bu durum soygazların tam dolu olan en dış elektron kabuğundan dolayıdır.
Kimyasal denge, asit ve baz kimyası, elektron aktarımı tepkimesi ve entropi gibi konular kimyasal reaktifliğin temel kavramlarıdır.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.

Sodyum azotür, NaN3 formüllü inorganik bileşiktir. Bu renksiz tuz çoğu araba hava yastığı sisteminde kullanılan gaz oluşturucusudur. Diğer azotür bileşiklerinin hazırlanabilmesi için de kullanılır. İyonik bir maddede olan sodyum azotür, suda oldukça iyi çözünür ve güçlü bir toksiktir.
Benzil klorür, C
6H
5CH
2Cl formüllü organik bileşik. Kimyasal tepkimelerde çokça kullanılan renksiz sıvı. Kaynama noktası 179 °C'dir. Suda çözünmez. Etanol, dietil eter, kloroform ve karbon tetraklorürde çözünür.

Sodyum fenolat (sodyum fenoksit) NaOC6H5 formülüne sahip bir organik bileşiktir. Beyaz kristalimsi bir katıdır. Aynı zamanda fenoksit olarak da bilinen fenolat anyonu, fenolün konjuge bazıdır. Aril eterler gibi diğer birçok organik bileşiğin öncül maddesi olarak kullanılır.

Baryum klorür, BaCl2 formüllü inorganik bir bileşik'tir. Bu bileşik baryum'un suda-çözünen en yaygın tuzlarından biridir. Diğer baryum tuzlarının çoğu gibi, baryum klorür beyaz toz halinde ve zehirlidir. Alevde sarı-yeşil renk verir. Ayrıca higroskopiktir, ilk önce dihidrat BaCl2(H2O)2' ye dönüşür.

Klor triflorür, formülü ClF3 olan interhalojen bir bileşiktir. Zehirli, aşındırıcı ve aşırı reaktiftir. Gaz hâlindeyken renksizken sıvı hâlindeyken solgun yeşilimsi sarı renktedir. Yarı iletken sanayiinde, nükleer yakıtların yeniden işlenmesinde, roket itici yakıtlarında ve diğer endüstriyel alanlarda kullanılır. Benzen, toluen, eter, alkol, asetik asit, hekzan gibi çözücüler ile reaksiyona girer. Karbon tetraklorürde çözünür ancak yüksek konsantrasyonlarda patlayıcı olabilir.
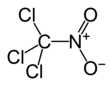
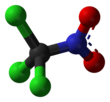
Nitrometan, bazen basitçe "nitro" olarak adlandırılan ve kimyasal formülü CH3NO2 olan bir organik bileşiktir. En basit organik nitro bileşiğidir. Ekstraksiyonlar, reaksiyon ortamı ve temizleme solventi gibi çeşitli endüstriyel uygulamalarda çözücü olarak yaygın bir şekilde kullanılan polar bir sıvıdır. Organik sentezde bir ara ürün olarak pestisit, patlayıcı, lif ve kaplama üretiminde yaygın olarak kullanılır. Nitrometan çeşitli Tap Fuel kalkış yarışı gibi motor sporlarında ve Radyo-kontrollü uçaklarda, tel kumanda kontrollü ve serbest uçuş model uçaklardaki minyatür içten yanmalı motorlarda yakıt katkı maddesi olarak kullanılır.
1,1-Dikloroetilen (1,1-DCE) veya viniliden klorür, C
2H
2Cl
2 moleküler formülüne sahip bir organoklorürdür. Keskin bir kokuya sahip renksiz bir sıvıdır. Çoğu klorokarbon gibi suda az çözünür, ancak organik çözücülerde çözünür. 1,1-DCE, gıda kullanımları için streç film Saran'ın öncüsüydü, ancak bu uygulama aşamalı olarak kaldırıldı.