Kurşun (Pb) atom numarası 82, atom kütlesi 207,19 olan mavi-gümüş rengi karışımı bir elementtir. 327,5 °C'ta erir ve 1740 °C'ta kaynar. Doğada, kütle numaraları 208, 206, 207 ve 204 olmak üzere 4 kararlı izotopu vardır.

Tuz, kimyada, bir asitle bir bazın tepkimeye girmesi neticesinde meydana gelen maddedir. Tuz, asitteki eksi yüklü iyonla (anyon) bazdaki artı yüklü iyondan (katyon) meydana gelir. Asitle baz arasındaki nötralleşme tepkimesi esnasında tuz ve su açığa çıkar. Erimiş tuz veya çözelti halindeki tuzların çoğu eksi ile artı yüklü iyonlarına ayrışır ve elektriği iletir. Tuz adı ayrıca sofra tuzu veya sodyum klorür (NaCl) için de kullanılır.

Kimyasal bileşik, kimyasal bağlarla bir arada tutulan birden fazla kimyasal elementin atomlarını içeren birçok özdeş molekülden oluşan kimyasal maddedir. Dolayısıyla tek bir elementin atomlarından oluşan bir molekül bileşik değildir. Bir bileşik, diğer maddelerle etkileşimi içerebilen kimyasal reaksiyonla farklı bir maddeye dönüştürülebilir. Bu süreçte atomlar arasındaki bağlar kırılabilir ve/veya yeni bağlar oluşabilir.

İnorganik, organik olmayan anlamına gelir. Biyolojide su, mineral, asit, baz, tuzlar gibi canlıların yapısında bulunan ancak canlı olmayan veya bir canlı tarafından üretilmemiş bileşiklerdir. Kimyada inorganik bileşikler, sıklıkla karbon taşımayan moleküllerdir. Bunlara örnek olarak da, anyonlar veya katyonlar olarak sınıflandırılan çeşitli iyonik bileşikler ile kovalent bileşikleri verilebilir. Birçoğu iyonlardan meydana gelmiş olsa da kovalent bağlı inorganik bileşikler de bulunur. Karbon disülfür, karbonmonoksit ve siyanürler gibi karbon bileşikleri inorganik olarak kabul edilir.

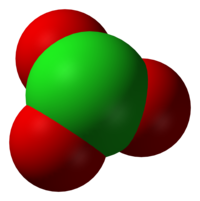
Klorik asit (HClO3), klorun bir oksoasiti ve klorat tuzlarının formal öncülüdür. Güçlü bir asit (pKa ≈1) ve oksitleyici ajandır.

Perklorat, ClO4− formülüyle göserilen bir kimyasal kök. Bileşiklerinde daima bir adet elektron alır. Perkloratlar perklorik asitin tuzlarıdır. Perkloratlar özellikle tıpta tiroid bezleri tedavisinde kullanılmaktadır. Bunlarla beraber, hava yastığı ve havai fişek gibi bazı ürünlerde perkloratlara rastlanmaktadır.

Sodyum perklorat formülü NaClO4 olan bir kimyasal bileşiktir. Perklorik asitin sodyum tuzu olan bu bileşik diğer perkloratlar gibi kuvvetli bir oksitleyicidir. Sodyum perkloratın çözünürlüğü diğer perklorat tuzları içinde en yüksek olanıdır. Beyaz kristallerden oluşan ve higroskopik özellikte olan sodyum perklorat suda ve alkolde oldukça çok çözünür. Genellikle monohidrat form halinde bulunur ve rombik bir kristal yapısına sahiptir. Standart oluşum entalpisi −382.75 kJ mol−1 dir.

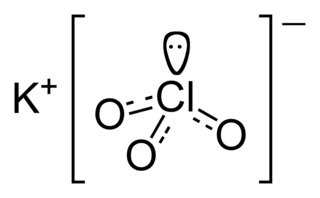
Potasyum perklorat formülü KClO4 olan bir kimyasal bileşiktir. Diğer perkloratlar gibi, bu tuz da güçlü bir oksitleyici olup potansiyel olarak birçok organik maddeyle reaksiyona girer. Havai fişek, mühimmat kapsülleri ve primer patlayıcılarda yaygın bir oksitleyici olarak kullanılan katı ve renksiz kristallerden oluşan bu madde çeşitli şekilde itici yakıtlar, flaş bileşimleri, yıldızlar ve maytaplarda da kullanılmaktadır. Daha yüksek performanslı amonyum perklorat yerine çoğu kez ikame edilerek katı yakıtlı roket itici yakıtı olarak da kullanılmıştır. KClO4 alkali metal perkloratlar içerisinde en düşük çözünürlüğe sahiptir (25 °C'deki 100 ml. suda 1.5 gr.).
Potasyum klorat formülü KClO3 olan bir kimyasal bileşiktir. Klorik asitin potasyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.

Baryum klorat formülü Ba(ClO3)2 olanbeyaz kristal yapıya sahip bir kimyasal bileşiktir. Tüm çözünür baryum bileşikleri gibi tahriş edici ve zehirlidir. Klorik asitin baryum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir. Bazen piroteknikte yeşil bir renk üretmek için kullanılır. Klorik asit üretiminde de kullanılır.

Sodyum klorat NaClO3 kimyasal formülüne sahip bir inorganik bileşiktir. Suda kolayca çözünür, beyaz kristal bir tozdur. Higroskopiktir. Sodyum klorat 300 °C’nin üzerinde ayrışarak oksijen ve sodyum klorür ortaya çıkar. Özellikle, çok parlak kâğıt imal etmek için ağartma hamurundaki uygulamalara yönelik olarak yılda birkaç yüz milyon ton üretilmektedir.
Magnezyum klorat formülü Mg(ClO3)2 olan bir kimyasal bileşiktir. Klorik asitin magnezyum tuzu olan bu bileşik diğer kloratlar gibi kuvvetli bir oksitleyicidir.
Bilinen inorganik ve organometalik bileşiklerin elementlere göre sıralanmış listesidir. Sıralama elementlerin kısaltmalarının alfabetik sırasına göredir.

Yükseltgen madde bir yükseltgenme-indirgenme (redoks) reaksiyonunda başka bir türden bir elektron alan element ya da bileşiktir. Yükseltgen maddelerin elektron kazandıklarından dolayı indirgendikleri söylenebilir.
Kalsiyum klorat kimyasal formülü Ca(ClO3)2 olan bir bileşiktir. Klorik asitin kalsiyum tuzudur. Potasyum klorat gibi, kuvvetli bir oksitleyici olan bu bileşik, piroteknik formülasyonlarda kullanılabilir. Kalsiyum klorat kuvvetle ısıtıldığında ya da organik madde gibi indirgeyici maddelerle karıştırıldığında patlayabilir.
Halojenür, bir kısmı halojen atom diğer kısmı ise halojenden daha az elektronegatif radikal veya element olan ikili bileşik. Uygun koşullar altında alkali metalleri halojenler ile direkt birleşerek genel formülü MX(X = F, Cl, Br veya I) olan halojenürleri oluştururlar. Çoğu tuz halojenürdür. Oda sıcaklığında bütün alkali metalleri beyaz katı halinde halojenürler oluştururlar.

Gümüş klorat (AgClO3) beyaz tetragonal kristaller formundadır. Tüm kloratlar gibi suda çözünür ve oksitleyici bir maddedir. Basit bir metal tuzu olarak, temel inorganik kimya deneylerinde kullanılan yaygın bir kimyasaldır. Işığa duyarlıdır, bundan dolayı oldukça koyu renkli kapalı kaplarda saklanmalıdır.

Kloril florür ClO2F formüllü bileşik. Sıklıkla klor florürlerinin oksijen kaynakları ile olan reaksiyonlarında yan ürün olarak görülür. Klorik asitin asil florürüdür.
Eksplosoforlar organik kimyada organik bileşiklere patlayıcı özellikler kazandıran fonksiyonel gruplardır.
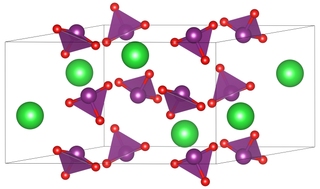
Baryum iyodat, kimyasal formülü Ba(IO3)2 olan inorganik bir kimyasal bileşiktir. Beyaz, granül bir maddedir.