
Pisagor teoremi veya Pisagor bağıntısı, Öklid geometrisinde üçgenin kenarları arasındaki temel ilişkiyi kuran ilk teoremlerden biridir. Teoreme gerçek hayattan örnek olarak telli çalgıları gösterilebilir; 'telin uzunluğu arttıkça titreşim artar' prensibine dayanır. Pisagor'un denklemi olarak da isimlendirilen bu teorem, a, b ve c kenarlarının arasındaki ilişkiyi şu şekilde açıklar:


Geometri, matematiğin uzamsal ilişkiler ile ilgilenen alt dalıdır. Yunanca Γεωμετρία "Geo" (yer) ve "metro" (ölçüm) birleşiminden türetilmiş bir isimdir.
Altın oran, matematikte iki miktardan büyük olanın küçüğe oranı, miktarların toplamının miktarları büyük olanına oranı ile aynı ise altın orandır. Altın oran aynı zamanda antik çağdan bu yana sanat ve mimaride en iyi uyum ve oranları veren düzen bağıntısı olarak kabul edilmekteydi.

Piramit, üçgen yüzler tek bir tepede birleşmek üzere n-köşeli bir çokgensel bir tabana oturtulmuş n+1 yüzü ve 2n ayrıtı olan polihedrondur. Piramitlerin isimlendirmesi tabanlarına göre yapılır. Örneğin tabanı kare olan piramit, kare piramit olarak adlandırılır. Tabanı dörtgen olan bir piramidin 5 yüzü vardır.

Bir kimyasal bileşiğin molekül kütlesi, bu bileşiğin bir molekülünün birleşik atom kütle birimi u cinsinden kütlesidir. Bağıl bir değer olduğundan bir maddenin molekül kütlesine yaygın olarak bağıl moleküler kütle denir ve Mr. diye de kısaltılır.

Salen, organometalik kimyada ve koordinasyon kimyasında kullanılan bir bileşiktir. İsmi salisilik aldehit ve etilendiamin kelimelerinin birleşmesinden meydana gelen bir kısaltmadır, çünkü bu bileşiklerin birleşmesi ile oluşmaktadır.
Değerlik kabuğu elektron çifti itmesi kuralları moleküllerin şekillerini tahmin etmede kullanılır ve değerlik elektron çiftlerinin birbirlerini elektrostatik kuvvetle itmesi temeline dayanır. Teorinin yaratıcısı olan bilim adamlarına atfen Gillespie–Nyholm teorisi olarak da adlandırılır. "VSEPR" kısaltması kimi zaman "vespır" olarak da telaffuz edilebilir.
Teoriye göre atomları çevreleyen değerlik elektron çiftleri birbirlerini iterek aralarındaki itme kuvvetini en aza indirirler ve böylece moleküle şeklini verirler. Merkez atoma bağlı atomların sayısı ile bağ yapmamış elektron çiftlerinin sayısının toplamı sterik numarayı verir.
Prizma ya da biçme, genelde en boy ve yükseklik kavramlarına sahip cisimler olarak adlandırılır. Ancak bazı cisimlerin (küre) en ve boyu tam olarak ifade edilememekle çap ve çevre de bu nicelikleri belirtmek için kullanılır.

Yükseklik cisimlerin referans alınan tabanından cismin tabana dik en uzak noktasıdır. Aynı zamanda yükseklik göreceli bir terimdir çünkü iki ve üç boyutlu cisimlerde değişebilmektedir. Bir örnek verecek olursak Bir kare piramidin yüksekliği tabanının(kare) merkezinden piramitin tepe noktasına çıkan bir doğru parçasıdır. Ancak yan yüzlerinin birindeki(üçgen) tabanından-ki bu taban iki boyutlu değildir bir boyutludur- tepesine bir dikme de yan yüz yüksekliği olarak tanımlanır.

Moleküler geometri molekülleri oluşturan atomların üç boyutlu uzaydaki dizilişidir. Kimyasal aktiflik, kimyasal polarite, faz, renk, manyetizma, biyolojik aktiflik gibi maddenin birçok özelliğini tanımlar. Atomların birbirleriyle oluşturduğu bağların arasındaki açı molekülün geri kalanıyla bağlantılıdır.

Kimyada, doğrusal moleküler geometri 180°'lik bir açıya yerleştirilmiş diğer iki atoma bağlanmış merkezi bir atom etrafındaki geometriyi tarif eder. Asetilen (HC≡CH) gibi doğrusal organik moleküller genellikle karbon merkezleri için sp orbital hibridizasyonu teşvik edilerek tarif edilir.
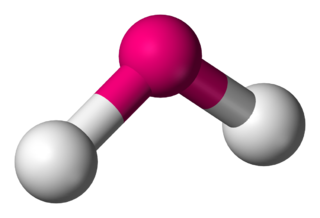
Kimyada, " açısal" ya da "bükülmüş" terimi bazı moleküllere moleküler geometrilerini tanımlamak için kullanılabilir. Oksijen gibi bazı atomlar, Elektron dizilimi nedeniyle hemen hemen her zaman iki (veya daha fazla) kovalent bağını doğrusal olmayan yönlerde ayarlarlar. Su (H2O), analoglarının yanı sıra açısal bir molekül örneğidir. İki hidrojen atomu arasındaki bağ açısı yaklaşık olarak 104,45°'dir. Doğrusal olmayan geometri genel olarak sadece ana grup elementleri içeren diğer üç atomlu molekülleri ve iyonlar için gözlemlenir, belirgin örnekler: Azot dioksit (NO2), kükürt diklorür (SCL2) ve metilen (CH2).

Kimyada, üçgen düzlemsel, merkezde bir atom ve birer üçgenin köşelerinde üç atom olan ve hepsi bir düzlemde çevresel atomlar olarak bulunduğu bir moleküler geometri modelidir. İdeal bir üçgen düzlemsel türde, üç ligand aynıdır ve bütün bağ açıları 120°'dir. Bu türler D3h nokta grubuna aittir. Üç ligandın aynı olmaadığı H2CO gibi moleküller, bu ideal geometri sapma gösterir. Üçgen düzlemsel bir şekle sahip moleküller arasında boron triflorür (BF3), formaldehit (H2CO), fosgen (COCl2) ve kükürt trioksit (SO3) bulunmaktadır. Üçgen düzlem geometrisi olan bazı iyonlar arasında nitrat (NO3-), karbonat (CO3−2) ve guanidinyum (C(NH2)3+)) bulunmaktadır. Organik kimyada, üçgen düzlemsel olarak karbon merkezlerine üç bağlı atomun bulunduğu moleküller çoğunlukla sp2 hibridizasyona sahip olarak tarif edilmiştir.

Kimyada üçgen piramit, apekste bir atomun ve dört yüzlüyü andıran üçgen temelin köşelerinde üç atomun bulunduğu moleküler geometridir (dörtyüzlü moleküler geometri ile karıştırılmamalıdır). Köşelerdeki üç atomun hepsi aynı olduğunda, molekül C3v nokta grubuna aittir. Üçgen piramit geometrisi olan bazı moleküller ve iyonlar; azot grubu hidritler (XH3), ksenon trioksit (XeO3), klorat iyonu ClO3- ve sülfit iyonu SO3−2. Organik kimyada, üçgen piramit geometriye sahip moleküller bazen sp3 hibridize olarak açıklanmaktadır. AXE yöntemi için Vsepr teori sınıflandırması AX3E1'dir.
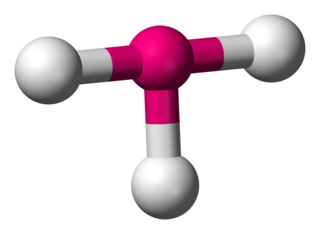
Kimyada, T-şeklindeki moleküler geometri, merkezi bir atomun üç liganda sahip olduğu bazı moleküllerin yapılarını açıklar. Normalde, üç koordineli bileşikler üçgen düzlemsel veya piramidal geometrileri kullanır. T-şekilli moleküllerin örnekleri arasında, halojen triflorürler vardır, örneğin ClF3.

Kimyada, üç kepli üçgen prizmatik moleküler geometri, dokuz atomun, atom grubunun veya ligandın merkezi bir atomun etrafına yerleştirildiği, üçgenselleştirilmiş üçgen bir prizmanın köşelerini tanımlayan bileşiklerin şeklini açıklar.

Kimyada, çift kepli üçgen prizmatik moleküler geometri, sekiz atom, atom grupları veya ligand gruplarının, çift-taraflı bir üçgen prizmanın köşelerini tanımlayan merkezi bir atomun etrafına yerleştirildiği bileşiklerin şeklini açıklar. Bu şekil, C2v olan simetri ile birlikte, okta-koordine geçiş metali kompleksleri için kare antiprizma ve onikiyüzlü ile birlikte üç genel biçimlerinden bir tanesidir.

Kimyada, onikiyüzlü moleküler geometri, sekiz atomun, atom gruplarının veya ligandların bir snub disfenojeninin köşelerini tanımlayan merkezi bir atomun etrafına yerleştirildiği bileşiklerin şeklini tarif eder. Bu şekil D2d simetriye sahiptir ve kare antiprizma ve çift kepli üçgen prizma ile birlikte oktakoordinat geçiş metali kompleksleri için üç ortak şekilden biridir.

Kare düzlemsel moleküler geometri, bazı bileşiklerde görülen ve molekülleri oluşturan atomların, merkezdeki bir atomun çevresinde bir kare oluşturacak şekilde bağlandığı moleküler geometri çeşididir. Trans- ve cis-PtCl2(NH3)2 bileşiklerinde gözlemlediği yapının ardından Alfred Werner tarafından ortaya atılmıştır.

Geometride adını Sakız Adalı Hipokrat'tan sonra alan Hipokrat ayı, iki çemberden oluşan yaylarla sınırlanmış bir aydır, daha küçük olanın çapı, daha büyük çember üzerinde dik bir açıyı kapsayan bir kirişe sahiptir.

















